原电池△G<0 化学能 2电能 电解池△G>0 T 负载 电极 电解质 多孔隔 溶液 阴 NaOH 阳 ZnSO CuSO 石棉隔膜 H20(0-→H2(g)+202(g) △G=-212 kJmol1 △G=237.2kJ.moll 电极:一般都由金属制成,属于电子导体(第一类导体) 电解质溶液:离子导体(第二类导体)。 6
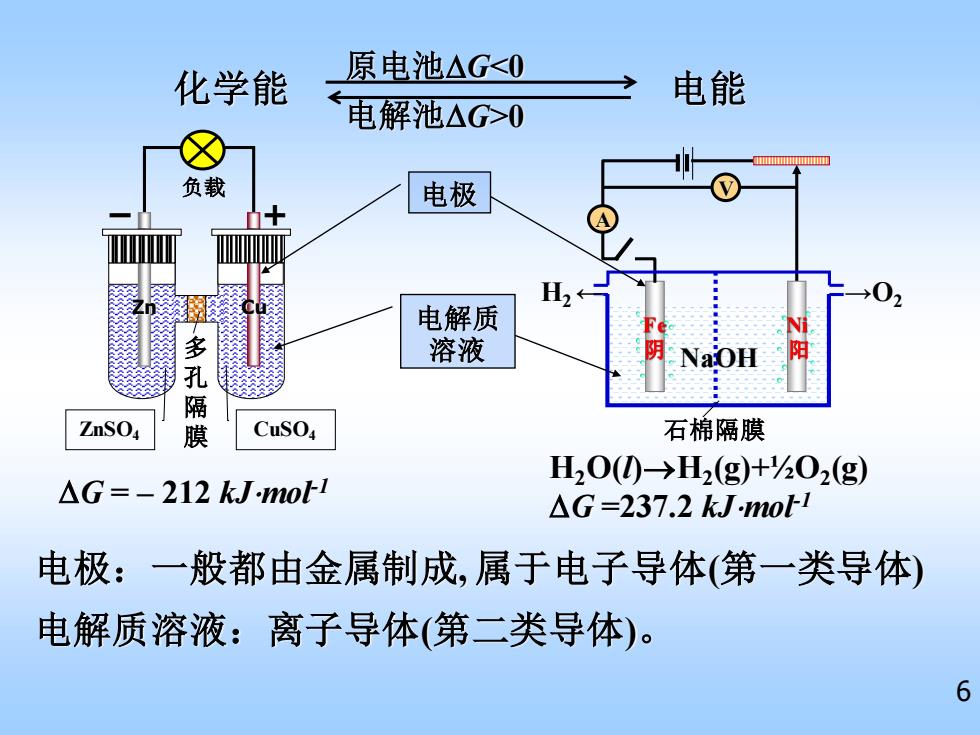
6 化学能 电能 原电池G<0 电解池G>0 G = – 212 kJmol-1 ZnSO4 CuSO4 Zn Cu – + 负载 多 孔 隔 膜 电极:一般都由金属制成, 属于电子导体(第一类导体) H2O(l)→H2 (g)+½O2 (g) G =237.2 kJmol-1 NaOH Fe 阴 Ni 阳 A V H2 ← →O2 石棉隔膜 电极 电解质 溶液 电解质溶液:离子导体(第二类导体)

1.电解质溶液的导电机理 1.1基本概念 (1)导体:能导电的物质称为导电体,通常分为两类: 第一类导体又称电子导体,如金属、石墨等 第一类导体的特点是: A.自由电子作定向移动而导电 B.导电过程中导体本身不发生变化 C.温度升高,电阻升高 7
7 A. 自由电子作定向移动而导电 B. 导电过程中导体本身不发生变化 第一类导体又称电子导体,如金属、石墨等 (1)导体:能导电的物质称为导电体,通常分为两类: 第一类导体的特点是: 1.电解质溶液的导电机理 1.1 基本概念 C. 温度升高,电阻升高

第二类导体又称离子导体,如电解质溶液、熔融电解质等 第二类导体的特点是 A.正、负离子作反向移动而导电,导电总量分别 由正、负离子分担 B.电解质溶液的连续导电过程必须在电化学装置中实现, 而且总是伴随有电化学反应和化学能与电能相互转换发 生。 C.温度升高,电阻下降 8
8 第二类导体又称离子导体,如电解质溶液、熔融电解质等 第二类导体的特点是: A. 正、负离子作反向移动而导电,导电总量分别 由正、负离子分担 B. 电解质溶液的连续导电过程必须在电化学装置中实现, 而且总是伴随有电化学反应和化学能与电能相互转换发 生。 C. 温度升高,电阻下降

1.1基本概念 (2)电极 正极、负极 正极: 电势高的极称为正极,电流从正极 流向负极。 负极: 电势低的极称为负极,电子从负极 流向正极。 9
9 正极、负极 电势低的极称为负极,电子从负极 流向正极。 负极: 电势高的极称为正极,电流从正极 流向负极。 正极: 1.1 基本概念 (2)电极

1.1基本概念 (2)电极 阴极、阳极 阴极: 发生还原作用的极称为阴极。 (Cathode) 阳极: 发生氧化作用的极称为阳极。 (Anode) 10
10 阴极、阳极 阴极: 发生还原作用的极称为阴极。 (Cathode) 发生氧化作用的极称为阳极。 阳极: (Anode) 1.1 基本概念 (2)电极