B Cu(OH)2-0.08Cu2O-0.358Cu Ag00.57_Ag200.344_Ag H2AuO3 0.7Au
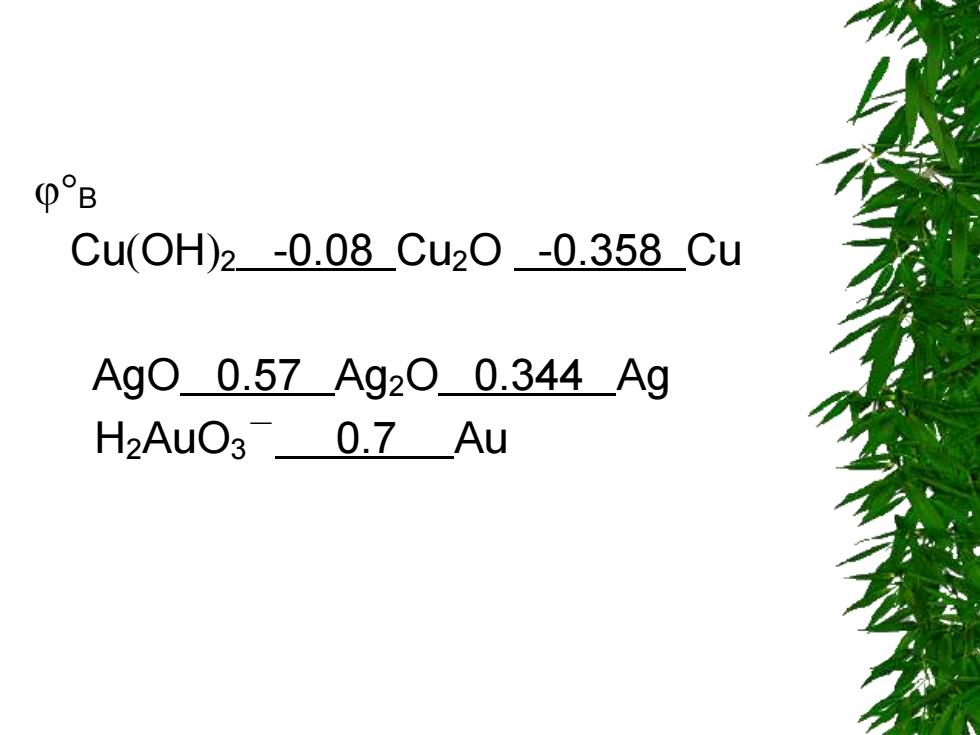
B Cu(OH)2 -0.08 Cu2O -0.358 Cu AgO 0.57 Ag2O 0.344 Ag H2AuO3 - 0.7 Au
Cu+Fe3+-→Cu2+Fe2+ Cut→Cu+Cu2+ Cu+HNO3(稀)→Cu2++NO+HO Cu+H2SO4(浓)→Cu2+SO2+H2O
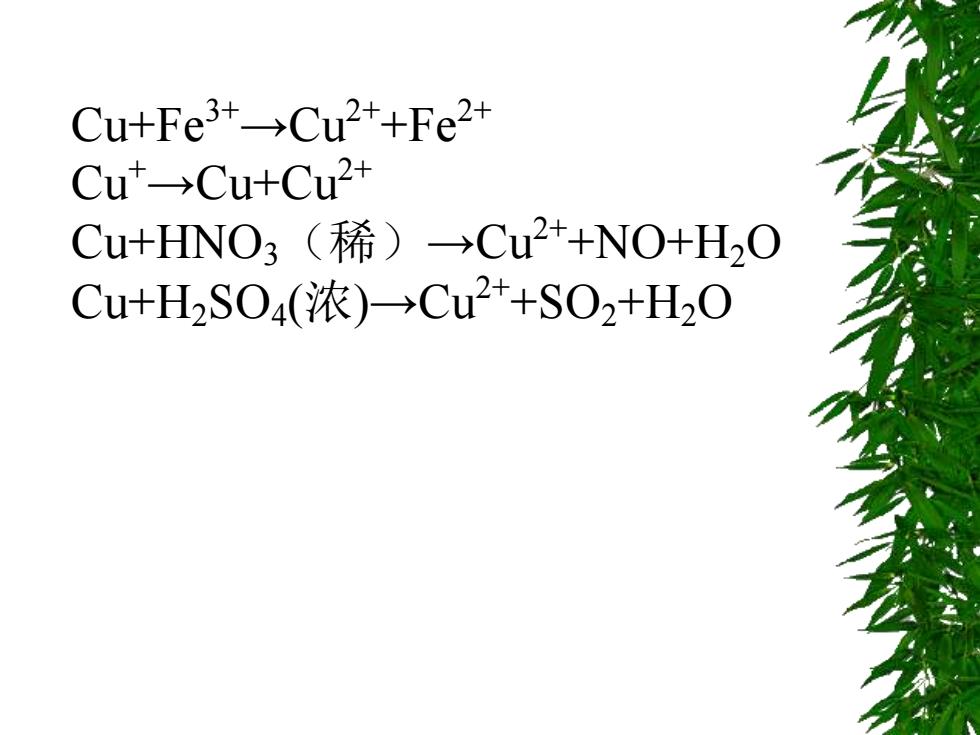
Cu+Fe3+→Cu2++Fe2+ Cu+→Cu+Cu2+ Cu+HNO3(稀)→Cu2++NO+H2O Cu+H2SO4(浓)→Cu2++SO2+H2O

铜外层电子:3dl4s1银:4d105s1金: 5d106s 从电子结构看它们的第一电离能较小( 比碱金属大的多),第二电离能就大的多 如11分别为:746、731、890,12:1958 、 2074、1980kJ●mo1-1 但为什么我们常见的是Cu+而不像Ag 呢? Cu2+水合热较大,为-2121kJmo1-1,可 促使二级电离
铜外层电子:3d 104s 1 银:4d 105s 1 金: 5d 106s 1 从电子结构看它们的第一电离能较小( 比碱金属大的多),第二电离能就大的多 ; 如I1分别为:746、731、890,I2:1958 、2074、1980 kJ•mol-1 但为什么我们常见的是Cu2+而不像Ag+ 呢? Cu2+水合热较大,为-2121 kJ•mol-1 ,可 促使二级电离

如果在没有水的环境中? 2Cuo >1273K>Cu20+1/202↑ 或碱性环境中也有利于生成+1价,Cu0 2Cu(OH)42-+C6H12O6=Cu20(红色) +2H20+C6H1207+40H 从金电势图看+1价金在酸介质也不稳定 3Au→2Au+Au3+
如果在没有水的环境中? 2CuO Cu2O +1/2O2↑ 或碱性环境中也有利于生成+1价,Cu2O 2Cu(OH)4 2-+C6H12O6 = Cu2O↓(红色) +2H2O+C6H12O7+4OH- 从金电势图看+1价金在酸介质也不稳定 3Au+ →2Au+Au3+ ⎯ ⎯1273 ⎯K →