
第七章 沉淀滴定法和重量分析法 化学分析 2.1银量法的基本原理 2.1.1滴定曲线 而Ag浓度则因为[Ag][C]=K。=1.8X10-10则 pAg pCI=-Igksp 9.74 故 pAg=9.74-2.28=7.46 同理,当加入AgN03溶液19.98mL时,溶液中剩余的C 浓度(mol/L)为 [C1-]=5.0×10-5 pC=4.30 pAg=5.51
化学分析 第七章 沉淀滴定法和重量分析法 而Ag+浓度则因为[Ag+][Cl- ] = Ksp = 1.8×10-10 则 pAg + pCl= -lgKsp = 9. 74 故 pAg = 9. 74-2.28 = 7.46 同理,当加入AgNO3 溶液19.98mL时,溶液中剩余的Cl- 浓度(mol/L)为 [Cl- ]=5.0×10-5 pCl =4.30 pAg = 5.51 2.1 银量法的基本原理 2.1.1 滴定曲线

第七章 沉淀滴定法和重量分析法 化学分析 2.1银量法的基本原理 2.1.1滴定曲线 (1)滴定开始至化学计量点前 (2)化学计量点时,溶液是AgCI的饱和溶液 PAg=pCI-PK-4.87 (3)化学计量点后,由过量AgNO3的量决定 例如,加入AgN03溶液20.02mL时(过量0.02mlL) 0.1000×0.02 [Ag*]= 20.00+20.02 =5.0×10 pAg=4.30 pC1=9.74-4.30=5.44
化学分析 第七章 沉淀滴定法和重量分析法 5.0 10 pAg 4.30 20.00 20.02 0.1000 0.02 [Ag ] 5 = = + = + − (3) 化学计量点后,由过量AgNO3的量决定 例如,加入AgNO3溶液20.02mL时(过量0.02mL) pCl = 9.74-4.30 = 5.44 2.1 银量法的基本原理 2.1.1 滴定曲线 (1) 滴定开始至化学计量点前 (2) 化学计量点时,溶液是AgCl的饱和溶液 sp 1 pAg pCl p 4.87 2 = = = K
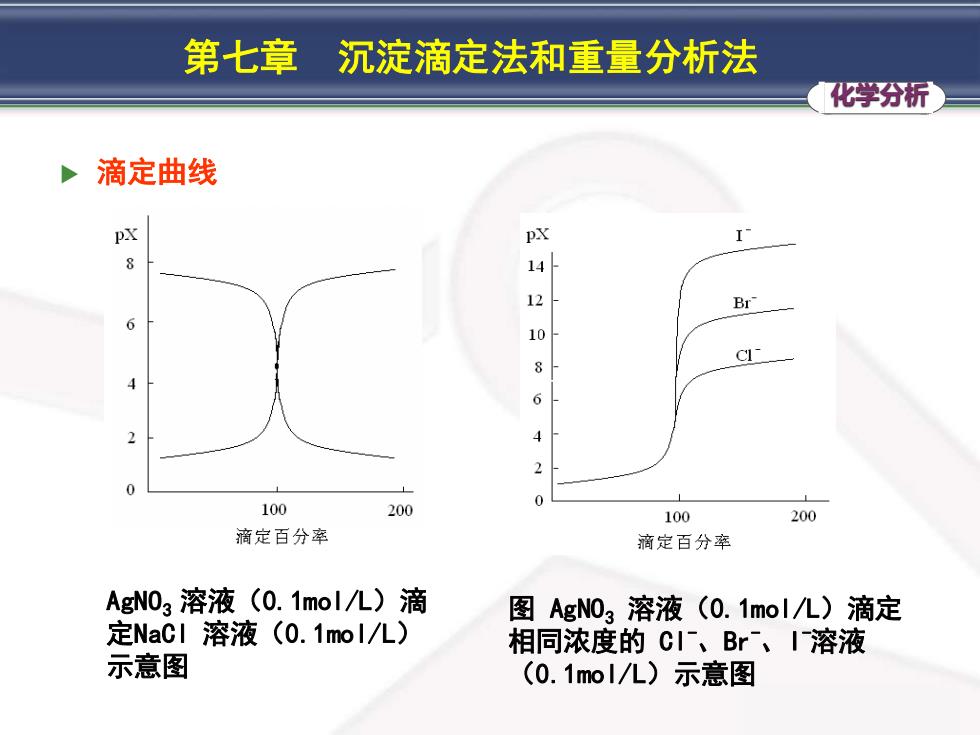
第七章 沉淀滴定法和重量分析法 化学分析 滴定曲线 pX pX Br 6 10 8 6 2 100 200 100 200 滴定百分率 滴定百分率 AgN03溶液(0.1mol/L)滴 图AgN03溶液(0.1mol/L)滴定 定NaCl溶液(0.1mol/L) 相同浓度的C、Br、I溶液 示意图 (0.1mol/八)示意图
化学分析 第七章 沉淀滴定法和重量分析法 滴定曲线 AgNO3 溶液(0.1mol/L)滴 定NaCl 溶液(0.1mol/L) 示意图 图 AgNO3 溶液(0.1mol/L)滴定 相同浓度的 Cl-、Br-、I -溶液 (0.1mol/L)示意图

第七章 沉淀滴定法和重量分析法 化学分析 由滴定曲线可以说明以下几点: >滴定曲线在化学计量点的附近形成滴定突跃。 突跃范围大小取决于沉淀的溶度积常数K。和溶 液浓度c。 100 200 滴定百分率 2.1.2分步滴定 CI厂、Br、I-可根据AgI、AgBr、 AgC1溶度积常数K。的差别进行分步滴定。 8 6 4 100 200 滴定百分率
化学分析 第七章 沉淀滴定法和重量分析法 由滴定曲线可以说明以下几点: ➢ 滴定曲线在化学计量点的附近形成滴定突跃。 ➢ 突跃范围大小取决于沉淀的溶度积常数Ksp 和溶 液浓度c。 2.1.2 分步滴定 Cl-、Br-、I - 可根据AgI、AgBr、 AgCl溶度积常数Ksp 的差别进行分步滴定

第七章 沉淀滴定法和重量分析法 化学分析 2.2银量法终点的指示方法 铬酸钾指示剂法(Mohr法) >铁铵钒指示剂法(Volhard法) 吸附指示剂法(Fajans法) 2.2.1铬酸钾指示剂法 (1)滴定原理 K,CrO,为指示剂,AgNO,液滴定CI和Br sp前:Ag+CI→AgC1↓(白色)Km=1.8×1010 sp:2Ag+Cr0→Ag2CrO4↓Km=1.2×1012 (砖红色)
化学分析 第七章 沉淀滴定法和重量分析法 K CrO 2 4 2.2 银量法终点的指示方法 铬酸钾指示剂法(Mohr 法) 铁铵钒指示剂法(Volhard 法) 吸附指示剂法(Fajans 法) 10 sp sp Ag Cl AgCl 1.8 10 K + − − 前 白色 : ( ) + → = 2- 12 4 2 4 sp sp 2Ag CrO Ag CrO 1.2 10 K + − : + → = (砖红色) 为指示剂, 2.2.1 铬酸钾指示剂法 (1) 滴定原理 AgNO Cl Br 3 液滴定 - - 和