
(2) 电化学极化电极反应总是分若于步进行,若其中一步反应速率较慢,需要较高的活化能为了使电极反应顺利进行所额外施加的电压称(亦称为活化超电势)为电化学超电势这种极化现象称为电化学极化
(2)电化学极化 电极反应总是分若干步进行,若其中一步反应 速率较慢,需要较高的活化能 为了使电极反应顺利进行所额外施加的电压称 为电化学超电势(亦称为活化超电势) 这种极化现象称为电化学极化
当有电流通过电极时,若电极-溶液界面处电极反应进行得不够快,导致电极带电程度的改变,使电极电势偏离可边。阴极反应:H++e-→1/2H,阳极反应:1/2Hz-e°→H*++++ HtHPtP不可逆,阴<可逆,阴P不可逆,阳>P可逆,阳
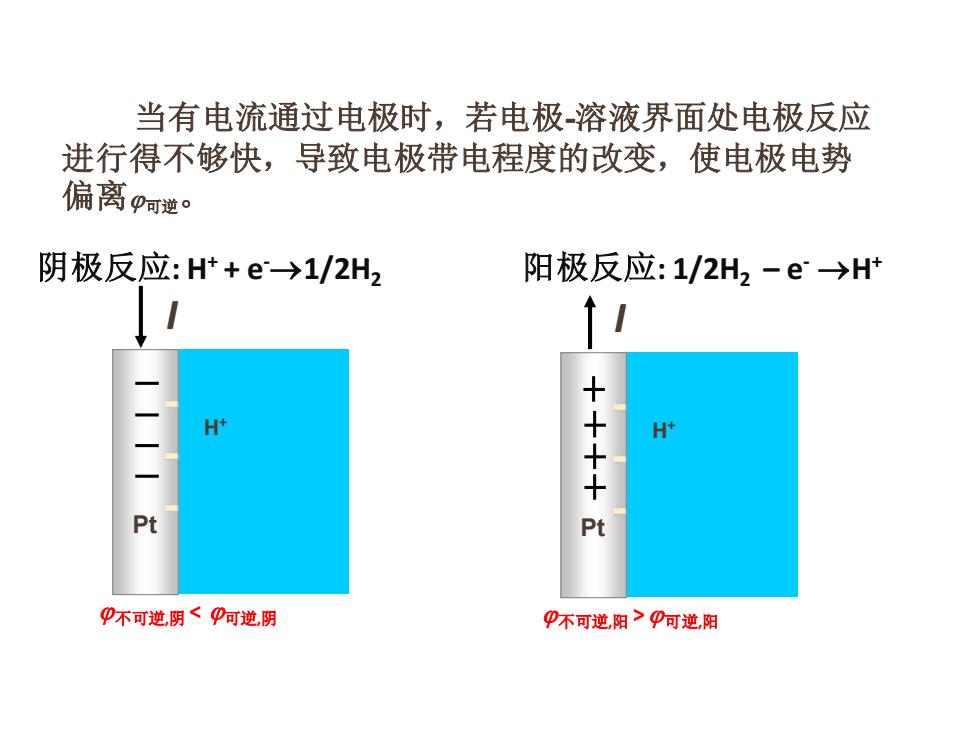
阴极反应: H+ + e-→1/2H2 阳极反应: 1/2H2 – e - →H+ 当有电流通过电极时,若电极-溶液界面处电极反应 进行得不够快,导致电极带电程度的改变,使电极电势 偏离 可逆。 不可逆,阴 < 可逆,阴 不可逆,阳 > 可逆,阳 Pt - - - I H+ Pt - - - I H+

2.超电势Φ不可逆在某一电流密度下,实际发生电解的电极电势与可逆电极电势可逆之间的差值称为超电势。阳极上由于超电势使电极电势变大,阴极上由于超电势使电极电势变小。和阳为了使超电势都是正值,把阴极超电势阴极超电势分别定义为:N阳n阴 =(β)一β不可逆阴可逆(不可逆N阳 =一可逆阳
为了使超电势都是正值,把阴极超电势 和阳 极超电势 分别定义为: 阴 阳 阳极上由于超电势使电极电势变大,阴极上由于 超电势使电极电势变小。 阴 阴 = − ( ) 可逆 不可逆 2.超电势 阳 阳 = − ( ) 不可逆 可逆 在某一电流密度下,实际发生电解的电极电势 与可逆电极电势 之间的差值称为超电势。 不可逆 可逆
2.1超电势的测定设测量电极1的超电势(1)将电极1与辅助电极2组成一个电解池。调节电阻,改变通过电极的电流大小。二电位计电极电极(2)将待测电极与甘汞电极2组成原电池,测量12该电池的电动势,可求出待测电极的电极电势。甘汞电极(3)每改变一次电流密度,可测出待测电极的一个稳定的电势值
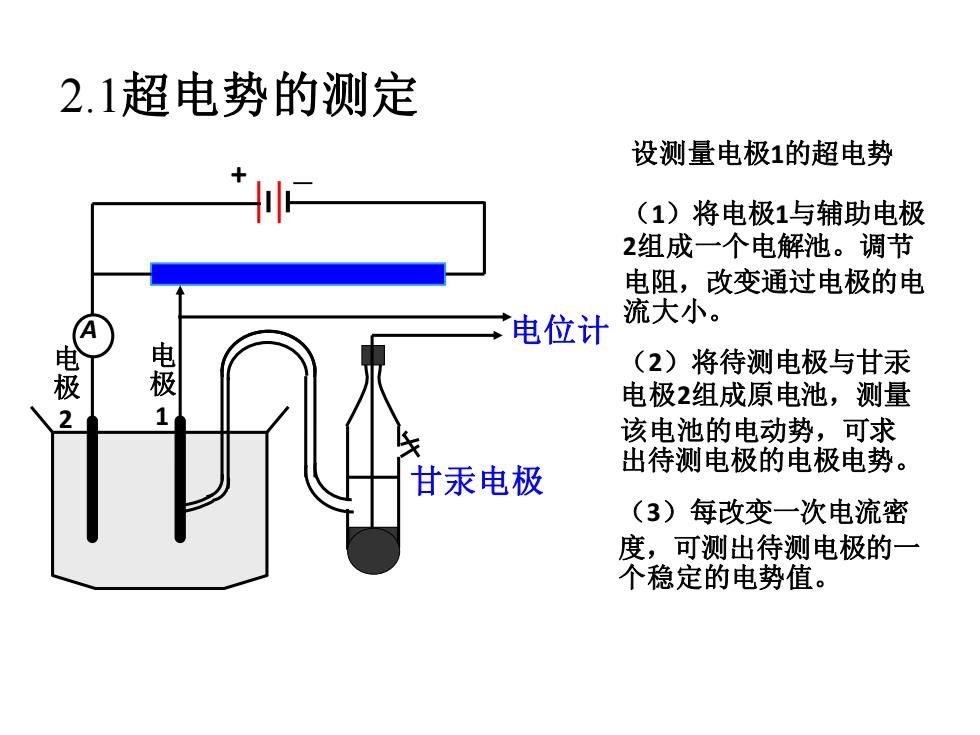
甘汞电极 电位计 电 极 1 电 极 2 A + − 2.1超电势的测定 设测量电极1的超电势 (1)将电极1与辅助电极 2组成一个电解池。调节 电阻,改变通过电极的电 流大小。 (2)将待测电极与甘汞 电极2组成原电池,测量 该电池的电动势,可求 出待测电极的电极电势。 (3)每改变一次电流密 度,可测出待测电极的一 个稳定的电势值
2.2极化曲线(polarization curve)超电势或电极电势与电流密度之间的关系曲线称为极化曲线,木极化曲线的形状和变化规律反映了电化学过程的动力学特征。β(阴)PrPrβ(阳)
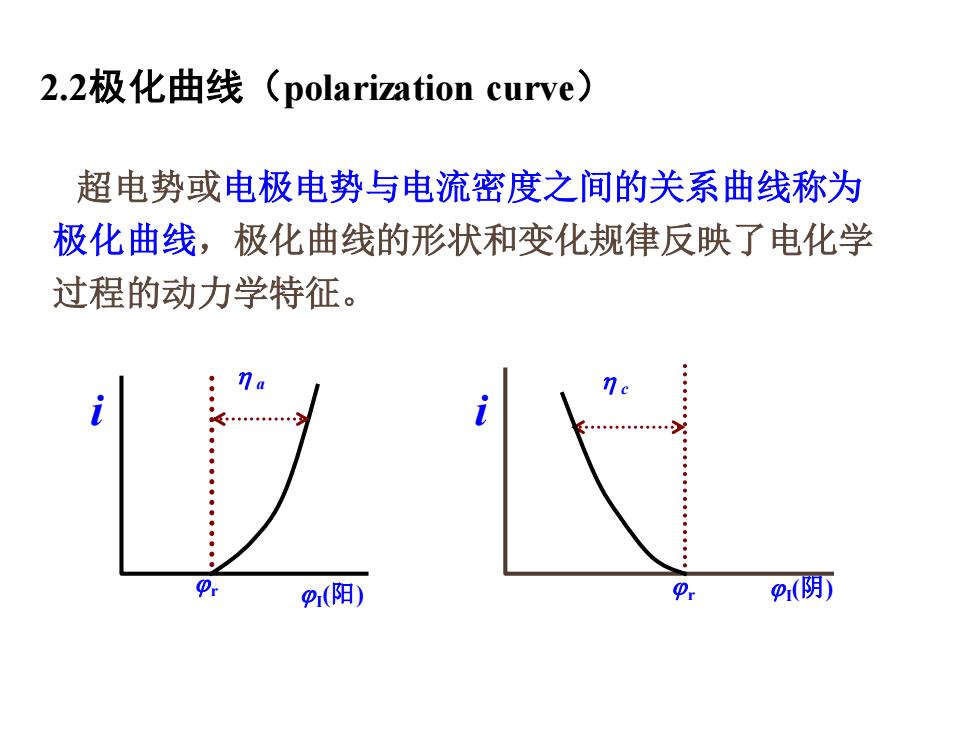
2.2极化曲线(polarization curve) 超电势或电极电势与电流密度之间的关系曲线称为 极化曲线,极化曲线的形状和变化规律反映了电化学 过程的动力学特征。 i r a I (阳) i r I (阴) c