
四、电极上半反应的电极电位(E) 电池中发生的反应是氧化还原反应,常用 氧化半反应和还原半反应来表示,分别构成两 个电极。电极上每个半反应的电极电位(E) 与溶液中对应离子活度之间的关系由能斯特方 程(Nernst equation)表示: 若某一电极上半反应的方程式为: Ox+ne Red 则其电极电位为 E=E+ RT dox nF aRed
四、电极上半反应的电极电位(E ) 电池中发生的反应是氧化还原反应,常用 氧化半反应和还原半反应来表示,分别构成两 个电极。电极上每个半反应的电极电位(E ) 与溶液中对应离子活度之间的关系由能斯特方 程(Nernst equation )表示: 若某一电极上半反应的方程式为: Ox + ne Red 则其电极电位为 a a d O x nF RT E E Re = + ln

五、电极的类型 1、基于电子交换反应的电极 (1)第一类电极:Mn+/M (2)第二类电极:M/MX (固体) (3)第三类电极:M/MX(S),NX(s),Nn*+ (4)第零类电极:惰性金属 2、选择性电极(ion selective electrode,ISE)
五、电极的类型 1、基于电子交换反应的电极 (1) 第一类电极: M n+/M (2) 第二类电极: M/MX(固体) (3) 第三类电极: M/MX (s),NX (s),N n+ (4) 第零类电极: 惰性金属 2、选择性电极(ion selective electrode, ISE)

§4-2电位分析法原理 电位分析法(potentiometry):是基于测量浸 入被测液中两电极间的电位差(电动势)来进行 测定的一种电化学分析法。包括直接电位法和间 接电位法(电位滴定法)。 直接电位法:是将电极插入被测液中构成原电池, 根据原电池的电动势与被测离子活度间的函数关 系直接测定离子活度的方法。 电位滴定法:是借助测量滴定过程中电池电动 势的突变来确定滴定终点,再根据反应计量关系 进行定量的方法
§4-2 电位分析法原理 电位分析法(potentiometry):是基于测量浸 入被测液中两电极间的电位差(电动势)来进行 测定的一种电化学分析法。包括直接电位法和间 接电位法(电位滴定法)。 直接电位法:是将电极插入被测液中构成原电池, 根据原电池的电动势与被测离子活度间的函数关 系直接测定离子活度的方法。 电位滴定法: 是借助测量滴定过程中电池电动 势的突变来确定滴定终点,再根据反应计量关系 进行定量的方法
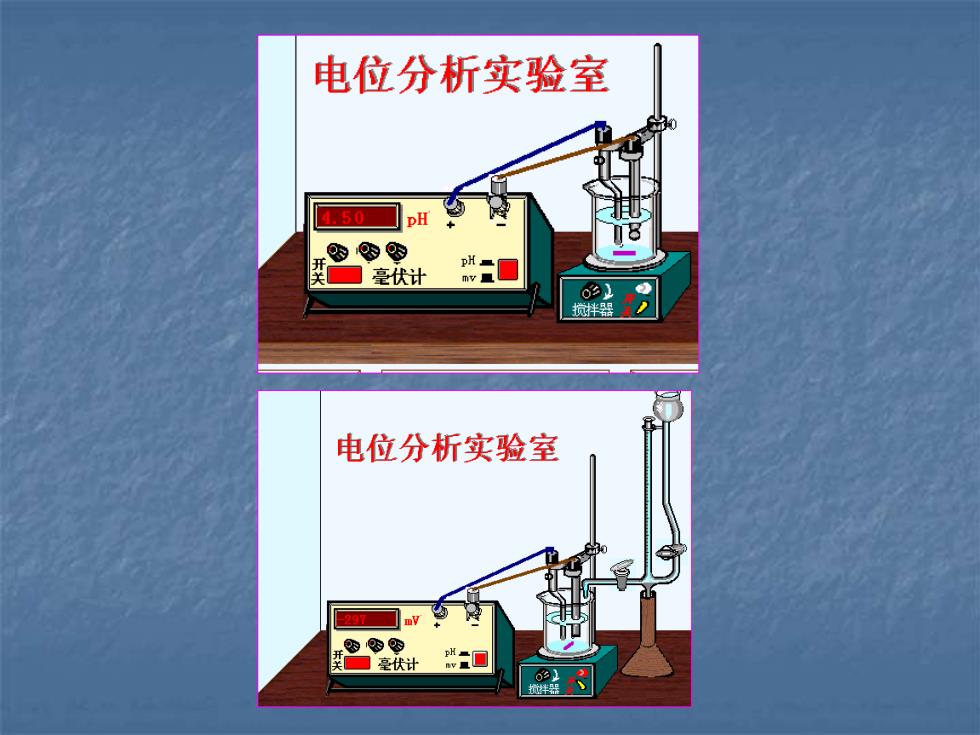
电位分析实验室 50 ]毫伏计 02 搅拌器 电位分析实验室 关☐毫伏计

原电池的原理:在零电流条件下测定两电极间 的电位差,即为所构成原电池的电动势。 组成测量原电池的电极:指示电极和参比电极。 E电池=E正极一E负极+△E相间电位 若参比电极的电极电位保持不变,则测得电池 的电动势就仅与指示电极有关,进而也就与被测 离子活度有关。 E=E+ RT In Cox nF aRed
原电池的原理:在零电流条件下测定两电极间 的电位差,即为所构成原电池的电动势。 组成测量原电池的电极:指示电极和参比电极。 若参比电极的电极电位保持不变,则测得电池 的电动势就仅与指示电极有关,进而也就与被测 离子活度有关。 a a d O x nF RT E E Re = + ln E 电池 = E 正极 − E 负极 + E 相间电位