2.熵的引出移项得:6000R(%)R21R2()R,=(RIP说明任意可逆过程的热温商的B值决定于始终状态,而与可逆途径任意可逆过程无关,这个热温商具有状态函数的性质
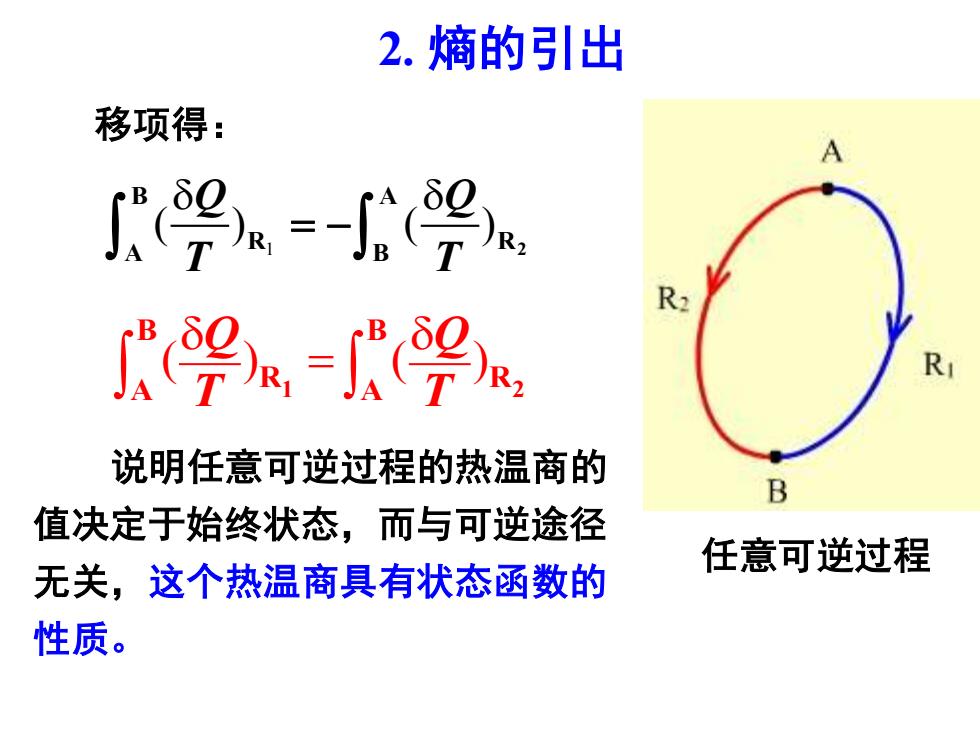
2. 熵的引出 说明任意可逆过程的热温商的 值决定于始终状态,而与可逆途径 无关,这个热温商具有状态函数的 性质。 移项得: ( ) ( ) Q Q T T = 1 2 B B R R A A 任意可逆过程 1 ( ) ( ) 2 B A R R A B Q Q T T = −

2.炳的引出Clausius根据可逆过程的热温商值决定于始终态而与这“炳”可逆过程无关这一事实定义了(entropy)个函数,用符号“S"表示,单位为:J·K-I设始、终态A,B的炳分别为SA和SB,则:-()S-S=AS=-(%) =060AS-或N(AS =o对微小变化dS:=这几个摘变的计算式习惯上称为炳的定义式即的变化值可用可逆过程的热温商值来衡量
Clausius根据可逆过程的热温商值决定于始终态而与 可逆过程无关这一事实定义了“熵”(entropy)这 个函数,用符号“S”表示,单位为: 1 J K− ( ) Q S T 对微小变化 d = R 这几个熵变的计算式习惯上称为熵的定义式, 即熵的变化值可用可逆过程的热温商值来衡量。 ( ) Q S S S T − = = B B A R A ( )i i i Q S T − = R ( )i 0 i i Q S T 或 = R 设始、终态A,B的熵分别为 SA 和 SB ,则: 2. 熵的引出

2.滴的引出说明:(1)熵是状态函数,广度性质;(2)公式中的温度为环境温度,在可逆过程中也是系统的温度;(3)4S计算需通过可逆过程进行,但并不是只有可逆过程才有变。不可逆过程的需要通过在同样的始终态间设计可逆途径来计算
2. 熵的引出 说明: (1)熵是状态函数,广度性质; (2)公式中的温度为环境温度,在可逆过程中 也是系统的温度; (3)ΔS计算需通过可逆过程进行,但并不是只 有可逆过程才有熵变。不可逆过程的需要通过 在同样的始终态间设计可逆途径来计算

3.5 Clausius不等式与摘增加原理不等式Clausius热力学第二定律的数学表达式滴增加原理
§3.5 Clausius 不等式与熵增加原理 Clausius 不等式—— 热力学第二定律的数学表达式 熵增加原理

1.Clausius不等式设温度相同的两个高、低温热源间有一个可逆热机和一个不可逆热机。TQT-TQn + Q则:nTNR :TQnQnT.ni<nR根据Carnot定理:Q.则Qh<0T.T推广为与n个热源接触的任意不可逆过程,得:(2%)<0
1. Clausius 不等式 设温度相同的两个高、低温热源间有一个可逆 热机和一个不可逆热机。 T T T T T − = = − h c c R h h 1 根据Carnot定理: I R Q Q T T + c h c h 则 0 I 0 n i i i Q T < 推广为与n个热源接触的任意不可逆过程,得: h c c I h h 1 Q Q Q Q Q + 则: = = +