
第四章食品添加剂含量的检测 实验一苯甲酸、山梨酸含量的检测 【、气相色谱法 一、目的与要求 1、了解气相色谱仪的基本原理及分析流程。 2、掌握气相色谱分析法操作技术。 3、掌握外标法定量的方法。 二、原理 样品酸化后,用乙醚提取山梨酸、苯甲酸,经浓缩后,用附氢火焰离子化检测器的气相 色谱仪进行分离测定,用外标法与标准系列比较定量。 三、仪器与试剂 1、仪器 (1)气相色谱仪,带有氢火焰离子化检测器: (2)具塞量简: (3)10mL具塞刻度试管或10mL容量瓶: (4)常用玻璃仪器: 2、试剂: (1)乙醚:不含过氧化物。 (2)石油醚:沸程30~60℃。 (3)盐酸(1+1): (4)石油醚一乙涨(3+1)混合液 (5)氯化钠酸性溶液(40g几):于氯化钠溶液(40g几)中加少量盐酸(1+1)酸化 (6)无水 酸钠 分析纯)。 (7)苯甲酸、山梨酸标准贮备液: 精密称取苯甲酸、山梨酸各0.2000g,置于100mL容量瓶中,用石油醚一乙醚(3+1) 混合溶剂溶解后并定容至刻度,混匀,此溶液每毫升相当于2mg苯甲酸或山梨酸。 (8)材料:饮料 四、测定步骤 1、样品的提取: 吸取10.00mL均匀饮料(如样品中含有二氧化碳,先加热除去),放入150mL分液漏斗中, 加1:1盐酸2mL,用15、10mL乙醚提取两次,每次振摇1min,将上层醚提取液吸入另 个25mL带塞量筒中, 合并乙醚提取液。用3mL氯化钠酸性 40gL)洗涤两次,静止 15min,用滴管将乙醚层通过无水硫酸钠滤入25mL容量瓶中。加乙醚至刻度,混匀。准确 吸取5.0mL乙酰提取液于10mL带塞离心管中,置40℃的水浴上挥干,加入2mL石油醚-乙 醚(3+1)混合溶剂溶解残渣,密塞保存备用
第四章 食品添加剂含量的检测 实验一 苯甲酸、山梨酸含量的检测 Ⅰ、气相色谱法 一、目的与要求 1、了解气相色谱仪的基本原理及分析流程。 2、掌握气相色谱分析法操作技术。 3、掌握外标法定量的方法。 二、原理 样品酸化后,用乙醚提取山梨酸、苯甲酸,经浓缩后,用附氢火焰离子化检测器的气相 色谱仪进行分离测定,用外标法与标准系列比较定量。 三、仪器与试剂 1、 仪器 (1)气相色谱仪,带有氢火焰离子化检测器; (2)具塞量筒; (3)10mL 具塞刻度试管或 10 mL 容量瓶; (4)常用玻璃仪器; 2、 试剂: (1)乙醚:不含过氧化物。 (2)石油醚:沸程 30~60℃。 (3)盐酸(1+1): (4)石油醚-乙醚(3+1)混合液: (5)氯化钠酸性溶液(40g /L):于氯化钠溶液(40g /L)中加少量盐酸(1+1)酸化。 (6)无水硫酸钠(分析纯)。 (7)苯甲酸、山梨酸标准贮备液: 精密称取苯甲酸、山梨酸各 0.2000g,置于 100mL 容量瓶中,用石油醚-乙醚(3+1) 混合溶剂溶解后并定容至刻度,混匀,此溶液每毫升相当于 2mg 苯甲酸或山梨酸。 (8)材料:饮料 四、测定步骤 1、 样品的提取: 吸取 10.00mL 均匀饮料(如样品中含有二氧化碳,先加热除去),放入 150mL 分液漏斗中, 加 1:1 盐酸 2mL,用 15、10mL 乙醚提取两次,每次振摇 1min,将上层醚提取液吸入另一 个 25mL 带塞量筒中,合并乙醚提取液。用 3mL 氯化钠酸性溶液(40g/L)洗涤两次,静止 15min,用滴管将乙醚层通过无水硫酸钠滤入 25mL 容量瓶中。加乙醚至刻度,混匀。准确 吸取 5.0mL 乙醚提取液于 10mL 带塞离心管中,置 40℃的水浴上挥干,加入 2mL 石油醚-乙 醚(3+1)混合溶剂溶解残渣,密塞保存备用
2、色谱条件 (1)色谱柱:玻璃柱,内径3mm,长2m,内装涂以质量分数为5%DEGS+1%HPO4固定 液的60 30目chromosorbWAW (2)气体流速:载气为氮气,50 mI/min(氨气和空气、氢气之比按各仪器型号不同选择名 自的最佳比例条件)。 (3)灵敏度:1000 (4)温度:进样口(气化温度)230℃:柱温170℃:监测器230℃ 3、测定 (1)取6支10mL容量瓶,编号,并按下表操作记录。 编号 1 2 3 试剂 取苯甲酸或山梨酸标准0.25 075 100 125 溶液(mL) 相当于苯甲酸或山梨酸50 100 150 200 250 量(ug) 取样品乙醚提取液体积 (mL) 用石油醚定容(mL) 10 10 10 10 10 进样量(L) 2 2 2 2 2 测定峰高值 (2)以苯甲酸或山梨酸量(g)为横坐标,与其对应的峰高值为纵坐标,绘制标准曲线。 (3)用样品测得峰高值与标准曲线比较定量, 五、结果计算 X= A×1000 m×3××100 25 式中 一样品中苯甲酸或山梨酸的含量。 g/kg: A 一测定用样品液中苯甲酸或山梨酸的含量,g: V,一一样品提取液残留物定容的体积,L: V2一一进样体积,L: m一一样品质量.,g或mL: 525.-测定时吸取乙酰提取液的体积(mL)样品乙醚提取液的总体积(mL) 六、注意事项 1、由测得的苯甲酸的量乘以1.18,即为样品中苯甲酸钠的含量。 2、样品处理时酸化可使山梨酸钾、苯甲酸钠转变为山梨酸、苯甲酸。 3、乙醚提取液应用无水硫酸钠充分脱水,进样溶液中含水会影响测定结果 4、气相色谱仪的操作按仪器操作说明进 注意:点火前严禁打开氨气调节阀,以避免氢气逸出引起爆炸:点火后,不允许再转动放大 调零旋钮
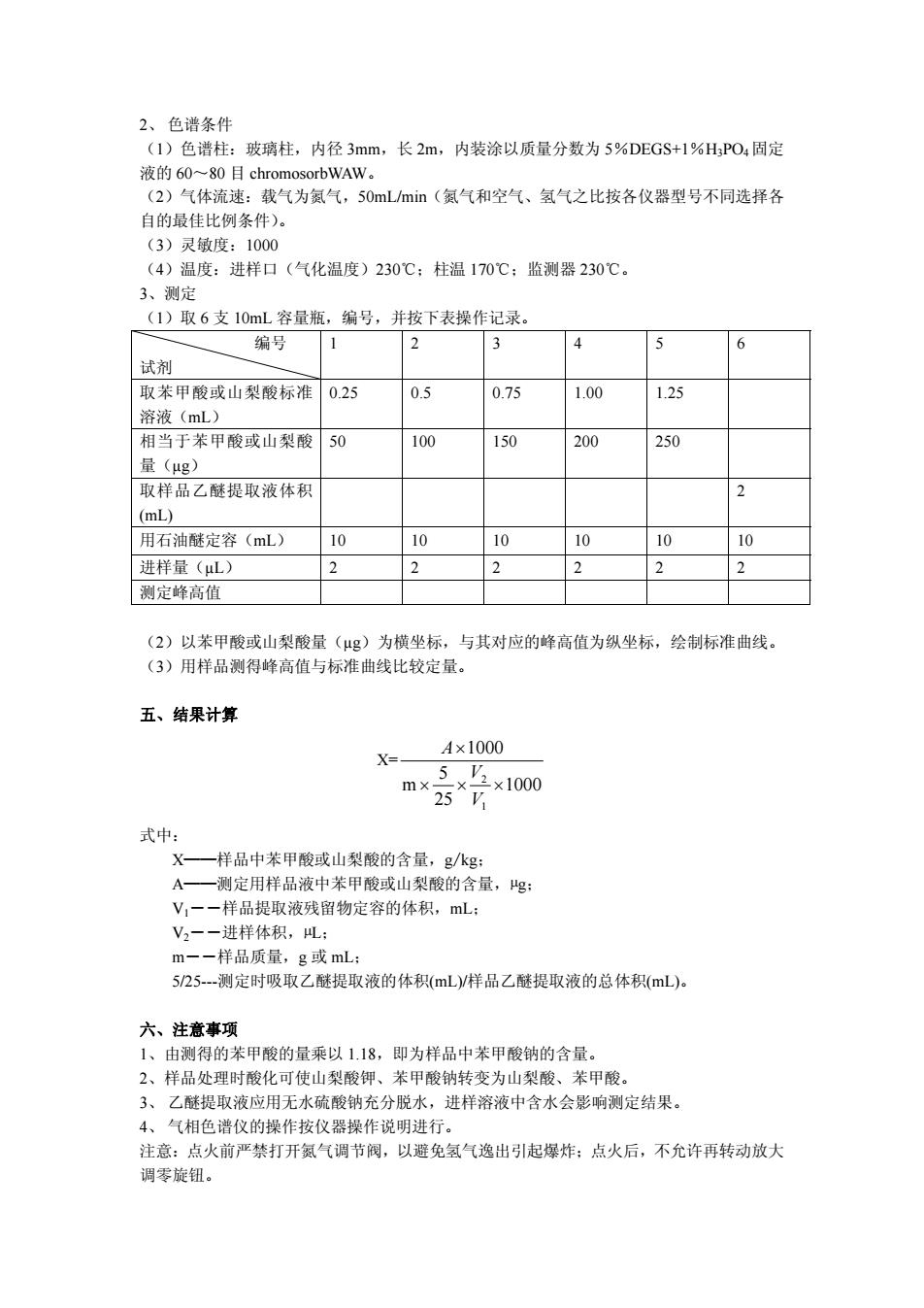
2、 色谱条件 (1)色谱柱:玻璃柱,内径 3mm,长 2m,内装涂以质量分数为 5%DEGS+1%H3PO4固定 液的 60~80 目 chromosorbWAW。 (2)气体流速:载气为氮气,50mL/min(氮气和空气、氢气之比按各仪器型号不同选择各 自的最佳比例条件)。 (3)灵敏度:1000 (4)温度:进样口(气化温度)230℃;柱温 170℃;监测器 230℃。 3、测定 (1)取 6 支 10mL 容量瓶,编号,并按下表操作记录。 编号 试剂 1 2 3 4 5 6 取苯甲酸或山梨酸标准 溶液(mL) 0.25 0.5 0.75 1.00 1.25 相当于苯甲酸或山梨酸 量(µg) 50 100 150 200 250 取样品乙醚提取液体积 (mL) 2 用石油醚定容(mL) 10 10 10 10 10 10 进样量(µL) 2 2 2 2 2 2 测定峰高值 (2)以苯甲酸或山梨酸量(µg)为横坐标,与其对应的峰高值为纵坐标,绘制标准曲线。 (3)用样品测得峰高值与标准曲线比较定量。 五、结果计算 X= 1000 25 5 m 1000 1 2 × × × × V V A 式中: X——样品中苯甲酸或山梨酸的含量,g/kg; A——测定用样品液中苯甲酸或山梨酸的含量,µg; V1――样品提取液残留物定容的体积,mL; V2――进样体积,µL; m――样品质量,g 或 mL; 5/25-测定时吸取乙醚提取液的体积(mL)/样品乙醚提取液的总体积(mL)。 六、注意事项 1、由测得的苯甲酸的量乘以 1.18,即为样品中苯甲酸钠的含量。 2、样品处理时酸化可使山梨酸钾、苯甲酸钠转变为山梨酸、苯甲酸。 3、 乙醚提取液应用无水硫酸钠充分脱水,进样溶液中含水会影响测定结果。 4、 气相色谱仪的操作按仪器操作说明进行。 注意:点火前严禁打开氮气调节阀,以避免氢气逸出引起爆炸;点火后,不允许再转动放大 调零旋钮

Ⅱ、薄层色谱法 一、目的与要求 1、学习薄层色谱法分离食品中苯甲酸、山梨酸的基本原理。 2、堂握薄层色谱法的基本操作技术。 二、实验原理 试样酸化后,用乙醚提取苯甲酸、山梨酸。将试样提取液浓缩,点于聚酰胺薄层板上 展开。显色后,根据薄层板上苯甲酸、山梨酸的比移值。与标准比较定性,并可进行半定量。 三、仪器与试剂 1、仪器 (1)吹风知 (2)层析缸 (3)玻璃板:10cm×18cm: (4)微量注射器:10L、100L: (5)喷雾器。 2、试剂 (1)异丙醇。 (2)正丁醇。 (3)石油醚:沸程30~60℃。 (4)乙醚:不含过氧化物。 (5)氨水 (6)无水乙醇 (7)聚酰胺粉:200目。 (8)盐酸(1+1):取100mL盐酸,缓慢顺入水中,并稀释至200mL。 (9)氯化钠酸性溶液(401L):于氯化钠溶液(401)中加入少量盐酸(1+1)酸化 (10)展开剂如下 ①正丁醇+氨水+无水乙醇(7+1+2) ②异丙醇+氨水+无水乙醇(7+1+2) (11)山梨酸标准溶液:准确称取0.2000g山梨酸,用少量乙醇溶解后移入100mL容量瓶 中,并稀释至刻度,此溶液每毫升相当于2.0mg山梨酸。 (12)苯甲酸标准溶液:准确称取0.2000g苯甲酸,用少量乙醇溶解后移入100mL容量瓶 中,并稀释至刻度 溶液每毫升相当于2.0mg苯甲酸 (13)显色剂:称取溴甲酚紫0.04g以(50%)乙醇溶解并稀释至100mL,用氢氧化钠溶液 (4g/L)调至DH=8。 四、烈定步骤 样品提取:同色谱法“四、1” (1)满层板的制备:称取1.6g聚酰胺粉,加0.4g可溶性淀粉,加约15mL水,研磨3min 5min,立刻倒入涂布器内制成10cm×18cm、厚度0.3mm的薄层板两块,室温干燥后,于
Ⅱ、薄层色谱法 一、目的与要求 1、学习薄层色谱法分离食品中苯甲酸、山梨酸的基本原理。 2、掌握薄层色谱法的基本操作技术。 二、实验原理 试样酸化后,用乙醚提取苯甲酸、山梨酸。将试样提取液浓缩,点于聚酰胺薄层板上, 展开。显色后,根据薄层板上苯甲酸、山梨酸的比移值。与标准比较定性,并可进行半定量。 三、仪器与试剂 1、 仪器 (1)吹风机; (2)层析缸; (3)玻璃板:10cm×18cm; (4)微量注射器:10µL、100µL; (5)喷雾器。 2、试剂 (1)异丙醇。 (2)正丁醇。 (3)石油醚:沸程 30~60℃。 (4)乙醚:不含过氧化物。 (5)氨水。 (6)无水乙醇。 (7)聚酰胺粉:200 目。 (8)盐酸(1+1):取 100mL 盐酸,缓慢倾入水中,并稀释至 200mL。 (9)氯化钠酸性溶液(40g/L):于氯化钠溶液(40g/L)中加入少量盐酸(1+1)酸化。 (10)展开剂如下: ①正丁醇+氨水+无水乙醇(7+1+2) ②异丙醇+氨水+无水乙醇(7+1+2) (11)山梨酸标准溶液:准确称取 0.2000g 山梨酸,用少量乙醇溶解后移入 100mL 容量瓶 中,并稀释至刻度,此溶液每毫升相当于 2.0mg 山梨酸。 (12)苯甲酸标准溶液:准确称取 0.2000g 苯甲酸,用少量乙醇溶解后移入 100mL 容量瓶 中,并稀释至刻度,此溶液每毫升相当于 2.0mg 苯甲酸。 (13)显色剂: 称取溴甲酚紫 0.04g 以(50%)乙醇溶解并稀释至 100mL,用氢氧化钠溶液 (4g/L)调至 pH=8。 四、测定步骤 1、 样品提取:同色谱法“四、1” 2、样品测定 (1)薄层板的制备: 称取 1.6g 聚酰胺粉,加 0.4g 可溶性淀粉,加约 15mL 水,研磨 3min~ 5min,立刻倒入涂布器内制成 10cm×18cm、厚度 0.3mm 的薄层板两块,室温干燥后,于

80℃干燥1h.取出,置于千燥器中保存, (2)点样:在海层板下端2cm的基线上,用微量注射器点10uL,20uL试样液,同时各点10uL 20uL山梨酸 苯甲酸标 (3)展开与显色:将点样后的薄层板放入预先盛有展开剂(10.①或10.②)的展开槽内,周 围贴有滤纸,待溶剂前沿上展至10cm,取出挥干,喷显色剂,斑点成黄色,背景为蓝色。 试样中所含山梨酸、苯甲酸的量与标准斑点比较定量(山梨酸、苯甲酸的比移值依次为0.82、 0.73)。 五、结果计算 试样中苯甲酸或山梨酸的含量按下式进行计算。 A×1000 X=- 10××1000 25V 式中: X一试样中苯甲酸或山梨酸的含量,单位为克每千克(gkg): A一测定用试样液中苯甲酸或山梨酸的质量,单位为毫克(mg): 加入乙醇的体积,单位为亮升(mL): Vz- -测定时点样的体积,单位为毫升(mL), m一试样质量,单位为克(g): 10一测定时吸取乙醚提取液的体积,单位为毫升(mL): 25 一试样乙醚提取液总体积,单位为毫升(mL): 六、注意事项 1、层析用的溶剂系统不可存放太久,否则浓度和极性都会变化,影响分离效果,应新鲜配 用制。 2、在展开之前,展开剂在缸中应预先平衡1h,使缸内蒸气压饱和,以免出现边缘效应。 3、展开剂液层高度不能超过原线高度,约在0.5~1cm,展开至上端,待溶剂前沿上展至 1Ocm时,取出挥干 4、在点样时最好用吹风机边点边吹干,在原线上点,直至点完一定量。且点样点直径不超 过2mm. 思考题 样品处理时,酸化的目的是什么? 2.气相色谱法定性的依据是什么?用已知物对照法定性时应注意什么? 3.气相色谱法测定中用外标法定量有何优缺点? 4.你对薄层色谱法测定食品中苯甲酸、山梨酸的实验有什么体会? 5.比较两种方法各有什么优缺点?
80℃干燥 1h,取出,置于干燥器中保存。 (2)点样:在薄层板下端 2cm 的基线上,用微量注射器点 10µL,20µL 试样液,同时各点 10µL、 20µL 山梨酸、苯甲酸标准溶液。 (3)展开与显色: 将点样后的薄层板放入预先盛有展开剂(10.①或 10.②)的展开槽内,周 围贴有滤纸,待溶剂前沿上展至 10cm,取出挥干,喷显色剂,斑点成黄色,背景为蓝色。 试样中所含山梨酸、苯甲酸的量与标准斑点比较定量(山梨酸、苯甲酸的比移值依次为 0.82、 0.73)。 五、结果计算 试样中苯甲酸或山梨酸的含量按下式进行计算。 X= 1000 25 10 m 1000 1 2 × × × × V V A 式中: X——试样中苯甲酸或山梨酸的含量,单位为克每千克(g/kg); A——测定用试样液中苯甲酸或山梨酸的质量,单位为毫克(mg); V1——加入乙醇的体积,单位为毫升(mL); V2——测定时点样的体积,单位为毫升(mL); m——试样质量,单位为克(g); 10——测定时吸取乙醚提取液的体积,单位为毫升(mL); 25——试样乙醚提取液总体积,单位为毫升(mL); 六、注意事项 1、 层析用的溶剂系统不可存放太久,否则浓度和极性都会变化,影响分离效果,应新鲜配 制。 2、 在展开之前,展开剂在缸中应预先平衡 1h,使缸内蒸气压饱和,以免出现边缘效应。 3、 展开剂液层高度不能超过原线高度,约在 0.5~1cm,展开至上端,待溶剂前沿上展至 10cm 时,取出挥干。 4、 在点样时最好用吹风机边点边吹干,在原线上点,直至点完一定量。且点样点直径不超 过 2mm。 思考题: 1. 样品处理时,酸化的目的是什么? 2. 气相色谱法定性的依据是什么?用已知物对照法定性时应注意什么? 3. 气相色谱法测定中用外标法定量有何优缺点? 4. 你对薄层色谱法测定食品中苯甲酸、山梨酸的实验有什么体会? 5. 比较两种方法各有什么优缺点?

实验二糖精含量的检测(薄层色谱法) 一、目的与要求 1,学习薄层色谱法测定食品中糖精含量的基本原理 2.掌握薄层色谱法的基本操作技术。 二、原理 在酸性条件下,食品中的糖精钠用乙醚提取,浓缩、薄层色谱分离、显色后,与标准比 较,进行定性和半定量测定。 三、仪器与试剂 1.试剂 (1)盐酸溶液(1:1)为 (2)乙醚(不含过氧化物): (3)无水硫酸钠:经550℃灼烧4h处理: (4)无水乙醇: (5)展开剂:苯:乙酸乙酯:醋酸=12:7:1: (6)糖精钠标准溶液:称取糖精钠0.1000g,用无水乙醇溶解并定容至100mL。此液含 标准精精钠为1mgmL。 (7)硅酸GF254: (8)羧甲基纤维素纳溶液(0.5%) 2.仪器 (1)玻璃板10×10cm (2)薄层层析装置:(见图4-1) (3)微量吸管及吹风筒: (4)紫外检测仪:波长254nm。 四、测定步骤 1.样品的提取 图41薄层层析装置 (1)饮料、冰棍、汽水: 1一层析缸:2一展开剂气:3一层板: 取10.0mL均匀试样(如试样中含有二氧化碳,先 4一盛液(悠展开剂:一隔 加热除去。如试样中含有酒精,加4%氢氧化钠溶液使其量碱性,在沸水浴中加热除去), 置于100mL分液漏斗中,加2mL盐酸(1+1),用30、20、20mL乙醚提取三次,合并乙 提取液,用5mL盐酸酸化的水洗涤一次,弃去水层。乙醚层通过无水硫酸钠脱水后,挥发 乙醚,加2.0mL乙醇溶解残留物,密塞保存,备用, (2)酱油、果汁、果酱等: 称取20.0g或吸取20.0mL均均试样,置于100mL容量瓶中,加水至约60mL,加20mL
实验二 糖精含量的检测(薄层色谱法) 一、目的与要求 1. 学习薄层色谱法测定食品中糖精含量的基本原理。 2. 掌握薄层色谱法的基本操作技术。 二、原理 在酸性条件下,食品中的糖精钠用乙醚提取,浓缩、薄层色谱分离、显色后,与标准比 较,进行定性和半定量测定。 三、仪器与试剂 1. 试剂 (1)盐酸溶液(1:1); (2)乙醚(不含过氧化物); (3)无水硫酸钠:经 550℃灼烧 4h 处理; (4)无水乙醇; (5)展开剂:苯:乙酸乙酯:醋酸=12:7:1; (6)糖精钠标准溶液:称取糖精钠 0.1000g,用无水乙醇溶解并定容至 100mL。此液含 标准精精钠为 1mg/mL。 (7)硅酸 GF254; (8)羧甲基纤维素钠溶液(0.5%)。 2. 仪器 (1)玻璃板 10×10cm; (2)薄层层析装置;(见图 4-1) (3)微量吸管及吹风筒; (4)紫外检测仪:波长 254nm。 四、测定步骤 1. 样品的提取 (1)饮料、冰棍、汽水: 取 10.0mL 均匀试样(如试样中含有二氧化碳,先 加热除去。如试样中含有酒精,加 4%氢氧化钠溶液使其量碱性,在沸水浴中加热除去), 置于 100mL 分液漏斗中,加 2mL 盐酸(1+1),用 30、20、20mL 乙醚提取三次,合并乙醚 提取液,用 5mL 盐酸酸化的水洗涤一次,弃去水层。乙醚层通过无水硫酸钠脱水后,挥发 乙醚,加 2.0mL 乙醇溶解残留物,密塞保存,备用。 (2)酱油、果汁、果酱等: 称取 20.0g 或吸取 20.0mL 均均试样,置于 100mL 容量瓶中,加水至约 60mL,加 20mL 图 4-1 薄层层析装置 1—层析缸;2—展开剂蒸气;3—薄层板; 4—盛液皿(盛展开剂);5—隔板