
2.电极极化原因 冰影军 NCNVRSETY OF TECHNOLOGY 2.2电化学极化 电极反应总是分若干步进行,其中可能某一步 反应速率较慢,需要较高的活化能。 为了使电极反应顺利进行所额外施加的电压称 为电化学超电势(亦称为活化超电势) 这种极化现象称为电化学极化
2.2 电化学极化 电极反应总是分若干步进行,其中可能某一步 反应速率较慢,需要较高的活化能。 为了使电极反应顺利进行所额外施加的电压称 为电化学超电势(亦称为活化超电势) 这种极化现象称为电化学极化。 2. 电极极化原因
2.电极极化原因 林影军 2.2电化学极化 当有电流通过电极时,若电极-溶液界面处电极反应 进行得不够快,导致电极带电程度的改变,使电极电势 偏离阿逆° 阴极反应:H++e→1/2H, 阳极反应:1/2H2-e→H+ e H H 十+ Pt Pt P不可逆,阴< P可逆,阴 不可逆,阳>可逆,阳
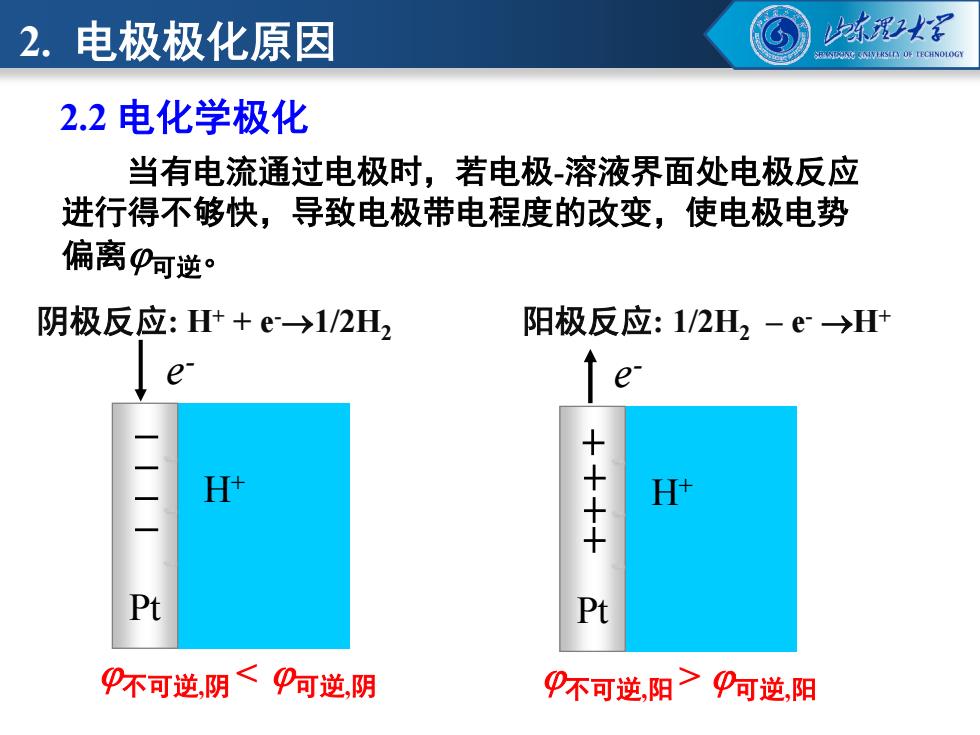
阴极反应: H+ + e-→1/2H2 阳极反应: 1/2H2 – e - →H+ 2. 电极极化原因 当有电流通过电极时,若电极-溶液界面处电极反应 进行得不够快,导致电极带电程度的改变,使电极电势 偏离可逆。 2.2 电化学极化 不可逆,阴 < 可逆,阴 不可逆,阳 > 可逆,阳 Pt - - - e - H+ Pt - - - e - H+

2.电极极化原因 冰影军 NCAVIRSETY OF IECHNOLOGY 极化后的结果: ①不可逆,阴<可逆,阴;P不可逆,阳之可逆,阳 结论:当电流通过电极时,由于电化学反应的 迟缓性造成电极带电程度与可逆情况时不同, 从而导致电极电势偏离p阿逆的现象,称作“电 化学极化
极化后的结果: 不可逆,阴 < 可逆,阴; 不可逆,阳 > 可逆,阳 结论:当电流通过电极时,由于电化学反应的 迟缓性造成电极带电程度与可逆情况时不同, 从而导致电极电势偏离可逆的现象,称作“电 化学极化”。 2. 电极极化原因

2.电极极化原因 林影深 NGAVRSETY OF TECHNOIOG 2.3超电势 。在某一电流密度下,实际发生电解的电极 电势P不可逆与可逆电极电势P可逆之间的 差值称为超电势。 ®阳极上由于超电势使电极电势变大,阴极 上由于超电势使电极电势变小。 。为了使超电势都是正值,把阴极超电势7阴 和阳极超电势门阳 分别定义为: 7阴=(9可逆一P不可逆)阴 门阳=(9不可逆一可逆)阳
为了使超电势都是正值,把阴极超电势 阴 和阳极超电势 阳 分别定义为: 阳极上由于超电势使电极电势变大,阴极 上由于超电势使电极电势变小。 阴 = − ( ) 可逆 不可逆 阴 阳 = − ( ) 不可逆 可逆 阳 在某一电流密度下,实际发生电解的电极 电势 与可逆电极电势 之间的 差值称为超电势。 不可逆 可逆 2.3 超电势 2. 电极极化原因

2.电极极化原因 冰影学 NCNVIRSETY OF TECHNOLOGY 2.3超电势 整个电池的分解电压等于阴、阳两极的析出 电势之差: E分解一P阳,不可逆P阴,不可逆 =(9阳,可逆+1阳(9阴,可逆1阴) =E可逆+1阳十1阴
整个电池的分解电压等于阴、阳两极的析出 电势之差: E分解= 阳,不可逆- 阴,不可逆 = ( 阳, 可逆+ η阳)- ( 阴, 可逆-η阴) = E可逆+η阳+ η阴 2. 电极极化原因 2.3 超电势