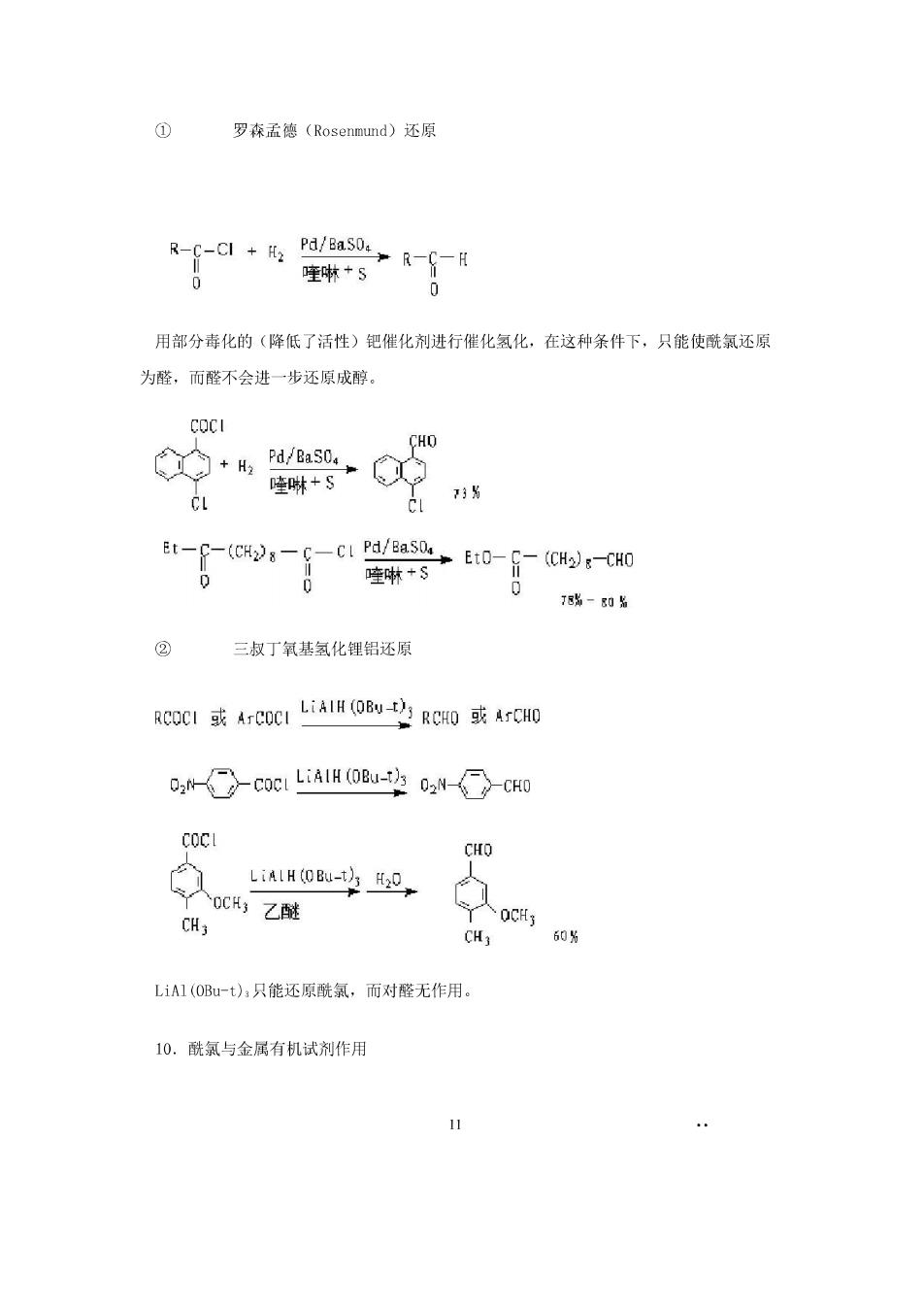
① 罗森孟德(Rosenmund)还原 R-S-C1+5Pa/a50:) 座嫩5R一日 0 用部分毒化的(降低了活性)钯催化剂进行催化氢化。在这种条件下,只能使酰氯还原 为醛,而醛不会进一步还原成醇。 COCI ○+H,a/Bas0:, CHO CL Et--(CH-c-c1 Pa/BaSD. 壁SEt0-fCg-00 78瑞-80名 三叔丁氧基氢化锂铝还原 Rc0Cl或I1H(OBW-RG0或ArO0 COC LiAIH (OBU-2 N-CHO COCL CHO LiAIH (OBU-t)2 人oCH乙酰 CH3 60% LiA1(OB-t),只能还原酰氯,而对整无作用。 10.酰氯与金属有机试剂作用 1

①与二烃基铜锂试剂作用 RXi→RL:CuK,R,CuLi Ar LiArLi Cu ArCuLi y0uLi+R--CI→R-C-Rr R与R”可以是烷基或芳基 二烃基铜锂与酰氯反应成酮。不与-N0,-CX,C-0,-C00R反应。 COCH: N02 0my0-f0,0m,f-C1+【C),cc,0m,l0uLi→ CROC-CHCK-CH>CH,CH(CK 0 ②与二烃基镉试剂作用 2R'WgK+Cdc2→R2Cd 背-0+a一R-育 二烃基镉试剂只与酰氯反应,不与酮反应 §12.3醛、酮的物理性质和光谱性质 12

12.3.1物理性质 -y3. G 00® 68 除甲醛是气体外,十二个碳原子以下的醛、酮都是液体,高级的醛、酮是固体。低级 醛常带有刺鼻的气味,中级醛则有花果香,所以CC的醛常用于香料工业。低级酮有清 爽味,中级酮也有香味。 羰基中,碳和氧以双键相结合,碳原子用三个$p杂化轨道形成三个。健,其中一个是和 氧形成一个。键,这三个键在同一个平面上。碳原子剩下来的一个p轨道和氧的一个卫轨 道与这三个。健所形成的平面垂直,彼此重叠形成一个云键 8 由于氧的电负性吸引电子的能力很强,所以羰基是一个极性基团,具有一个偶极矩, 负极向氧一面,正极朝向碳的一面 由于羧基的偶极矩,增加了分子间吸引,所以它们的沸点与分子量相近的烷烃和醚相比 较,增高50℃以上。但因为醛酮分子间不能形成氢键,故其沸点则低于相应的醇。 基氧能和水分子形成氢键,故低级醛、酮溶于水。 12.3.2光谱性质 IR:醛C-0伸缩在1725cm附近,有强吸收峰。(共轭作用使吸收波数减少) 13
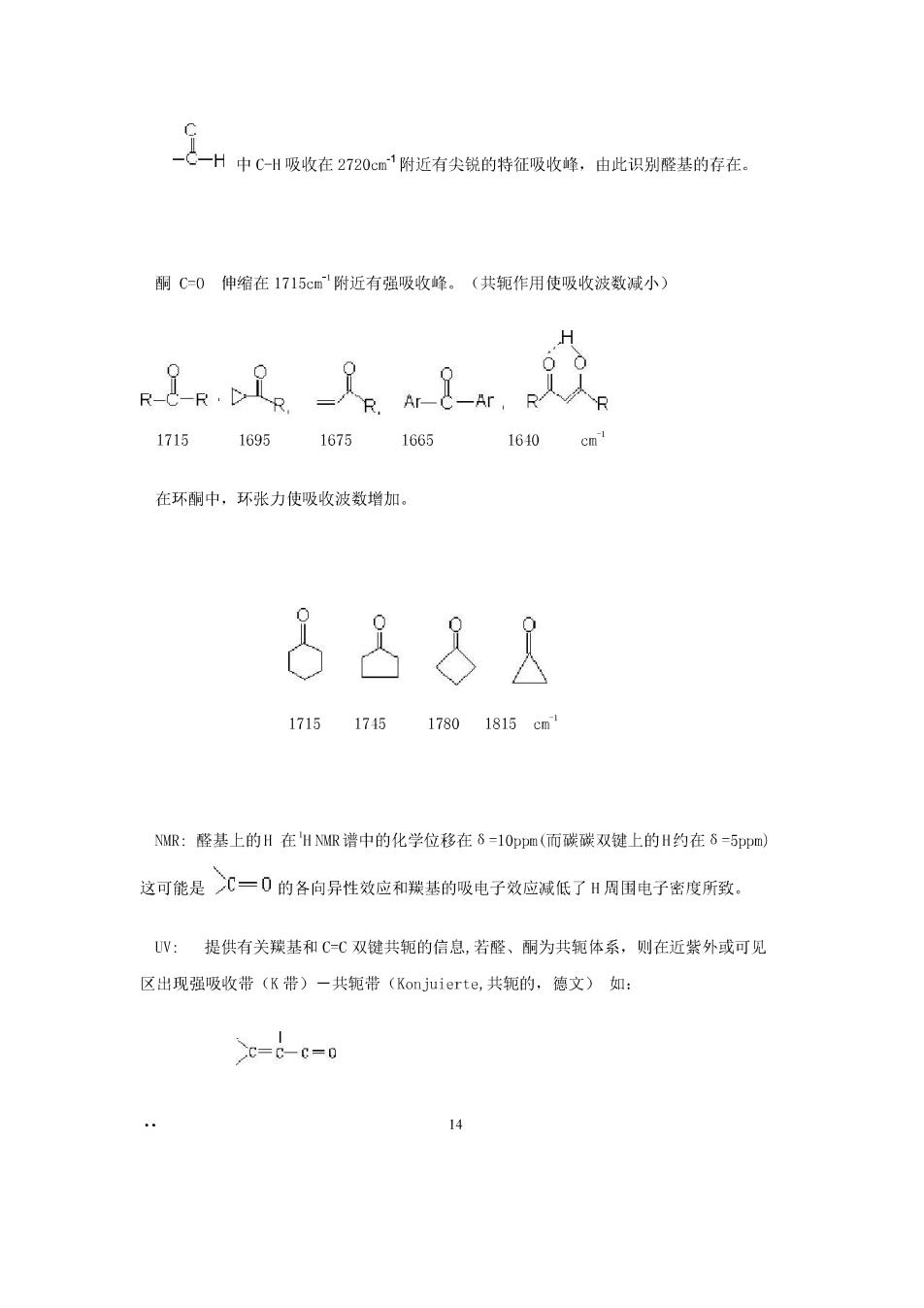
1吸收在2720'附近有尖锐的特征吸收峰,由此识别基的 丽C-0伸缩在1715c附近有强吸收峰。(共轭作用使吸收波数减小) 1715 169516751665 160 cm 在环酮中,环张力使吸收波数增加。 888公 1715174517801815cm NMR:醛基上的H在HMR谱中的化学位移在6=1Oppm(而碳碳双键上的H约在5-5ppm) 这可能是>C=0的各向异性效应和装基的吸电子效应减低了H周围电子密度所致, UV:提供有关羰基和CC双键共轭的信总,若醛、酮为共轭体系,则在近紫外或可见 区出现强吸收带(K带)一共轭带(Konj加ierte,共钯的,德文)如: >c=0-c-0 14

K带:入mx215-250mm(eax10000-20000)元一* R带:(基团型的,Radiralartig德文)入max300-350nm(emax10-10)-1· §12.4醛、酮的化学性质 醛酮中的基由于π键的极化,使得氧原子上带部分负电荷,碳原子上带部分正电荷。 氧原子可以形成比较稳定的氧负离子,它较带正电荷的碳原子要稳定得多,因此反应中心 是羰基中带正电荷的碳。所以羰基易与亲核试剂进行加成反应(亲核加成反应)。 此外,受羧基的影响,与羧基直接相连的α-碳原子上的氢原子(α-H)较活泼,能 发生一系列反应, 亲核加成反应和α-H的反应是醛、酮的两类主要化学性质。 醛、酮的反应与结构关系一般描述如下: ·碱和亲核试剂进攻缺电子的碳 一涉及醛的反应(氧化反应) α~H的反应厂羟醛缩合反应 !卤代反应 12.4.1亲核加成反应 醛,酮分子中的碳氧双键与烯烃分子中的碳碳双键均是由一个。键和一个π键组成 因此,醛、酮能够发生一系列加成反应。娇烃的加成一般由亲电试剂进攻而发生,是 亲电加成:而醛、酮的加成是在亲核试剂的进改下发生的,是亲核加成。 1.与氢氰酸的加成反应 CN a羟基睛 15