
第十九章氨基酸蛋白质核酸 一学习目的和要求 1.掌握氨基酸的分类、常见氨基酸的结构和名称。 2.掌握氨基酸的合成方法及化学性质。 3,掌握蛋白质的性质。 4.理解多肽的一般结构。 5.了解蛋白质的一级结构、二级结构、三级结构和四级结构。 6.了解蛋白质的性质。 7.了解氨基酸、蛋白质在生命活动中的重要意义, 二.本章节重点、难点: 氨基酸、蛋白质的化学性质二十种常见氨基酸的名称和分类:蛋白质的四级结构 引言: 蛋白质和核酸都是天然高分子化合物,是生命物质的基础。我们知道,生命活动的基 本特征就是蛋白质的不断自我更新。蛋白质是一切活细胞的组织物质,也是酶、抗体和许 多激素中的主要物质。所有蛋白质都是α-由氨基酸构成的,因此,α-由氨基酸是建筑蛋白 质的砖石。要讨论蛋白质的结构和性质,首先要研究α-由氨基酸的化学 19.1氨基酸 19.11结构、分类、命名和构型 组成蛋白质的氨基酸(天然产氨基酸)都是α-氨基酸,即在α-碳原子上有一个氨基, 可用下式表示: R-C-COOH NH2 天然产的各种不同的ā-由氨基酸只R不同而已.氨基酸目前已知的已超过100种以上, 但在生物体内作为合成蛋白质的原料只有二十种(见P46表19-1)。 1.分类: 按烃基类型可分为脂肪族氨基酸,芳香族氨基酸,含杂环氨基酸

按分子中氨基和羧基的数目分为中性氨基酸,酸性氨基酸,碱性氨基酸。 2.命名:多按其来源或性质而命名。国际上有通用的符号(见P66表20-1)。 3.构型:用DL体系表示一在费歇尔投影式中氨基位于横键右边的为D型,位于 左边的为L型。例如 COOH COOH H-C-NH2 NH2一C-H R R D-氨基酸 L-氨基酸 天然氨基酸(出甘氨酸外)其他所有α,碳原子都是手性的,都有旋光性,而且发现主 要是L型的(也有D型的,但很少)。 19.12氨基酸的性质 1,氨基酸的酸-碱性一一两性与等电点 氨基酸分子中的氨基是碱性的,而线基是酸性的,因而氨基酸既能与酸反应,也能与 碱反应,是一个两性化合物。 R-CH-COOHH R-CH-COOH OH -R-CH-COO NHa NH2 NH2 (1)两性 氨基酸在一般情况下不是以游离的羧基或氨基存在的,而是两性电离,在固态或水溶 液中形成内盐。 R-CH-COOH±R-CH-COO NH> +NH3 (2)等电点 在氨基酸水溶液中加入酸或碱,至使羧基和氨基的离子化程度相等(即氨基酸分子所 带电荷呈中性一一处于等电状态)时溶液的pH值称为氨基酸的等电点。常以p表示

R-CH-COOH NH2 H© R-CH-COO三 =R-CH-COO NH2 NH OHO 溶液pH>等电点 等电点(p 溶液pH等电点 强调: a,等电点为电中性而不是中性(即pH=7),在溶液中加入电极时其电荷迁移为零, 中性氨基酸 pl=4.8-63 酸性氨基酸 pl=2.7-3.2 碱性氨基酸 pl=7.610.8 b.等电点时,偶极离子在水中的溶解度最小,易结品析出。 2.氨基酸氨基的反应 (1)氨基的酰基化氨基酸分子中的氨基能酰基化成酰胺。 乙酰氯、醋酸酐、苯甲酰氯邻苯二甲酸酐等都可用作酰化剂。在蛋白质的合成过程中 为了保护氨基则用苄氧甲酰氯作为酰化剂。 at-o8a+mtoo一Oo6o-8m&tco 选用苄氧甲酰氯这一特殊试剂,是因为这样的酰基易引入,对以后应用的种种试剂较 稳定,同时还能用多种方法把它脱下来。 (2)氨基的烃基化氨基酸与RX作用则烃基化成N烃基氨基酸: NO, R NO2 R NO-F+NH2 CH-COOH-NO-NH-CH-COOH 氟代二硝基苯在多肽结构分析中用作测定N端的试剂。 (3)与亚硝酸反应 R-CH-COOH+HNO2 R-CH-COOH N2t+H2o NH2 OH
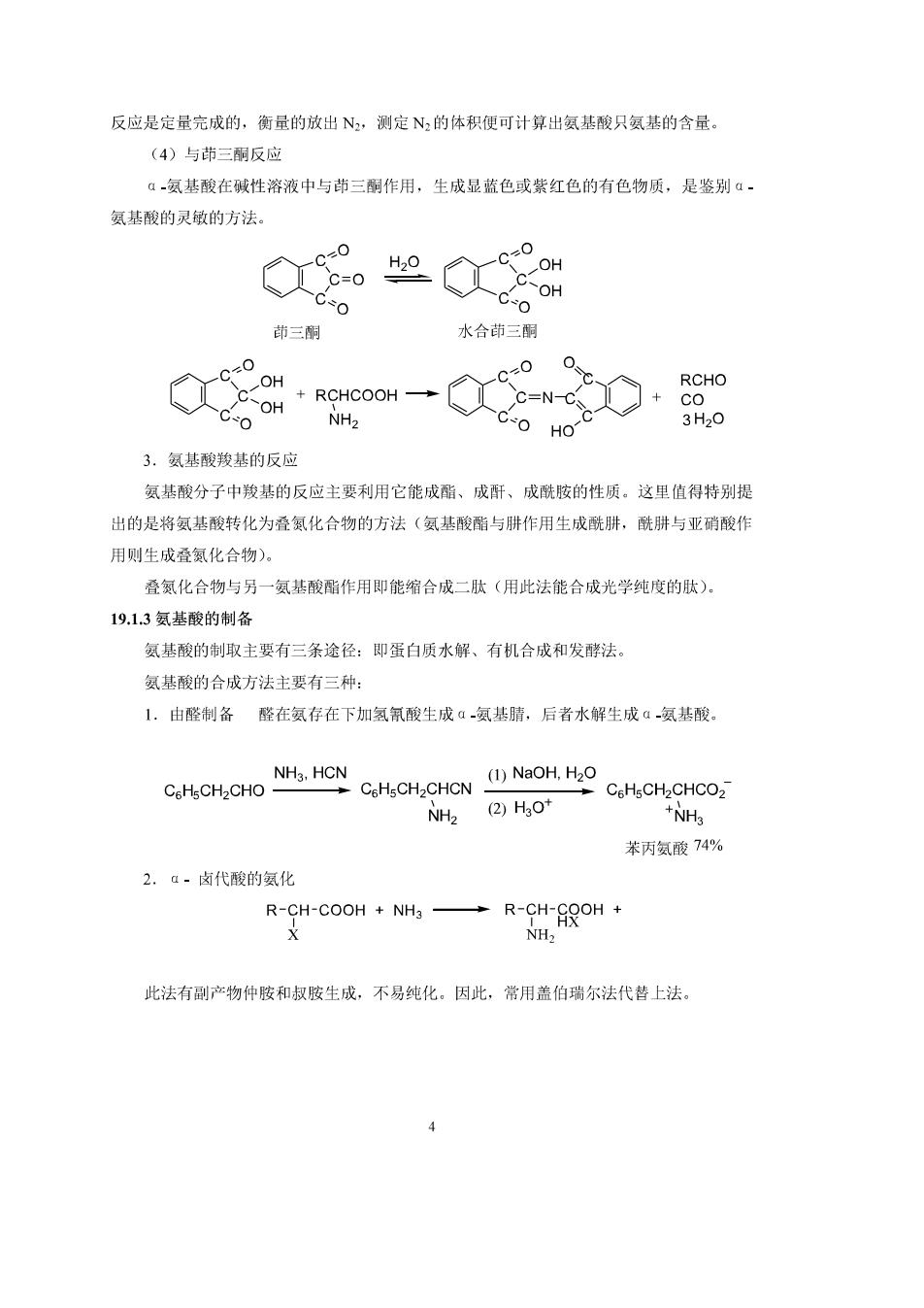
反应是定量完成的,衡量的放出N,测定N的体积便可计算出氨基酸只氨基的含量。 (4)与茚三酮反应 á一氨基酸在碱性溶液中与茚三酮作用,生成显蓝色或紫红色的有色物质,是鉴别α 氨基酸的灵敏的方法 c=0 OH OH 茚三削 水合茚三酮 00 OH RCHO COHROHCOOH-二c0h0% NH2 3H20 3.氨基酸羧基的反应 氨基酸分子中羧基的反应主要利用它能成酯、成酐、成酰胺的性质。这里值得特别提 出的是将氨基酸转化为叠氮化合物的方法(氨基酸酯与肼作用生成酰肼,酰肼与亚硝酸作 用则生成叠氮化合物). 叠氮化合物与另一氨基酸酯作用即能缩合成二肽(用此法能合成光学纯度的肽) 19.13氨基酸的制备 氨基酸的制取主要有三条途径:即蛋白质水解、有机合成和发酵法。 氨基酸的合成方法主要有三种: L.由醛制各醛在氨存在下加氢氯酸生成a氨基睛,后者水解生成氨基酸。 CCHCHO N.HCN CoHsCHaCHCN (1)NaoH,H2o CeHsCH2CHCO2 NH2 (②H0+ +NH3 苯丙氨酸74% 2.a-卤代酸的氨化 R-9rco1+一R-股o1+ 此法有副产物仲胺和叔胺生成,不易纯化。因此,常用盖伯瑞尔法代替上法。 4
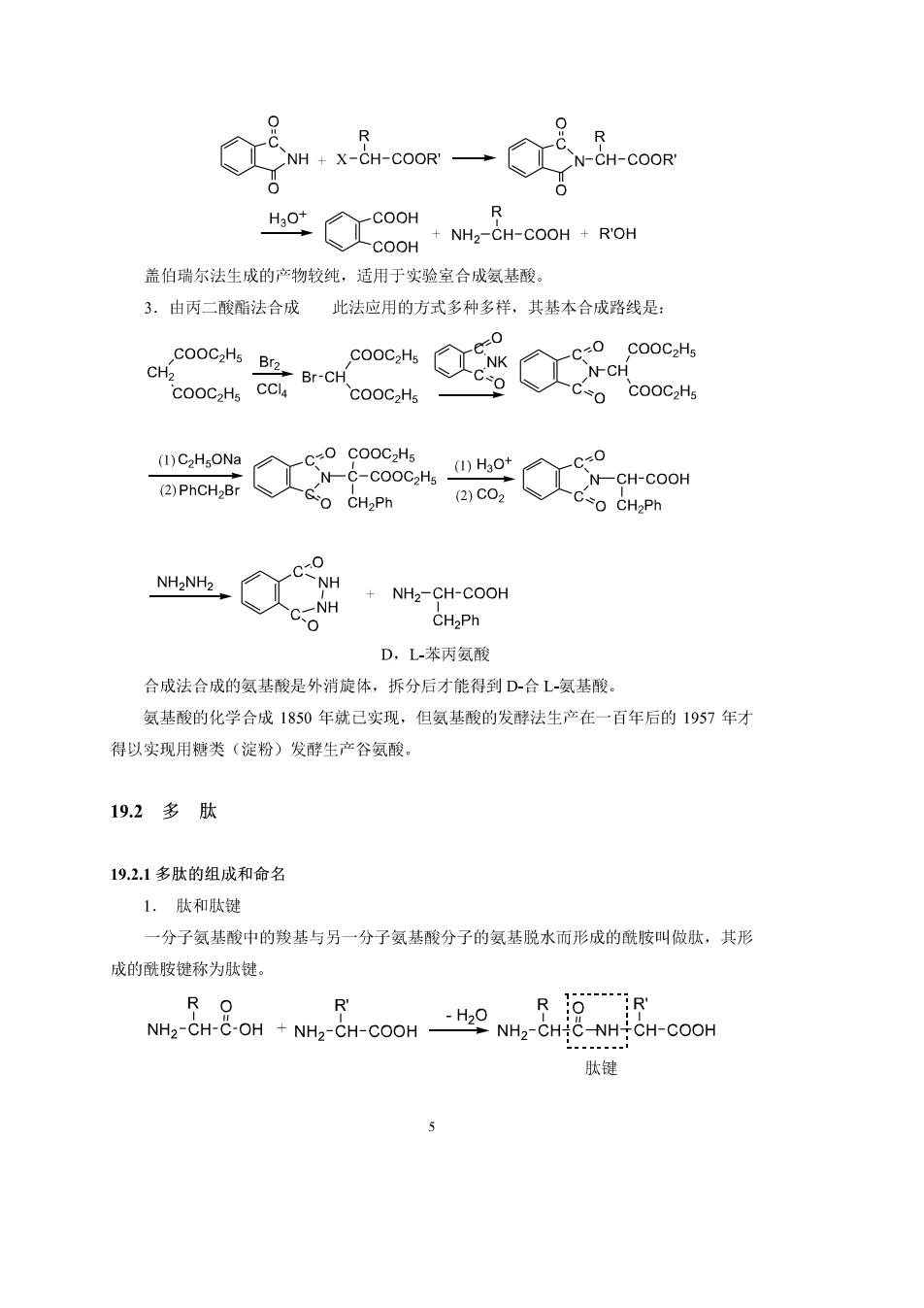
R NH+x-H-cooR一 Q R CN-CH-COOR COOOM 盖伯瑞尔法生成的产物较纯,适用于实验室合成氨基酸。 3.由丙二酸酯法合成 此法应用的方式多种多样,其基本合成路线是 COOCzHs Br2 0 COOC2H Br-CH cooc N-CH COOC2Hs CO COOC2Hs N-COOCH (1)Ho 0 (2)PhCH,Br NCH-COOH GO CH2Ph (2)C02 CO CH2Ph NH2NH2 c-o NH2-CH-COOH CH2Ph D,L苯丙氨酸 合成法合成的氨基酸是外消旋体,拆分后才能得到D-合L氨基酸。 氨基酸的化学合成1850年就己实现,但氨基酸的发酵法生产在一百年后的1957年才 得以实现用糖类(淀粉)发酵生产谷氨酸 19.2多肽 19.2.1多肽的组成和命名 1.肽和肽键 一分子氨基酸中的羧基与另一分子氨基酸分子的氨基脱水而形成的酰胺叫做肽,共形 成的酰胺键称为肽键。 NH2CH-COH-NH2-CH-COOH NH-CHIC-NHTCH-COOH 肽键