
7构型异构 一 种配合物可以采取两种或两种以上的空间构型 时,则会产生构型异构现象。如NiCL(Ph2PCH2Ph)2l 有四面体和平面四边形两种构型。 常见的构型异构有五配位的三角双锥和四方锥; 八配位的十二面体和四方反棱柱体。等等
7 构型异构 一种配合物可以采取两种或两种以上的空间构型 时, 则会产生构型异构现象。如[NiCl2 (Ph2PCH2Ph)2 ] 有四面体和平面四边形两种构型。 常见的构型异构有五配位的三角双锥和四方锥; 八配位的十二面体和四方反棱柱体。等等

7.3过渡元素的配位化学 过渡元素具有强烈的形成配合物的趋向。这是因为: 1过渡元素有能量相近的属同一个能级组的(n一1)d、 ns、 p共九条价电子轨道。按照价键理论,这些能量相近 的轨道可以通过不同形式的杂化,形成成键能力较强的杂 化轨道,以接受配体提供的电子对,形成多种形式的配合物。 2过渡金属离子是形成配合物的很好的中心形成体。 这是因为: ①过渡金属离子的有效核电荷大; ②电子构型为9~17型,其极化力和变形性都较强,因 而过渡金属离子可以和配体产生很强的结合力。 当过渡金属离子的轨道未充满抛,易生成内轨的配 合物;如果电子较多,还易与配位体生成附加的反馈π键, 从而增加配合物的稳定性。 因而有人说,过渡元素化学就是山电子的配位化学
2 过渡金属离子是形成配合物的很好的中心形成体。 这是因为: ① 过渡金属离子的有效核电荷大; ② 电子构型为9~17型, 其极化力和变形性都较强, 因 而过渡金属离子可以和配体产生很强的结合力。 当过渡金属离子的d轨道未充满时, 易生成内轨型的配 合物;如果d电子较多, 还易与配位体生成附加的反馈 π 键, 从而增加配合物的稳定性。 7.3 过渡元素的配位化学 过渡元素具有强烈的形成配合物的趋向。这是因为: 1 过渡元素有能量相近的属同一个能级组的(n-1)d、 ns、np共九条价电子轨道。按照价键理论, 这些能量相近 的轨道可以通过不同形式的杂化, 形成成键能力较强的杂 化轨道, 以接受配体提供的电子对, 形成多种形式的配合物。 因而有人说,过渡元素化学就是d电子的配位化学

7.3.1价键理论(VB理论) 配合物的价键理论的基本思想是: 配合物是通过给予体和接受体的反应而生成的, 给予体原子具有孤对电子,它给出孤对电子进入作为 配合物中心原子或离子的空轨道,为了接受这些电子 对,中心原子的原子轨道首先要进行杂化形成一组新 的具有一定方向性和对称性的等价杂化轨道,再与配 体的给予体轨道重叠形成σ配健。如果中心原子还有 合适的孤对电子,而配体又有合适的空轨道,这时中 心原子上的孤对电子将进入配体空轨道从而形成反馈 的元配键。 显然,配合物的配位数就是中心原子在成键时动用 的空轨道数
显然,配合物的配位数就是中心原子在成键时动用 的空轨道数。 7.3.1 价键理论(VB理论) 配合物的价键理论的基本思想是: 配合物是通过给予体和接受体的反应而生成的, 给予体原子具有孤对电子,它给出孤对电子进入作为 配合物中心原子或离子的空轨道,为了接受这些电子 对,中心原子的原子轨道首先要进行杂化形成一组新 的具有一定方向性和对称性的等价杂化轨道,再与配 体的给予体轨道重叠形成配键。如果中心原子还有 合适的孤对电子,而配体又有合适的空轨道,这时中 心原子上的孤对电子将进入配体空轨道从而形成反馈 的 配键

价键理论顺利地解释了配合物的分子构型。 显然,分子构型决定于杂化轨道的类型: 配位数 2 3 4 4 杂化轨道 sp sp2 Sp3 dsp2 分子构型 直线 三角形 正四面体 正方形 配位数 5 5 6 杂化轨道sp3dd2sp2, d4s sp3d2,d2sp3 分子构型 三角双锥 四方锥 正八面体 根据配合物的磁矩可以计算配合物中成单的电子数并由此 确定杂化轨道的类型: u=n(n+2) 其中为配合物中的成单电子数,u为配合物的磁矩
= 其中n为配合物中的成单电子数,为配合物的磁矩。 n(n + 2) 价键理论顺利地解释了配合物的分子构型。 显然, 分子构型决定于杂化轨道的类型: 根据配合物的磁矩可以计算配合物中成单的电子数并由此 确定杂化轨道的类型: 配 位 数 2 3 4 4 杂化轨道 sp sp2 sp3 dsp2 分子构型 直线 三角形 正四面体 正方形 配 位 数 5 5 6 杂化轨道 sp3d d2 sp2 , d4 s sp3d 2 , d2 sp3 分子构型 三角双锥 四方锥 正八面体
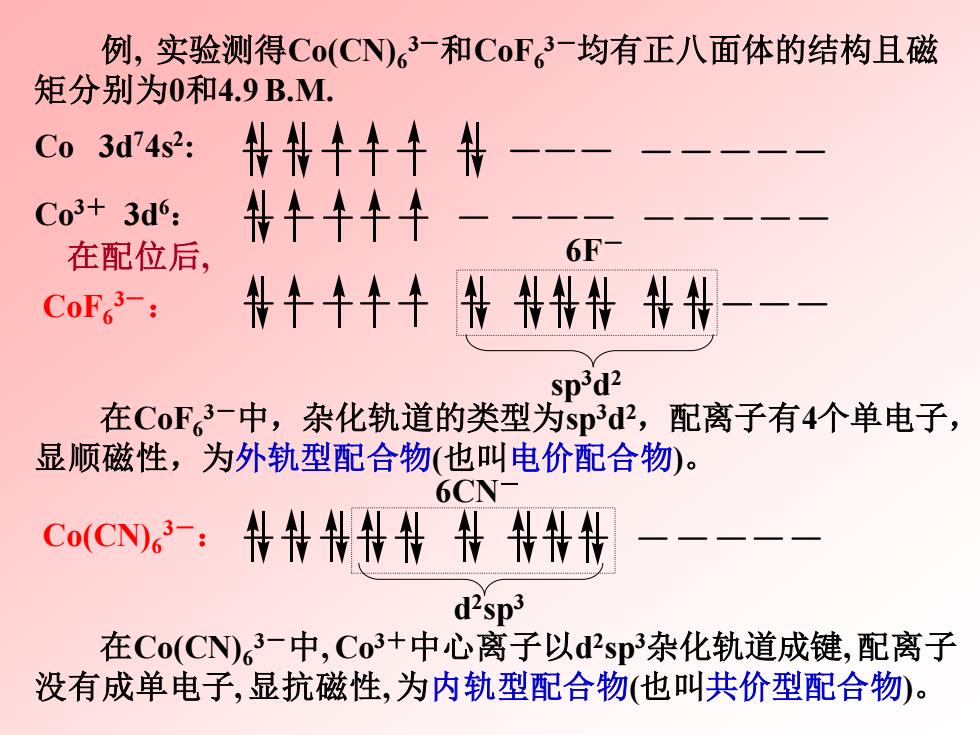
例,实验测得Co(CN)。3-和CoF。3-均有正八面体的结构且磁 矩分别为0和4.9B.M. C03d4s2: 料料牛牛牛 Co3+3d6: 牛++ 在配位后, 6F- 料十牛千牛书拌料料柑 sp3d2 在CoF。3-中,杂化轨道的类型为sp3d2,配离子有4个单电子, 显顺磁性,为外轨型配合物(也叫电价配合物)。 6CN Co(CN-:朴钱钱什朴朴杆 d2sp3 在Co(CN)63-中,Co3+中心离子以d2sp3杂化轨道成键,配离子 没有成单电子,显抗磁性,为内轨型配合物(也叫共价型配合物)
例, 实验测得Co(CN)6 3-和CoF6 3-均有正八面体的结构且磁 矩分别为0和4.9B.M. d 2 sp3 6CN- Co(CN)6 3-: 在配位后, sp3d 2 6F- CoF6 3-: 在Co(CN)6 3-中, Co3+中心离子以d 2 sp3杂化轨道成键, 配离子 没有成单电子, 显抗磁性, 为内轨型配合物(也叫共价型配合物)。 在CoF6 3-中,杂化轨道的类型为sp3d 2,配离子有4个单电子, 显顺磁性,为外轨型配合物(也叫电价配合物)。 Co 3d74s2 : Co3+ 3d6: