62热力学第一定律对理想气体准静态过程的应用 6.2热力学第一定律 对理想气体准静态过程的应用 一.等体过程 系统体积保持不变的 状态变化过程。 P2 A=0 AE="iR(T-T) M2 2y=△E 前页后页且录 1
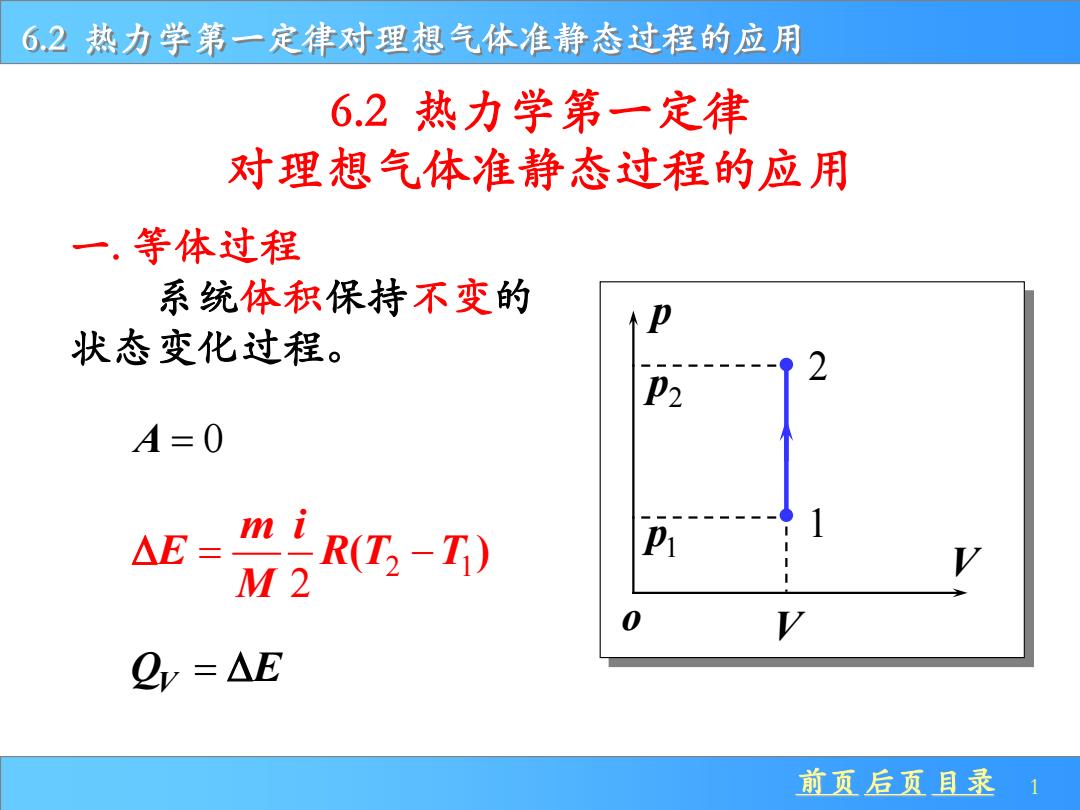
前页 后页 目录 1 6.2 热力学第一定律对理想气体准静态过程的应用 一. 等体过程 系统体积保持不变的 状态变化过程。 p V 1 2 2 p 1 p o V A = 0 2 1 2 ( ) m i E R T T M = − Q E V = 6.2 热力学第一定律 对理想气体准静态过程的应用

62热力学第一定律对理想气体准静态过程的应用 热容(物质温度升高1K所吸收的热量) c=№ dT 比热容(单位质量物质温度升高1K所吸收的热量) c=d№_c mdT m 摩尔热容:(1mol物质温度升高1K所吸收的热量) Cm do =Mc dT M 前页后页目录2
前页 后页 目录 2 6.2 热力学第一定律对理想气体准静态过程的应用 热容(物质温度升高1K所吸收的热量) d d Q C T = 比热容(单位质量物质温度升高1K所吸收的热量) d d Q C c m T m = = 摩尔热容: (1mol物质温度升高1K所吸收的热量) m d d Q C Mc m T M = =
6.2热力学第一定律对理想气体准静态过程的应用 等体摩尔热容 dQy =dE=miRdT M2 Cv,m= dov Cy,m= dT M vm(7-T) 巴sm 内能和内能的增量写为 E= v.mT △E= M M 前页后页目录 3
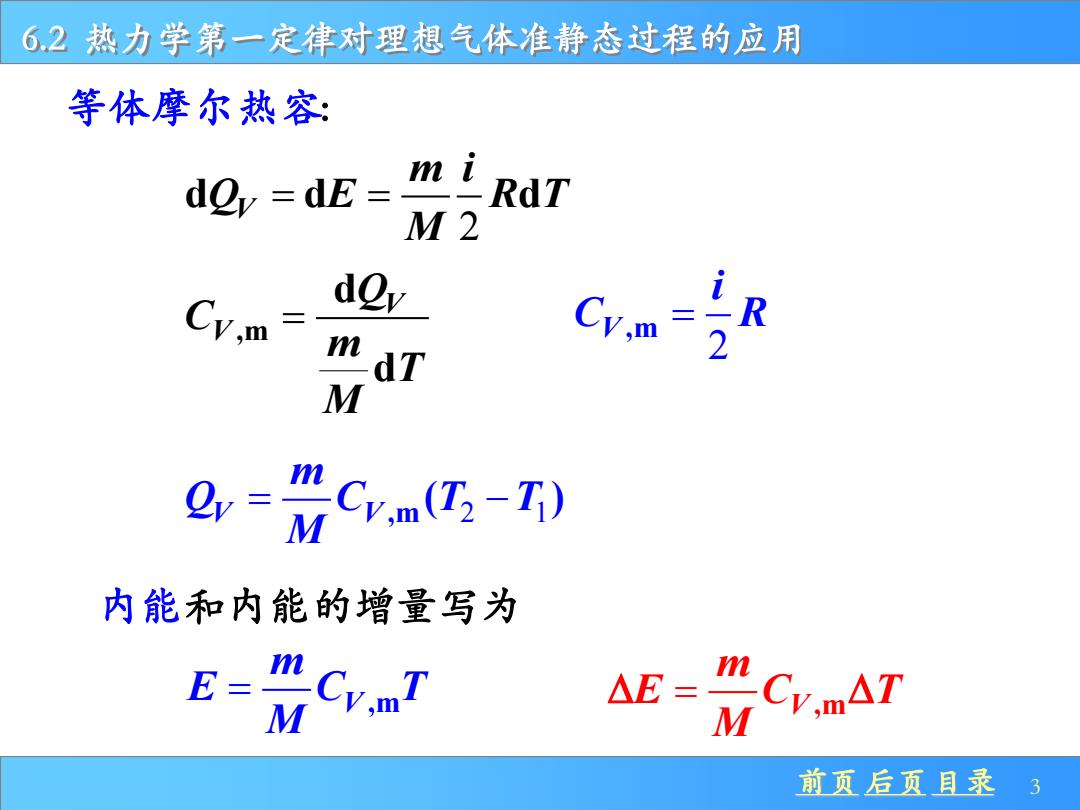
前页 后页 目录 3 6.2 热力学第一定律对理想气体准静态过程的应用 等体摩尔热容: 2 d d d V m i Q E R T M = = ,m d d V V Q C m T M = 内能和内能的增量写为 V ,m m E C T M = 2 V ,m i C R = V ,m m E C T M = ,m 2 1 ( ) V V m Q C T T M = −
62热力学第一定律对理想气体准静态过程的应用 二.等压过程 系统压强保持不变的状态变化过程。 -pdv-) p m 2 R(T-T M D AE=MCy.m(T2-Ti) M Cp=AE+A 前页后页目录4
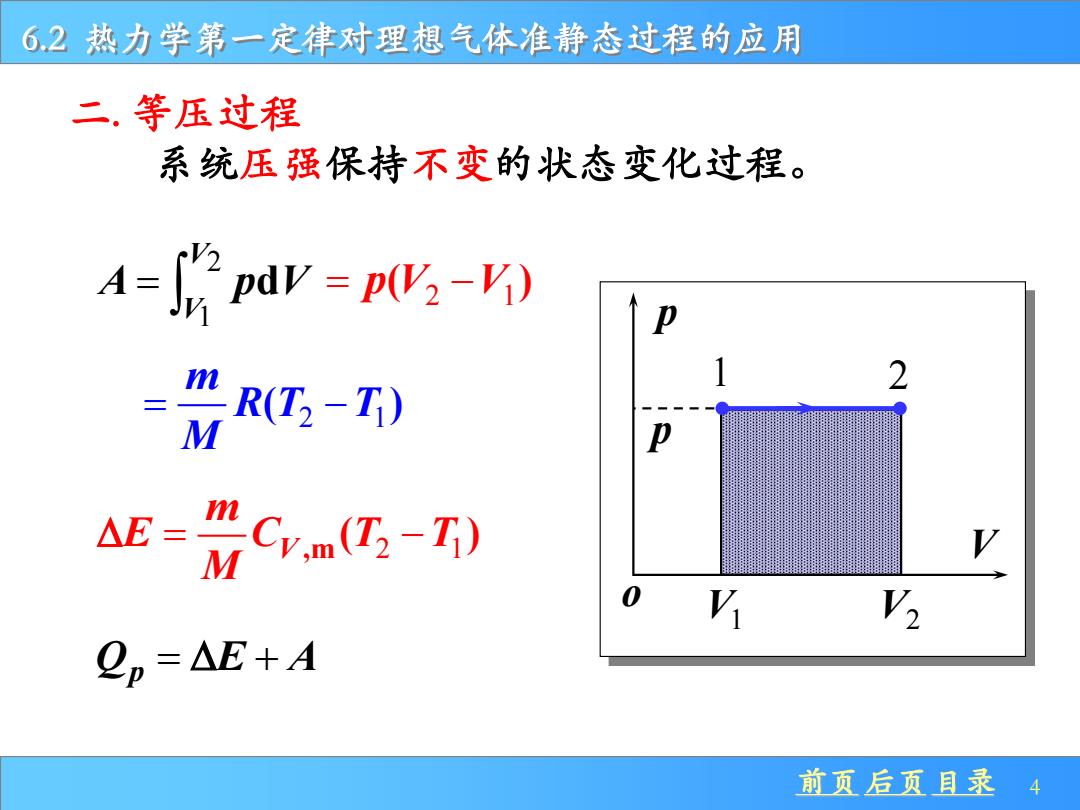
前页 后页 目录 4 6.2 热力学第一定律对理想气体准静态过程的应用 二. 等压过程 系统压强保持不变的状态变化过程。 p V 1 2 V1 V2 p o 2 1 d V V A p V = 2 1 = − p V V ( ) 2 1 ( ) m R T T M = − ,m 2 1 ( ) V m E C T T M = − Q E A p = +

62热力学第一定律对理想气体准静态过程的应用 等压摩尔热容 dop =dE+dA d0,cndr m RdT M Cp:m= dCp T M Cp.m =Cv,m+R 迈耶公式 n Cp.m(-T) 前页后页目录5
前页 后页 目录 5 6.2 热力学第一定律对理想气体准静态过程的应用 等压摩尔热容 d d d Q E A p = + C C R p V ,m ,m = + 迈耶公式 d d d p V ,m m m Q C T R T M M = + ,m d d p p Q C m T M = ,m 2 1 ( ) p p m Q C T T M = −