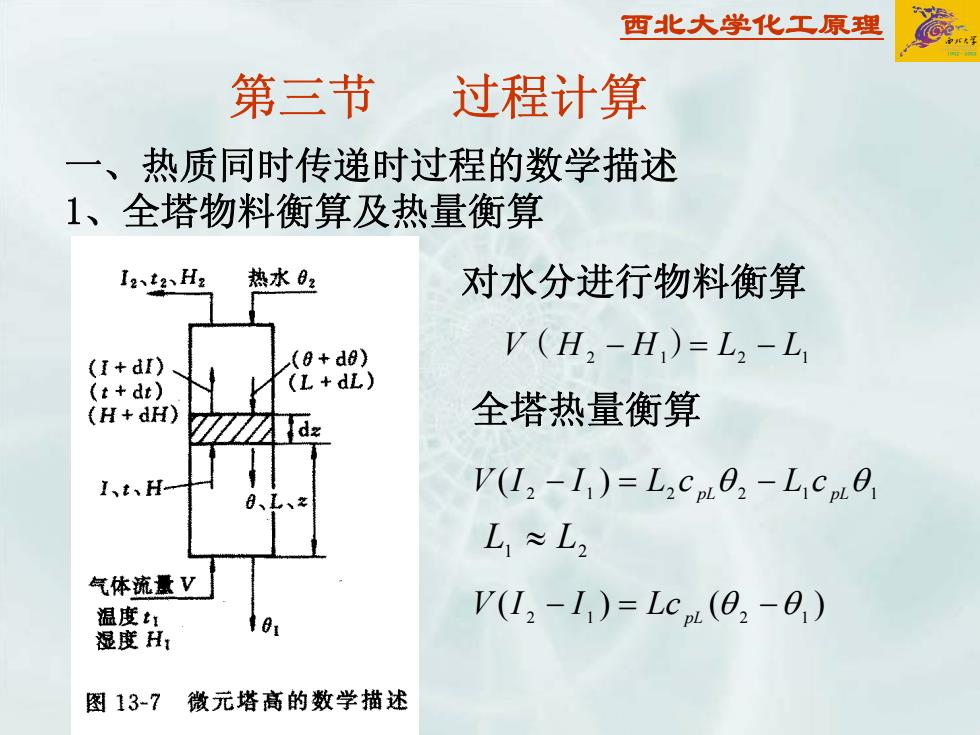
西北大学化工原理 第三节 过程计算 一、热质同时传递时过程的数学描述 1、全塔物料衡算及热量衡算 对水分进行物料衡算 ( 12 ) −=− LLHHV 12 )()( − 12 = LcIIV pL θ −θ 12 全塔热量衡算 ≈ LL 21 12 1122 − )( = pLθ − cLcLIIV pLθ
西北大学化工原理 第三节 过程计算 一、热质同时传递时过程的数学描述 1、全塔物料衡算及热量衡算 对水分进行物料衡算 ( 12 ) −=− LLHHV 12 )()( − 12 = LcIIV pL θ −θ 12 全塔热量衡算 ≈ LL 21 12 1122 − )( = pLθ − cLcLIIV pLθ

西北大学化工原理 2、物料衡算微分方程式 在微元控制体内对水分作物料衡算 = dLVdH 式中,V—气体流率,以干气体为基准,kg干气/(s.m2塔截面); L—液相流率,kg/(s.m2塔截面)。 微元体内水分的变化量 = A adzNdL = A adzNVdH = H e − )( dzHHakVdH 将传质速率NA表达式 eHA HHkN )( 带入得 则 = −
西北大学化工原理 2、物料衡算微分方程式 在微元控制体内对水分作物料衡算 = dLVdH 式中,V—气体流率,以干气体为基准,kg干气/(s.m2塔截面); L—液相流率,kg/(s.m2塔截面)。 微元体内水分的变化量 = A adzNdL = A adzNVdH = H e − )( dzHHakVdH 将传质速率NA表达式 eHA HHkN )( 带入得 则 = −

西北大学化工原理 3、热量衡算微分方程式 对微元控制作热量衡算 dLLdcVdI )( = pL θ +θ 式中,I—湿空气的热焓,kJ/kg。 湿空气的热焓:1kg干气的焓及其所带Hkg水汽的焓 之和。 HrHtctcI = pg + pV + 0 对空气-水系统 pH = pg + pV Hccc = + 88.101.1 H 空气的湿比热容 I = + + 2500)88.101.1( HtH kJ/(kg干气.℃) I=f(t,H)
西北大学化工原理 3、热量衡算微分方程式 对微元控制作热量衡算 dLLdcVdI )( = pL θ +θ 式中,I—湿空气的热焓,kJ/kg。 湿空气的热焓:1kg干气的焓及其所带Hkg水汽的焓 之和。 HrHtctcI = pg + pV + 0 对空气-水系统 pH = pg + pV Hccc = + 88.101.1 H 空气的湿比热容 I = + + 2500)88.101.1( HtH kJ/(kg干气.℃) I=f(t,H)

西北大学化工原理 dLLdcVdI )( = pL θ +θ = pL LdcVdI θ pLθ << pL LdcdLc θ qadzdtVc pH = dztadtVc pH = α θ − )( 从传热速率角度考虑,气液两相在微元控制体内传递的 热量qadz等于气体温度升高dt所需要的热量
西北大学化工原理 dLLdcVdI )( = pL θ +θ = pL LdcVdI θ pLθ << pL LdcdLc θ qadzdtVc pH = dztadtVc pH = α θ − )( 从传热速率角度考虑,气液两相在微元控制体内传递的 热量qadz等于气体温度升高dt所需要的热量

西北大学化工原理 4、凉水塔的设计型计算 已知:空气入口状态(t、H) 任务:将一定流量的热水从θ2 θ1 目的:确定塔高 通过实验确定kHa和αa 计算方法: = eH − )( dzHHakVdH HrtcI = pH + 0 = pL LdcVdI θ dztadtVcpH =α θ − )( 计算方法:逐段计算法和以焓差为推动力的近似计算法
西北大学化工原理 4、凉水塔的设计型计算 已知:空气入口状态(t、H) 任务:将一定流量的热水从θ2 θ1 目的:确定塔高 通过实验确定kHa和αa 计算方法: = eH − )( dzHHakVdH HrtcI = pH + 0 = pL LdcVdI θ dztadtVcpH =α θ − )( 计算方法:逐段计算法和以焓差为推动力的近似计算法