
初期温度速度 末期温度速度 在主期中温度上升不小于0.3℃的间隔 (V+V)m AT- 数十第1间隔(不管其是否小于0.3℃)】 2+V.r 在主期中温度上升小于0.3℃的间隔数) 3.3仪器药品 氧弹热量计 1套 氧气钢瓶 1只 压片机 1台 容量瓶 2000mL 1个 万用表 1个 烧杯(1000mL2000mL) 各1只 专用燃烧丝(中间绕几圈成电炉丝状)10~15cm HR一15B多功能控制箱 1台 可与微机连接并打印输出 苯甲酸(AR)1.0~1.2克 萘(AR)0.60.8克 均压成片状。 经典式:贝克曼温度计 现代式:铂电阻+电桥代替贝克曼温度计 新式氧弹与压片机 半自动:热敏电阻探头,数显型或微机型外夹套恒温式。 全自动式:铂电阻传感,WZR~1微电脑精密快速自动热量计,自动数据敔处理。 半自动式:WHR一15A(B)数显型氧弹式(B型可配微机)热量计主机部分: HR一15B多功能控制箱 0000 温度传感探头 网00.000☐ 温度/切换 分雾炎提 环境水夹套 长沙长兴高教仪器设备公司 分伴分厦位揽拥点少 时间间隔数 点火插孔 充放气口 点火插头 螺纹通 接不锈 电极 内搅拌器 盛水内桶 氧弹 杯体 金属小杯 定位圈 进气筍 兼电极 样品片 图2.1.1量热计图 图2.12全自动及半自动式单头氧弹图 3.4实验步骤 1.检验多功能控制器数显读数是否稳定。熟习压片和氧弹装样操作,量热计 安装注意探头不得碰弯,温度与温差的切换功能键钮,报时及灯闪烁提示功能等。 19
19 V r V V m T + + 1 1 2 ( ) = 3.3 仪器药品 氧弹热量计 1 套 氧气钢瓶 1 只 压片机 1 台 容量瓶 2000mL 1 个 万用表 1 个 烧杯(1000mL 2000mL) 各 1 只 专用燃烧丝(中间绕几圈成电炉丝状) 10~15cm HR—15B 多功能控制箱 1 台 可与微机连接并打印输出 苯甲酸(AR)1.0~1.2 克 萘(AR)0.6~0.8 克 均压成片状。 经典式: 贝克曼温度计 现代式: 铂电阻+电桥代替贝克曼温度计 新式氧弹与压片机 半自动: 热敏电阻探头,数显型或微机型外夹套恒温式。 全自动式:铂电阻传感,WZR-1 微电脑精密快速自动热量计,自动数据处理。 半自动式:WHR—15A(B)数显型氧弹式(B 型可配微机)热量计主机部分: 3.4 实验步骤 1. 检验多功能控制器数显读数是否稳定。熟习压片和氧弹装样操作,量热计 安装注意探头不得碰弯,温度与温差的切换功能键钮,报时及灯闪烁提示功能等。 初期温度速度 在主期中温度上升小于 0.3℃的间隔数) 在主期中温度上升不小于 0.3℃的间隔 数+第 1间隔(不管其是否小于 0.3℃)_ 末期温度速度 样品片 金属小杯 电极 螺纹连 接不锈 钢盖和 杯体 充放气口 进气管 兼电极 图 2.1.2 全自动及半自动式单头氧弹图 时间间隔数 点火插孔 图 2.1.1 量热计图 温度传感探头 环 境 水 夹 套 盛水内桶 氧弹 内 搅 拌 器 定位圈 点火插头 HR—15B 多功能控制箱 1 分 半 分 点 火 00 0 0. 0 0 0 温度/切换 搅 拌 长沙长兴高教仪器设备公司 1 分 半分 复位 搅拌 点火

2.干燥恒重苯甲酸(0.9~1.2g)和萘(0.6~0.8g)压片,注意紧实度,分析天平称样 并记录准确称样后质量。 3.容量瓶量取3000mL水,调节水温低于室温1K;注意水是倒入盛水内筒而 非外侧。 4.量取两根10厘米点火丝,中段在原珠笔蕊上绕几圈。燃烧丝缚紧使接触电 阻尽可能小。氧弹充氧注意小动作缓缓旋开减压阀。 5.氧弹内预滴10mL水,促产物凝聚成硝酸。 准阁 ①压苯甲酸片、萘片后,称样、绕点火丝成螺旋状。②量3000m配 水入内筒,多功能控制箱切换温度档测水温、外夹套水温和室温。 氧弹装样 缚铁丝不碰杯,接于两电极良好,放药片靠近自绕的铁丝螺圈。 充氧 氧弹内预注10mL馏水.缓旋减压阀充氧2MPa大气压后复验氧 弹电阻,放水中不冒气泡。漏气则需查明原因。 热量计安装 启盖前拔出探头,氧弹入量热容器内筒水中时不碰搅拌棒。 3000mL水淹至氧弹进气阀螺帽高度的23处.按密度校正重量。 初期记温度: 1次/30s 测温探头插入内筒,触摸搅拌键,数显置零。听控制箱报时读 10个基线温度数据,至0.001℃精度。 主期点火,记上 升温度:1次/30s 氧弹接上点火二电极。触摸点火开关,读温升值, 直到温度达最高折点,主期结束。 末期记温度: 读数目的与初期同,读8个数据以明确温度回落基线作雷诺校 正图的走势。做第二个样品时需换内筒水。重测环境和水温。 1次/min 热容量准确测定完毕,取出氧弹,用放气帽缓缓放气1 分钟,量出未燃尽的引火线长度,计算实际消耗量。用 基准试样宜 150~200mL蒸馏水洗氧弹,得硝酸液量。盛烧杯加盖煮 、准确测定? 沸5分钟,加2滴酚酞,以0.1M氢氧化钠液滴至粉红 色。实验结束,擦净氧弹内外表面及弹盖。整理热量计 Y 数据处理 雷诺图求△T值,利用式(2.1.1)、(2.1.2)求Qy和Qp值。 3.5注意事项 1.实验关键:点火成功、试样完全燃烧是实验成败关键,可以考虑以下几项技 术措施: 20
20 充氧 氧弹装样 热量计安装 缚铁丝不碰杯,接于两电极良好,放药片靠近自绕的铁丝螺圈。 氧弹内预注 10mL 馏水。缓旋减压阀充氧 2MPa 大气压后复验氧 弹电阻,放水中不冒气泡。漏气则需查明原因。 启盖前拔出探头,氧弹入量热容器内筒水中时不碰搅拌棒。 3000mL水淹至氧弹进气阀螺帽高度的 2/3 处。按密度校正重量。 雷诺图求T 值,利用式(2.1.1)、(2.1.2)求 QV 和 Qp值。 读数目的与初期同,读 8 个数据以明确温度回落基线作雷诺校 正图的走势。做第二个样品时需换内筒水。重测环境和水温。 测温探头插入内筒,触摸搅拌键,数显置零。听控制箱报时读 10 个基线温度数据,至 0.001C 精度。 热容量准确测定完毕,取出氧弹,用放气帽缓缓放气 1 分钟,量出未燃尽的引火线长度,计算实际消耗量。用 150~200mL 蒸馏水洗氧弹,得硝酸液量。盛烧杯加盖煮 沸 5 分钟,加 2 滴酚酞,以 0.1M 氢氧化钠液滴至粉红 色。实验结束,擦净氧弹内外表面及弹盖。整理热量计。 氧弹接上点火二电极。触摸点火开关,读温升值, 直到温度达最高折点,主期结束。 2. 干燥恒重苯甲酸(0.9~1.2g)和萘(0.6~0.8g)压片,注意紧实度,分析天平称样 并记录准确称样后质量。 3. 容量瓶量取 3000mL 水,调节水温低于室温 1K;注意水是倒入盛水内筒而 非外侧。 4. 量取两根 10 厘米点火丝,中段在原珠笔蕊上绕几圈。燃烧丝缚紧使接触电 阻尽可能小。氧弹充氧注意小动作缓缓旋开减压阀。 5. 氧弹内预滴 10mL 水,促产物凝聚成硝酸。 3.5 注意事项 1. 实验关键:点火成功、试样完全燃烧是实验成败关键,可以考虑以下几项技 术措施: 准备 ①压苯甲酸片、萘片后,称样、绕点火丝成螺旋状。②量 3000mL 水入内筒,多功能控制箱切换温度档测水温、外夹套水温和室温。 初期记温度: 1 次/30s 主期点火,记上 升温度:1 次/30s 末期记温度: 1 次/min 基准试样宜 准确测定? 数据处理 Y N

①试样应进行磨细、烘干、干燥器恒重等前处理,潮湿样品不易燃烧且有误 差。 压片紧实度:一般硬到表面有较细密的光洁度,棱角无粗粒,使能燃烧又不至于 引起爆炸性燃烧残剩黑糊等状。 ②点火丝与电极接触电阻要尽可能小,注意电极松动和铁丝碰杯短路问题。 ③充足氧(2MP)并保证氧弹不漏氧,保证充分燃烧。燃烧不完全,还时常形 成灰白相间如散棉絮状。 ④注意点火前才将二电极插上氧弹并对准再按点火钮,否则因仪器未设互锁 功能,极易发生(按搅拌钮或置0时)误点火,样品先已燃烧的事故。 2.氧弹内预滴几滴水,使氧弹为水汽饱和,燃烧后气态水易凝结为液态水。 试样在氧弹中燃烧产生的压力可达14MP,长期使用,可能引起弹壁的腐蚀, 减少其强度。故氧弹应定期进行20MPa水压检查,每年一次。 氧弹、量热容器、搅拌器等,在使用完毕后,应用干布擦去水迹,保持表面 清洁干燥。恒温外套(即外简)内的水,应采用软水。长期不使用时应将水倒掉。 氧弹以及氧气通过的各个部件,各联接部分不允许有油污,更不允许使用润 滑油,在必须润滑时,可用少量的甘油。 3.仪器应置放在不受阳光直射的单独一间试验室内进行工作。室内温度和湿度 应尽可能变化小。最适宜的温度是20士5℃。每次测定时室温变化不得大于1℃。 因此。室内禁止使用各种热源,如电炉、火炉、暖气等。 4.如用贝克曼温度计,其调节可以归纳为倒立连接、设定温度、正立震断和校 验四步,注意别让水银过多地流向弯曲贮管,导致因水银重而在正立时,玻管扩 张处挂不住。也绝不允许放在电炉上烤等骤冷骤热情况出现。在精密的测量中, 应进行贝克曼温度计的校正。改进后的本实验普遍采用热敏电阻温度计、铂电阻 温度计或者热电堆等,相应配以电桥、指示V值,实际己转换为温度(数显温 度计)的仪器,能自动记录温度,精密度可达104~10-5K。国产型号为半自动 HR一15A(B)数显微机型或WHR一15全自动微机型氧弹式热量计。进入了全面 启用电脑处理数据的新时代。 5.苯甲酸和萘燃烧产物的热容差别因为产物量小而仪器热容的基数相对较大而 可以忽略。 21
21 ①试样应进行磨细、烘干、干燥器恒重等前处理,潮湿样品不易燃烧且有误 差。 压片紧实度:一般硬到表面有较细密的光洁度,棱角无粗粒,使能燃烧又不至于 引起爆炸性燃烧残剩黑糊等状。 ②点火丝与电极接触电阻要尽可能小,注意电极松动和铁丝碰杯短路问题。 ③充足氧(2MPa)并保证氧弹不漏氧,保证充分燃烧。燃烧不完全,还时常形 成灰白相间如散棉絮状。 ④注意点火前才将二电极插上氧弹并对准再按点火钮,否则因仪器未设互锁 功能,极易发生(按搅拌钮或置 0 时)误点火,样品先已燃烧的事故。 2. 氧弹内预滴几滴水,使氧弹为水汽饱和,燃烧后气态水易凝结为液态水。 试样在氧弹中燃烧产生的压力可达 14MPa,长期使用,可能引起弹壁的腐蚀, 减少其强度。故氧弹应定期进行 20MPa 水压检查,每年一次。 氧弹、量热容器、搅拌器等,在使用完毕后,应用干布擦去水迹,保持表面 清洁干燥。恒温外套(即外筒)内的水,应采用软水。长期不使用时应将水倒掉。 氧弹以及氧气通过的各个部件,各联接部分不允许有油污,更不允许使用润 滑油,在必须润滑时,可用少量的甘油。 3. 仪器应置放在不受阳光直射的单独一间试验室内进行工作。室内温度和湿度 应尽可能变化小。最适宜的温度是 205℃。每次测定时室温变化不得大于 1℃。 因此。室内禁止使用各种热源,如电炉、火炉、暖气等。 4. 如用贝克曼温度计,其调节可以归纳为倒立连接、设定温度、正立震断和校 验四步,注意别让水银过多地流向弯曲贮管,导致因水银重而在正立时,玻管扩 张处挂不住。也绝不允许放在电炉上烤等骤冷骤热情况出现。在精密的测量中, 应进行贝克曼温度计的校正。改进后的本实验普遍采用热敏电阻温度计、铂电阻 温度计或者热电堆等,相应配以电桥、指示 mV 值,实际已转换为温度 (数显温 度计) 的仪器,能自动记录温度,精密度可达 10−4~10−5K。国产型号为半自动 HR—15A(B)数显微机型或 WHR—15 全自动微机型氧弹式热量计。进入了全面 启用电脑处理数据的新时代。 5. 苯甲酸和萘燃烧产物的热容差别因为产物量小而仪器热容的基数相对较大而 可以忽略
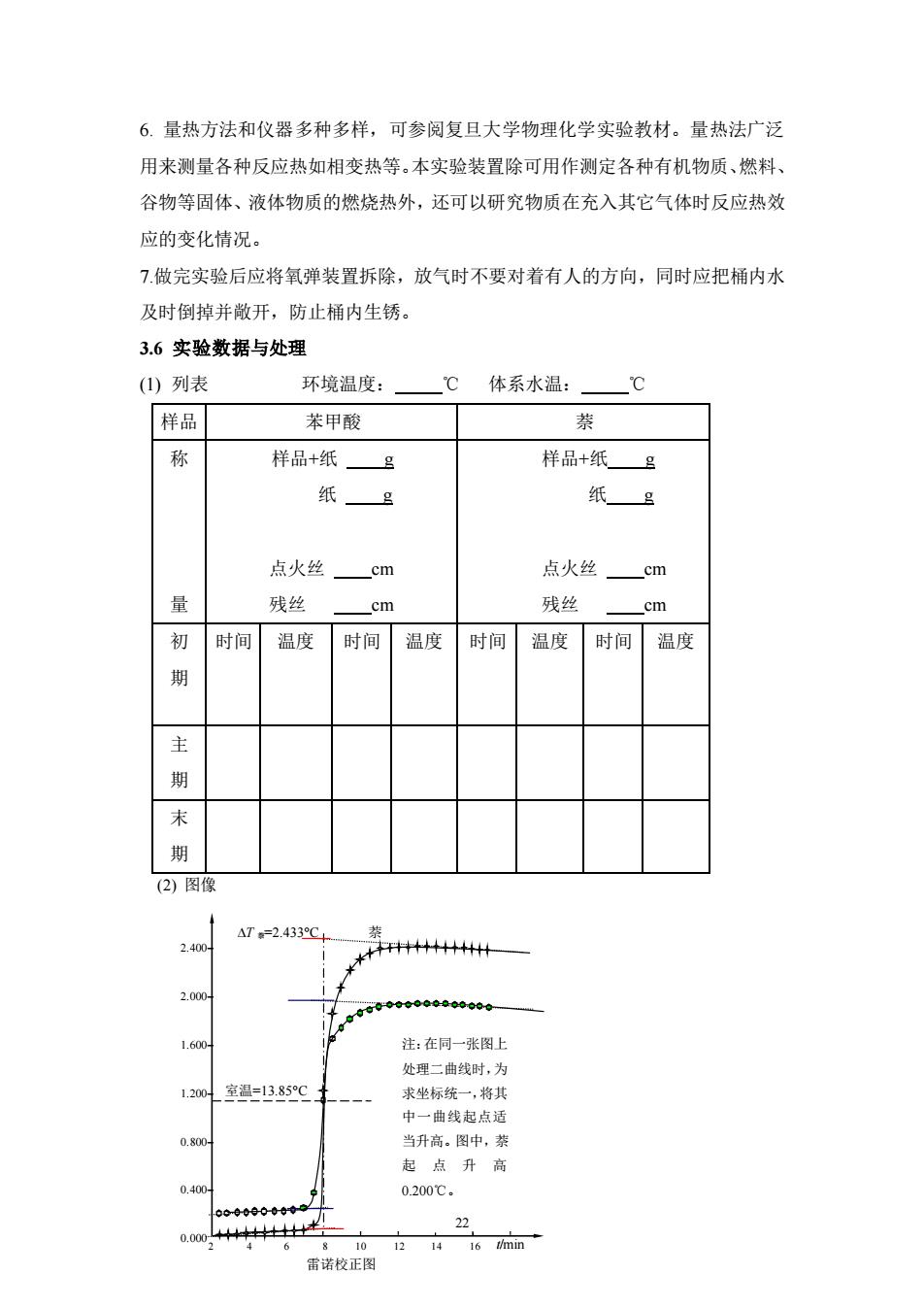
6.量热方法和仪器多种多样,可参阅复旦大学物理化学实验教材。量热法广泛 用来测量各种反应热如相变热等。本实验装置除可用作测定各种有机物质、燃料、 谷物等固体、液体物质的燃烧热外,还可以研究物质在充入其它气体时反应热效 应的变化情况。 7做完实验后应将氧弹装置拆除,放气时不要对着有人的方向,同时应把桶内水 及时倒掉并敞开,防止桶内生锈。 3.6实验数据与处理 (1)列表 环境温度: C 体系水温: ℃ 样品 苯甲酸 萘 称 样品+纸 g 样品+纸g 纸 g 纸g 点火丝cm 点火丝 cm 量 残丝 cm 残丝 cm 初 时间 温度 时间 温度 时间 温度 时间 温度 期 主 期 末 期 (2)图像 △T=2.433C 2.400 ++++ 2.000 1.600- 注:在同一张图上 处理二曲线时,为 1.200 室温=13.85C 求坐标统一,将其 中一曲线起点适 0.800 当升高。图中,萘 起点升高 0.400 0.200℃。 0⊙00日000t9 0.0002 林4牡 22 6 8101214 16 t/min 雷诺校正图
22 6. 量热方法和仪器多种多样,可参阅复旦大学物理化学实验教材。量热法广泛 用来测量各种反应热如相变热等。本实验装置除可用作测定各种有机物质、燃料、 谷物等固体、液体物质的燃烧热外,还可以研究物质在充入其它气体时反应热效 应的变化情况。 7.做完实验后应将氧弹装置拆除,放气时不要对着有人的方向,同时应把桶内水 及时倒掉并敞开,防止桶内生锈。 3.6 实验数据与处理 (1) 列表 环境温度: ℃ 体系水温: ℃ 样品 苯甲酸 萘 称 量 样品+纸 g 纸 g 点火丝 cm 残丝 cm 样品+纸 g 纸 g 点火丝 cm 残丝 cm 初 期 时间 温度 时间 温度 时间 温度 时间 温度 主 期 末 期 (2) 图像 T 萘=2.433C 萘 2 4 6 8 10 12 14 16 t/min 雷诺校正图 2.400− 2.000− 1.600− 1.200− 0.800− 0.400− 0.000 注:在同一张图上 处理二曲线时,为 求坐标统一,将其 中一曲线起点适 当升高。图中,萘 起点升高 0.200℃。 室温=13.85C

(3)计算 M苯甲酸=122.12 M=128.11 ①求卡计水当量C,(JK-1) ②求萘的恒容燃烧热 ③求萘的恒压燃烧热Qp=Qv+AnRT ④误差估算 (4)误差分析与结果要求 实验的主要误差来自绝热条件不够引起的热辐射即热泄漏问题。理想的热量 计应做到量热系统与作为环境的①外夹套水同步升温:②搅拌热的修正问题。改 进后的精密弹式量热计。重复性测量误差通常能达到小于0.1%,一些与现代电 子技术相关的完全自动化的热量测定仪器已经进入实验室。不过为了考虑实验原 理的教学需要而有时反而更青睐半自动仪器。 3.7思考题 1.量热计中哪些部分是系统?哪些部分是环境?系统和环境通过哪些途径进 行热交换? 2.使用氧气应注意哪些问题?用电解水制得的氧气可否直接用来做本实验? 为什么? 3.本实验测得的是Qv还是Q?它们相差多少?如何换算? 预习与提问 (1)什么是燃烧热?其终极产物是什么? (2)实验测仪器常数采用什么样的办法?水当量是什么含义? (3)氧弹式热量计测燃烧热的简单原理?主要测量误差是什么?如何求Q? (4)为什么说高精度的燃烧热数据较之生成热数据更显得必要? 23
23 (3) 计算 M 苯甲酸=122.12 M 萘=128.11 ①求卡计水当量 CJ(JK−1) ②求萘的恒容燃烧热 ③求萘的恒压燃烧热 QP=QV+nRT ④误差估算 (4) 误差分析与结果要求 实验的主要误差来自绝热条件不够引起的热辐射即热泄漏问题。理想的热量 计应做到量热系统与作为环境的①外夹套水同步升温;②搅拌热的修正问题。改 进后的精密弹式量热计。重复性测量误差通常能达到小于 0.1%,一些与现代电 子技术相关的完全自动化的热量测定仪器已经进入实验室。不过为了考虑实验原 理的教学需要而有时反而更青睐半自动仪器。 3.7 思考题 1.量热计中哪些部分是系统?哪些部分是环境?系统和环境通过哪些途径进 行热交换? 2.使用氧气应注意哪些问题?用电解水制得的氧气可否直接用来做本实验? 为什么? 3.本实验测得的是 QV 还是 Qp?它们相差多少?如何换算? 预习与提问 (1) 什么是燃烧热?其终极产物是什么? (2) 实验测仪器常数采用什么样的办法?水当量是什么含义? (3) 氧弹式热量计测燃烧热的简单原理?主要测量误差是什么?如何求 Qp? (4) 为什么说高精度的燃烧热数据较之生成热数据更显得必要?