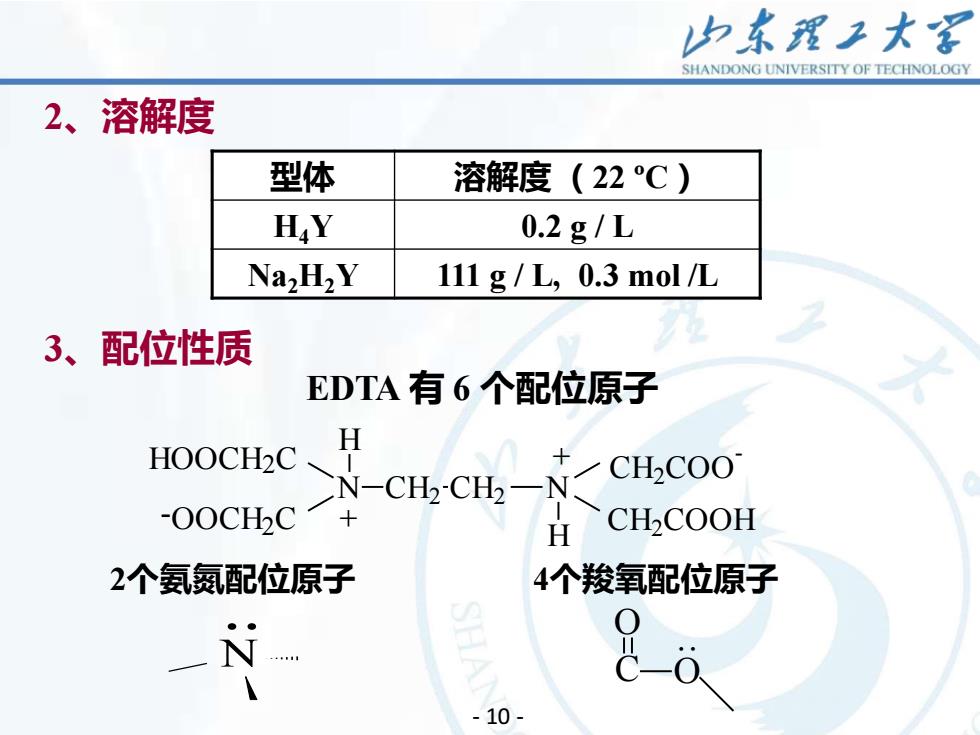
山东理工大客SHANDONGUNIVERSITYOFTECHNOLOGY2、溶解度型体溶解度(22 °℃)HY0.2 g / LNa,H,Y111 g / L, 0.3 mol /L九3、配位性质EDTA有6个配位原子H1HOOCH20十CH2COON-CH2-CH2-N-00CHC+CH2COOHH2个氨氮配位原子4个羧氧配位原子0NP1- 10 -
11 2、溶解度 型体 溶解度 (22 ºC) H4Y 0.2 g / L Na2H2Y 111 g / L, 0.3 mol /L 3、配位性质 EDTA 有 6 个配位原子 HOOCH2C N H CH2 COO - CH2 COOH N H CH2 CH2 -OOCH2 C + + 2个氨氮配位原子 N . 4个羧氧配位原子 O C O . - 10 -
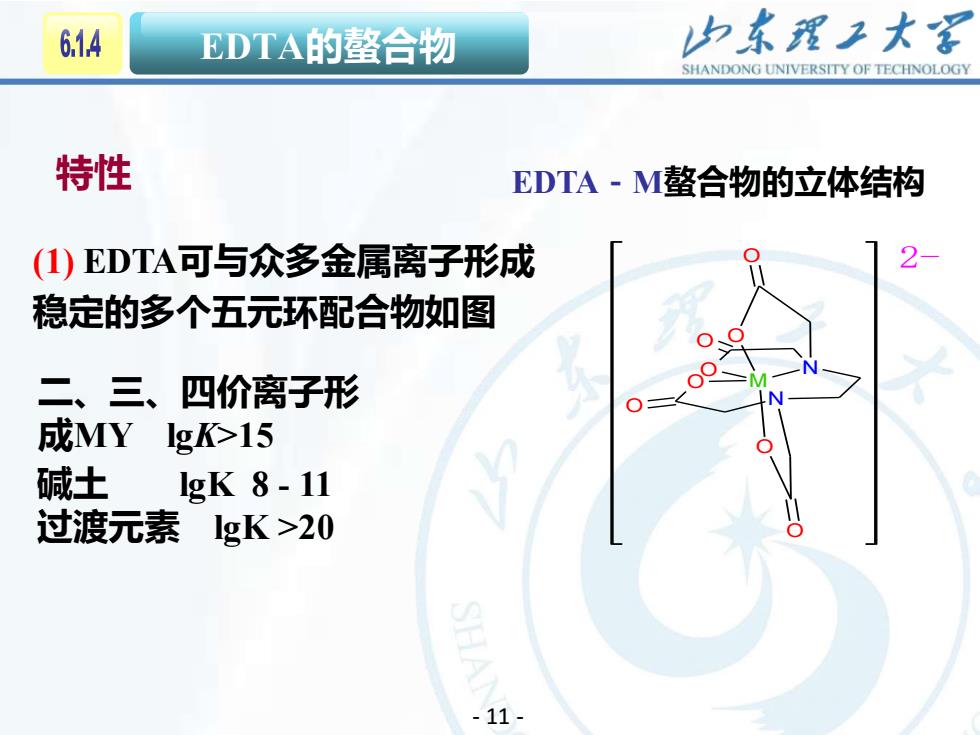
山东理工大客6.1.4EDTA的螯合物SHANDONGUNIVERSITYOFTECHNOLOGY特性EDTA-M螯合物的立体结构2-EDTA可与众多金属离子形成(1)稳定的多个五元环配合物如图店二、三、四价离子形成MY IgK>15碱土IgK 8 - 11过渡元素IgK >2011
12 EDTA的螯合物 EDTA-M螯合物的立体结构 N M N O O O O O O O (1) EDTA可与众多金属离子形成 O 2- 稳定的多个五元环配合物如图 二、三、四价离子形 成MY lgK>15 碱土 lgK 8 - 11 过渡元素 lgK >20 特性 - 11 -

山东理工大客SHANDONGUNIVERSITYOFTECHNOLOGY(2)配合比固定而简单,多数为1:1型,少数为2:1型(如 : Mo(V))计量数关系为1:1,通式(略电荷):M+Y-MY强配合物带电荷且易溶于水(3)(4)反应快,滴定终点易判断EDTA与无色的金属离子形成无色的络合物;金属离子带色(5)形成MY也带色且颜色加深,可定性分析CuYCoYNiYMnY(紫红)(深蓝)(蓝绿(玫瑰)Fe(OH)Y2CrYCr(OH)Y2-FeY黄(蓝)(褐)(深紫)- 12 -
13 (5) EDTA与无色的金属离子形成无色的络合物;金属离子带色, 形成MY也带色且颜色加深,可定性分析 CuY NiY CoY MnY (深蓝) (蓝绿) (玫瑰) (紫红) CrY Cr(OH)Y2- FeY Fe(OH)Y2- (深紫) (蓝) (黄) (褐) (3) 配合物带电荷且易溶于水 (4) 反应快,滴定终点易判断 (2) 配合比固定而简单,多数为1:1型,少数为2:1型 (如:Mo(Ⅴ)) 计量数关系为1:1,通式(略电荷): M+Y=MY - 12 -

山东理工大客6.2络合物的平衡常数一一稳定常数SHANDONGUNIVERSITY OFTECHNOLOGY6.2.1络合物的稳定常数一、螯合物(1:1型络合物)[CaY?-]Cay2-Ca2+ + Y4- K稳[Ca?+]·[Y4-][MY]KMYM+YEMY[M]·[Y]- 13 -
14 络合物的平衡常数——稳定常数 络合物的稳定常数 [Ca ] [ ] [C Y ] 2 4 2 + − − = Y a Ca K稳 2+ + Y 4- CaY 2- 一、螯合物(1:1型络合物) M + Y MY [M] [Y] [MY] KMY = - 13 -

山东理工大客二、1:n型络合物(简单络合物)SHANDONGUNIVERSITYOFTECHNOLOGY1、逐级稳定常数K稳金属离子M能与配位剂L逐步形成ML.型配合物,每一步都有配位平衡和相应的稳定常数(逐级稳定常数K稳)[ML]KM+L←ML稳1[M][L][ML,]KML+LML稳2[ML][L][ML,]K稳nMLn-1 +L<←ML[ML,-I ][L]- 14 -
15 二、 1:n型络合物(简单络合物) 金属离子M能与配位剂L逐步形成MLn型配合物,每一 步都有配位平衡和相应的稳定常数(逐级稳定常数K稳n ) M+ L ML [ ][ ] [ ] 1 M L ML K稳 = ML + L ML2 [ ][ ] [ ] 2 2 ML L ML K稳 = MLn−1 + L MLn [ ][ ] [ ] ML 1 L ML K n n n − 稳 = 1、逐级稳定常数K稳 ● ● ● ● ● ● - 14 -