
常见的变化过程有: (1)等温过程 T=T=T环 (2)等压过程 P1=P2=P环 (3)等容过程 d/=0 (4)绝热过程 2=0 (5)环状过程 ∮dW=0 (循环过程)
(1)等温过程 (2)等压过程 (3)等容过程 (4)绝热过程 (5)环状过程 (循环过程) T T T 1 2 = = 环 1 2 p p p = = 环 d 0 V = Q = 0 d 0 U = 常见的变化过程有:

7.热和功 (1)热(heat) 系统与环境之间因温度不同而传递的能量称为热, 用符号卫表示。 Q的取号: 系统吸热,Q>0 系统放热,Q<0 热总是与大量分子的无规则运动相联系 计算热一定要与系统与环境之间发生热交换的过程 联系在一起,系统内部的能量交换不可能是热
系统吸热,Q>0 系统放热,Q<0 (1)热(heat) 系统与环境之间因温度不同而传递的能量称为热, 用符号Q 表示。 7. 热和功 Q的取号: 热总是与大量分子的无规则运动相联系 计算热一定要与系统与环境之间发生热交换的过程 联系在一起,系统内部的能量交换不可能是热

7.热和功 (2)功(work) 系统与环境之间传递的除热以外的其他能量都称 为功,用符号W表示。 W的取号: 环境对系统作功,>0 系统对环境作功,W<0 2和的单位都用能量单位“J”表示 Q和W都不是状态函数,其数值与变化途径有关。 2和W的微小变化用符号"δ"而不能用"d”表示
(2)功(work) 系统与环境之间传递的除热以外的其他能量都称 为功,用符号W表示。 环境对系统作功,W>0 系统对环境作功,W<0 W的取号: Q和W的微小变化用符号" " 而不能用 "d" 表示 Q和W的单位都用能量单位 “J” 表示 Q和W都不是状态函数,其数值与变化途径有关。 7. 热和功

7.热和功 广义的功可以看作强度因素与广度因素变化量的乘积 5W=-pdV+(Xdx+Ydy+Zdz+.) =δW.+δW 式中p,X,Y,Z,.是强度因素 dV,dx,y,dz.是相应的广度因素变化量 功可以分为膨张功和非膨胀功,热力学中 一般不考虑非膨胀功
广义的功可以看作强度因素与广度因素变化量的乘积 δW = − + + + + p V X x Y y Z z d ( d d d ) e f = + δW Wδ 式中 p X Y Z , , , , 是强度因素 d d d d V x y z , , , 是相应的广度因素变化量 功可以分为膨胀功和非膨胀功,热力学中 一般不考虑非膨胀功 7. 热和功
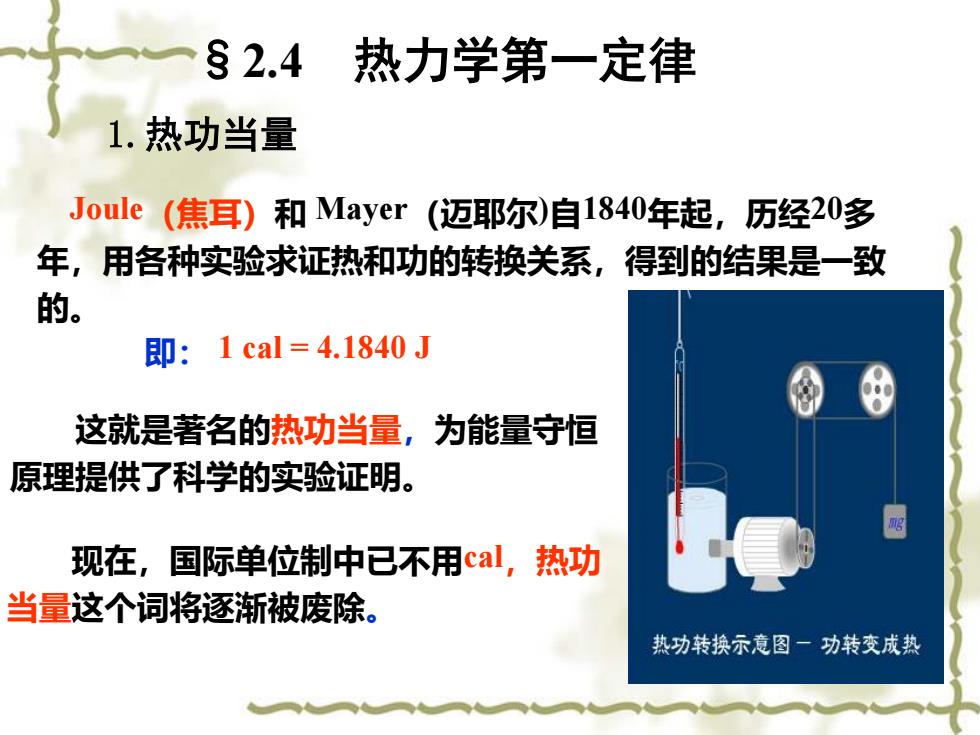
§2.4 热力学第一定律 1.热功当量 Joule(焦耳)和Mayer(迈耶尔)自1840年起,历经20多 年,用各种实验求证热和功的转换关系,得到的结果是一致 的。 即:1cal=4.1840J 这就是著名的热功当量,为能量守恒 原理提供了科学的实验证明。 现在,国际单位制中已不用cal,热功 当量这个词将逐渐被废除。 热功转换示意图一功转变成热
§2.4 热力学第一定律 Joule(焦耳)和 Mayer(迈耶尔)自1840年起,历经20多 年,用各种实验求证热和功的转换关系,得到的结果是一致 的。 这就是著名的热功当量,为能量守恒 原理提供了科学的实验证明。 即: 1 cal = 4.1840 J 现在,国际单位制中已不用cal,热功 当量这个词将逐渐被废除。 1.热功当量