
第十三章氨基酸,蛋白质和核酸 除了脂类和糖类化合物以外,重要的生物大分子还有蛋白质和核酸,这两类化合物是构 成生命的基本物质,其中核酸是遗传信息的携带者,为生命的外在形式提供了建设蓝图,而 蛋白质侧承担着各种各样复杂的生理功能,从整体上维持着生物机体新陈代谢活动的进行。 因此,生命是蛋白质的存在形式,而生命的基本特征就是蛋白质的不断自我更新。 多糖盼水解 低聚糖完全水解 苷键把多个单糖基本单元以同种或不 单糖同的方式连接起来,构成多糖分子链。 肆(珠安建)巴多个写其哈其太 蛋白质部分水解 多肽 完全水解 氨基酸 单元方式按 序连接起来,构成蛋白 质分子链。氨基酸是构成蛋白质的基石。 S13-1氨基酸(Aminoacid) 一、分类,命名和构型 1.分类 「脂肪族 ()按R结构 芳香族 (2按CO0H和-NH, 的相位置 杂环 迄今发现的天然氨基酸有700多种,但组成蛋白质的氨基酸有20余种,而受遗传密码 支配的氨基酸只有20种,且其中19种都属于-氨基酸。 中性 pH≠7 (3)按分子中所含 -0 的个数 减性 pH-7 酸性 pH<7 ,R为脂肪烃基 R中含有羟基和硫 非极性 (4)按RCHNH2COOH中 R中含有芳基 (⑤)按氨基酸在生理 带正电 侧链R一的性质 R中含有碱性基团 带负电 R中含有酸性基团 条件下的解离 不带点 R中含有酰胺基 ·R为环状 (6按来自遗传信息调控?

2.命名 氨基酸多用俗名,即根据来源和性质命名,在表达多肽和蛋白质结构时,常用英文名 称的前三个字母表示,也可用中文名称的第一个或前两个字表示。详见教材。 3.c-氨基酸的构型 受遗传密码支配的20种RC*HNH,COOH中,除甘复酸外,其余19种均为手性分子,且 都是L型。苏氨酸和异亮复酸另有一个不对称碳原子。细菌体内有少数D-型复基酸。 CHO COOH COOH HO- 一H HO —H H2N- CHOH CH3 R L(-)-甘油醛 L(+乳酸 L氨基酸 单糖分子中决定构型OH所连的C*距离羰基最远,而-氨基酸分子中决定构型的 -NH所连的C*(Q~C)距离羧基最近。 二、-氨基酸的物理性质 mp.较高,一般在200-300℃,加热到mp.时常易分解。一般能溶于水,不溶于石油醚等 非极性溶剂。 三、c-氨基酸的化学性质 一COOH→羧酸的性质 -COOH 相互影响 特性 一NH→1°胺的性质 L1.两性和等电点((Isocricpoint) R-CH-COO÷H=R—CH-COO :NH2 NH3+ 内盐(偶极离子或两性离子) 固体氨基酸→是格中的结点之间靠静电引力形戒是体·品格能↑·mp.↑ 接受质子:碰性 RCHCOOH HCI- -RCHCOOH NH2 :NH3+CI- 给出质子:酸性 RCHCOOH NaOH- ·RCHCOONa+H2O :NH2 :NH2

各种-氨基酸在水溶液中的存在形式,取决于氨基酸的结构和水溶液的H值 RCHCOO Ht OH- -RCHCO0一O=-RCHCOOH :NH2 NH3 :NH3+ 负离子 偶极离子 正离子 (在强礪溶液中的 (在强酸溶液中的 主要存在形式) 主要存在形式) pH>pl pH=pl pH<pl +→强酸性溶液,一NH接受质子→NH,]远大于[CO0]→在电场中向负极移动 抑制一COOH电离 +OH→强减性溶液→一NH,失去质子→[COO]远大于NH]→在电场中向负极移动 促进-COOH电离 调节溶液的pH值→[CO0]NH,门]→在电场中不发生迁移→此时溶液的pH值称为该氨基酸的 等电点,用pl表示 酸性氨基酸水溶液→pH<7-[CO0]>NH门+H广-→抑制COOH电离pH=pl (pl值:2.8-3.2) 一NH接受质子 减性氨基酸水溶液-pHK7-[CO0]<NH门+OH促进COOH电离pH=pl (pl值:7.6-10.8) -NH*失去质子 中性氨基酸水溶液pH路7-[C00]路NH门+少量H,抑制-COOH电离pH=p (pl值:一般在56.3) 一NH2接受质子 应用不同的氨基酸,p值各不相同。在等电点时,氨基酸呈电中性,在电场中不迁移, 且偶极离子的浓度最高,而复基酸的溶解度最小,易生成沉淀。可用调节H值的方法,分离 氨基酸混合物。常用的方法:分级沉淀,电泳和色谱法。 这种两性解离性质为20种α-氨基酸所共有,共同赋子蛋白质的两性解离特性。氨基酸的 两性解离性质是氨基酸和蛋白质最主要的化学特性。理解和运用这一性质,是分离、纯化氨 基酸和蛋白质,进而理解核酸性质,理解生物大分子的构象和之间的相互作用以及酶作用的 机理等分子生物学基本理论的基础。 2.脱羧反应(α-取代酸的共性) RCHCOOH 或脱酶RCH2NH2+CO2 NH2 2
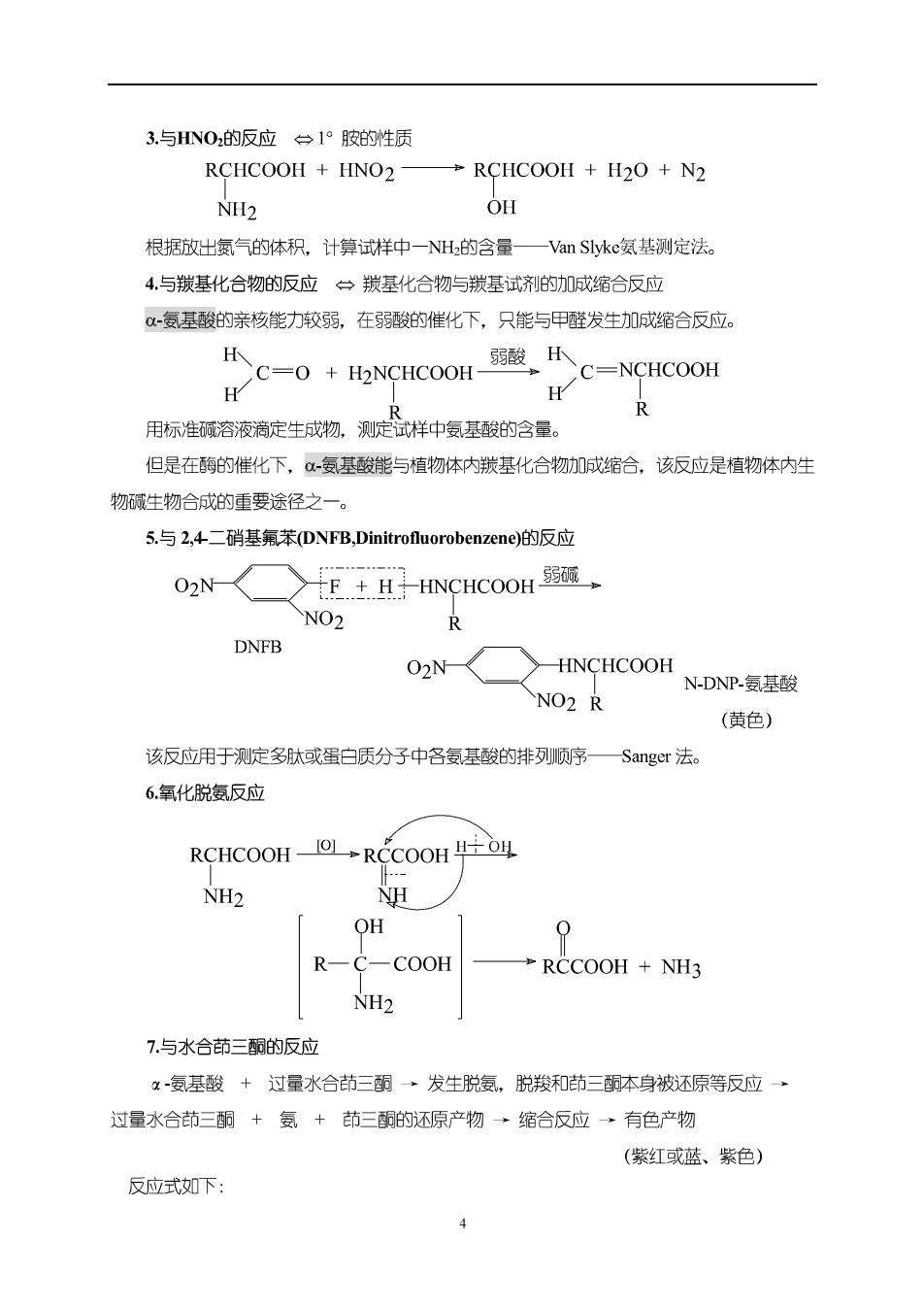
3.与HNO的反应一1°胺的性质 RCHCOOH HNO2 →RCHCOOH+H2O+N2 NH2 OH 根据放出氨气的体积,计算试样中一NH的含量—Van Slyke氨基测定法。 4.与羰基化合物的反应一羰基化合物与羰基试剂的加成缩合反应 -氨基酸的亲核能力较弱,在弱酸的催化下,只能与甲醛发生加成缩合反应。 H H >C=0+H2 CHCOOH-弱酸K C=NCHCOOH 用标准诚溶液滴定生成物,测定试样中复基酸的含量。 但是在酶的催化下,α-氨基酸能与植物体内羰基化合物加成缩合,该反应是植物体内生 物碱生物合成的重要途径之一。 5.与2,4二硝墓氣苯(DNFB,Dinitrofluorobenzene)的反应 02N< FH HNCHCOOH NO2 R DNFB O2N〈>-HNCHCOOH NO2 R N-DNP-氨基酸 (黄色) 该反应用于测定多肽或蛋白质分子中各复基酸的排列顶序一—Sanger法。 6.氧化脱氨反应 RCHCOOH-0L+RCCOOH NH2 H OH 0 R一C-COOH RCCOOH NH3 NH2 7.与水合茚三酮的反应 x-氨基酸+过量水合茚三霸发生脱复,脱羧和茚三酮本身被还原等反应→ 过量水合茚三酮+氨+茚三的还原产物→缩合反应→有色产物 (紫红或蓝、紫色) 反应式如下:
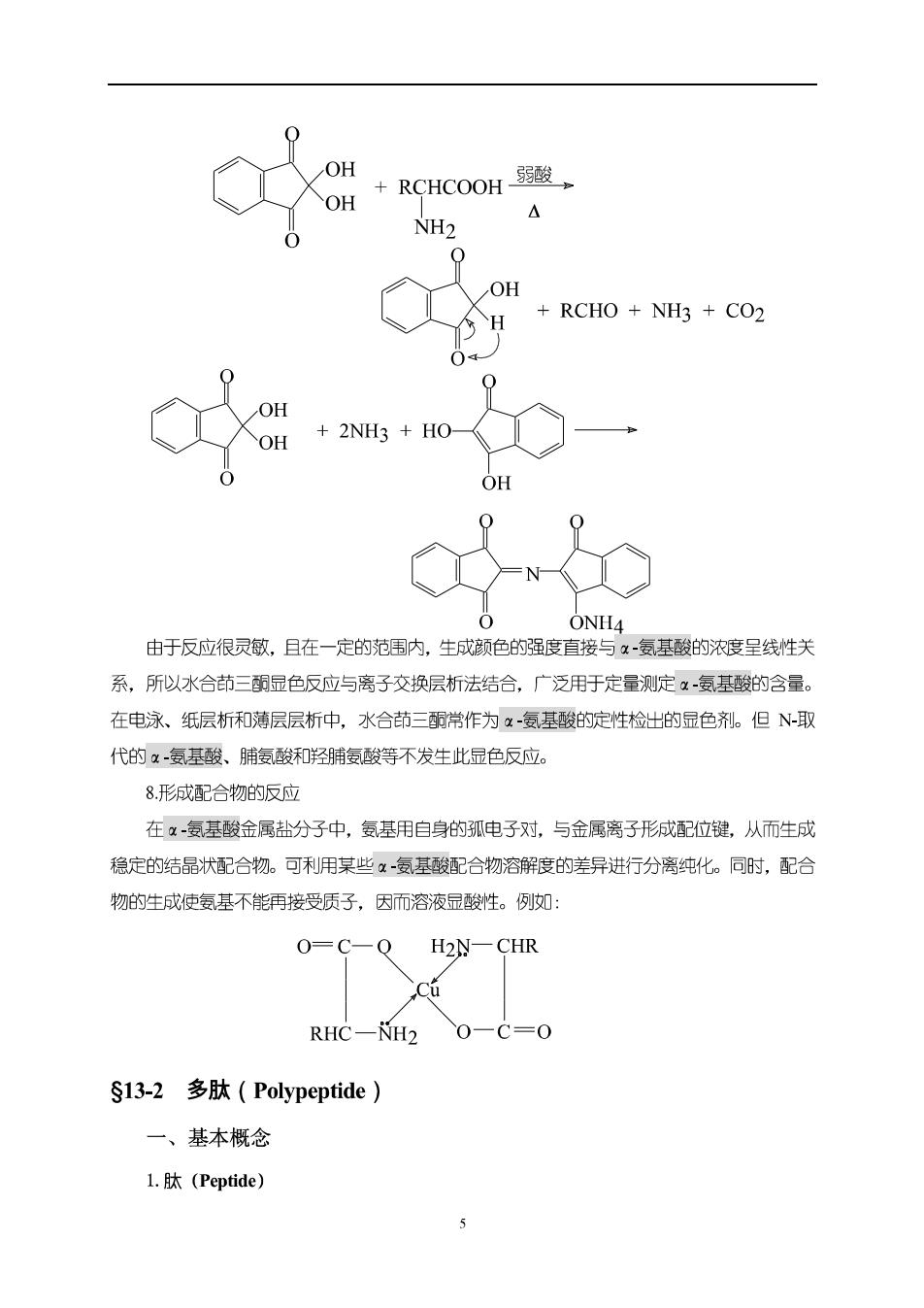
0 OH OH +RCHCOOH弱酸 NH2 OH H RCHO NH3 CO2 O 2NH3 HO- OH 0 ONH4 由于反应很灵敏,且在一定的范用内,生成颜色的强度直接与x-氨基酸的浓度呈线性关 系,所以水合茚三酮显色反应与离子交换层析法结合,广泛用于定量测定x氨基酸的含量。 在电泳、纸层析和薄层层析中,水合茚三酮常作为x-氨基酸的定性检出的显色剂。但N-取 代的x-氨基酸、脯氨酸和羟脯氨酸等不发生此显色反应。 8.形成配合物的反应 在x-复基酸金属盐分子中,氨基用自身的孤电子对,与金属离子形成配位键,从而生成 稳定的结晶状配合物。可利用某些α氨基酸配合物溶解度的嗟异进行分离纯化。同时,配合 物的生成使复基不能再接受质子,因而溶液显酸性。例如: O=C-Q H2N-CHR RHC-H2O一C=O S13-2多肽(Polypeptide)】 一、基本概念 l.肽(Peptide)