
解:由于0=0.344V,是铜电极对NHE而言 ,故铜电极对WE的电极电位为: 0.05 0=0+ log[Cu2]. 2 =0.344+ 0.059 og[0.01] 2 =0.285(V 换算成对SCE的电极电位为: pc=0.285-0.242=0.043W) 给酒渭商業大 HARBIN LNTVERSTTY OF COMMERCE
0.285 0.242 0.043( ) 0.285( ) log[ 0.01] 2 0.059 0.344 log[ ] 2 0.059 0.344 2 V SCE V C u NHE V NHE Cu = − = = = + = + = − + − 换算成对 的电极电位为: 故铜电极对 的电极电位为: 解:由于 ,是铜电极对 而言

电位测定法:根据测量某一电极的电位,再由 能斯特方程直接求得待测物质的浓度(活度)。 电位滴定法:根据滴定过程中,某个电极电位 的突变来确定滴定终点,·从滴定剂的体积和 浓度来计算待测物的含量。 疮潮清月業大孕 HARBIN LNTVERSITY OP COMMERCE
电位测定法:根据测量某一电极的电位,再由 能斯特方程直接求得待测物质的浓度(活度)。 电位滴定法:根据滴定过程中,某个电极电位 的突变来确定滴定终点,从滴定剂的体积和 浓度来计算待测物的含量

第二节电位分析法基本原理 电位分析法:电化学分析法的重要分支,其实 。 质是通过零电流情况下测得两电极之间的电 位差(即所构成原电池的电动势)进行分析 测定。 电位分析法包括: 电位测定法 电位滴定法 给酒演商常大是 HARBIN LNTVERSTTY OF COMMERCE
第二节 电位分析法基本原理 电位分析法:电化学分析法的重要分支,其实 质是通过零电流情况下测得两电极之间的电 位差(即所构成原电池的电动势)进行分析 测定。 电位分析法包括: 电位测定法 电位滴定法

能斯特方程-电位分析法的依据 0.059 p.=0+2l0g [Ox] n [Re d] 上式(能斯特方程),给出了电极电位与溶液中对应离 子活度的简单关系。 对于氧化还原体系,应用该公式,通过测定一个可逆电 池的电位来确定溶液中某组分的离子活度或浓度的方法 就是电极电位法。 哈蘭頌商業大孕 HARBIN LNTVERSITY OP COMMERCE
能斯特方程-电位分析法的依据 [Re ] [ ] log 0.059 d Ox n = + − 上式(能斯特方程),给出了电极电位与溶液中对应离 子活度的简单关系。 对于氧化还原体系,应用该公式,通过测定一个可逆电 池的电位来确定溶液中某组分的离子活度或浓度的方法 就是电极电位法
第三节参比电极与指示电极 单个电极的电位是无法测 量的,因此,由待测电极 电位计 与参比电极组成电池用电 位计测量该电池的电动势, 指示 参比电 电极 即可得到该电极的相对电 位。相对于同一参比电极 的的不同电极的相对电位 是可以相互比较的,并可 用于计算电池的电动势。 常用的参比电极有标准氢 电极与甘汞电极。 给酒渭商業大是 HARBIN LNTVERSTTY OF COMMERCE
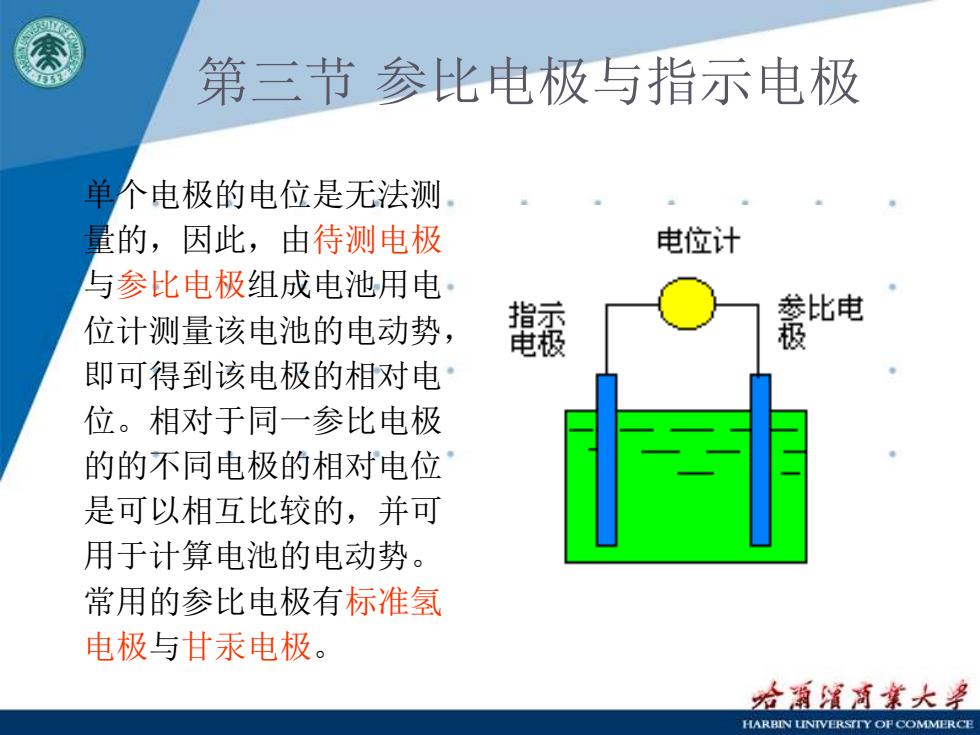
第三节 参比电极与指示电极 单个电极的电位是无法测 量的,因此,由待测电极 与参比电极组成电池用电 位计测量该电池的电动势, 即可得到该电极的相对电 位。相对于同一参比电极 的的不同电极的相对电位 是可以相互比较的,并可 用于计算电池的电动势。 常用的参比电极有标准氢 电极与甘汞电极