
例1 g1molL-HC1溶液中,cce4+=1.00×102molL1, cce3+=1.00×103 mol-L-时Ce4+/Ce3+电对的电势? 解: 查表得:E8o=128 .E=1.28+0.059lg 1.00×10-2 1.00×10-3 =1.34V 上一页 下一页返回退出
上一页 下一页 返回 退出 例 1 1mol·L-1HCl 溶液中 , cCe 4+=1.00×10-2 mol·L-1 , cCe 3+ =1.00×10-3mol·L-1时Ce4+ /Ce3+电对的电势? 解: E V E V Ce Ce 1.34 1.00 10 1.00 10 1.28 0.059lg 1.28 3 2 0 / 4 3 = = + = − − 查表得: + + 返回

例2 矿在1 mol-L-HC1溶液中,用固体亚铁盐将 0.100molL-1K2Cr207还原至一半时的电势? 解: 查表得:E8o,o+=1.00r ·E=1.00+ 0.0590.0500 6 =1.01y 0.1002 上一页下一页返回退出
上一页 下一页 返回 退出 例 2 在 1mol·L-1HCl 溶液中 , 用 固 体 亚 铁 盐 将 0.100mol·L-1 K2Cr2O7还原至一半时的电势? 解: E V E V Cr O Cr 1.01 0.100 0.0500 lg 6 0.059 1.00 1.00 2 0 / 2 3 2 7 = + = = 查表得: + + 返回

三、外界条件对条件电极电位的影响 1.离子强度的影响 2.副反应的影响 3.酸度的影响 上一页下一页 返回退出
上一页 下一页 返回 退出 三、外界条件对条件电极电位的影响 1. 离子强度的影响 2. 副反应的影响 3. 酸度的影响 返回
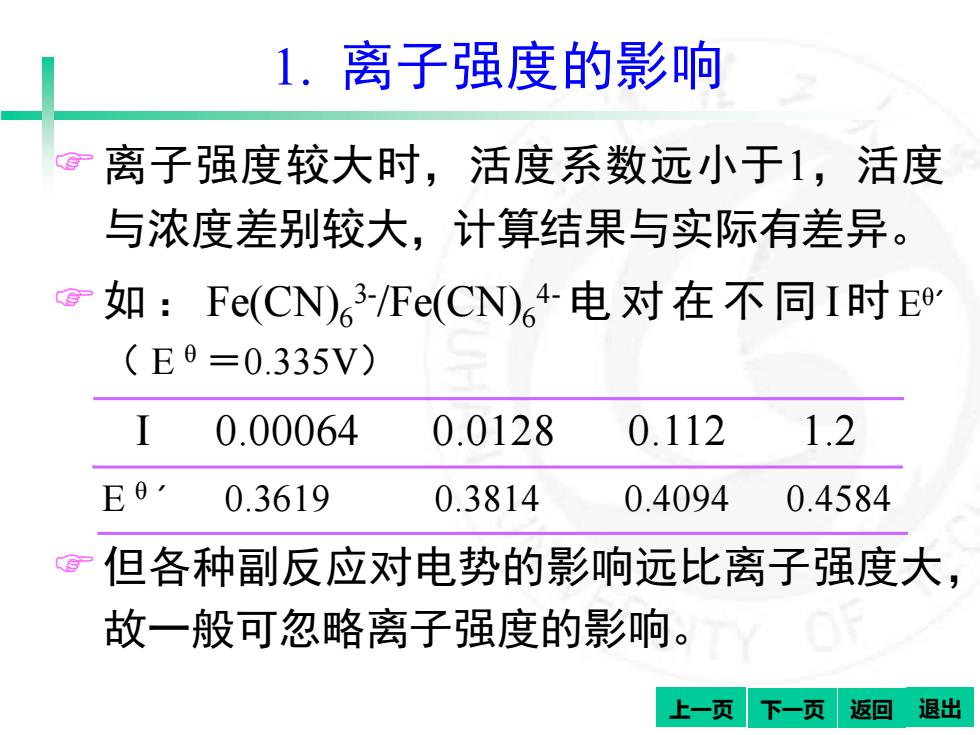
1.离子强度的影响 离子强度较大时,活度系数远小于1,活度 与浓度差别较大,计算结果与实际有差异。 o如:Fe(CN)63-/Re(CN)64-电对在不同I时E (E0=0.335V) 0.00064 0.0128 0.112 1.2 E 0.3619 0.3814 0.4094 0.4584 但各种副反应对电势的影响远比离子强度大, 故一般可忽略离子强度的影响。 上一页 下一页返回退出
上一页 下一页 返回 退出 1. 离子强度的影响 离子强度较大时,活度系数远小于1,活度 与浓度差别较大,计算结果与实际有差异。 如: Fe(CN)6 3- /Fe(CN)6 4-电 对在不同 I时 Eθ´ ( E θ =0.335V) I 0.00064 0.0128 0.112 1.2 E θ ´ 0.3619 0.3814 0.4094 0.4584 但各种副反应对电势的影响远比离子强度大, 故一般可忽略离子强度的影响。 返回

2.副反应的影响 沉淀反应或络合反应使电对的氧化形或 还原形浓度发生变化,改变电极电势。 口如碘量法测定Cu2+: 2Cu2++4=2CuV+2 (E0c2+cut+=0.16V, E°20.53V) Cu沉淀的生成,使Cu2+可氧化碘化物。 上一页 下一页返回 退出
上一页 下一页 返回 退出 2. 副反应的影响 沉淀反应或络合反应使电对的氧化形或 还原形浓度发生变化,改变电极电势。 ♫如碘量法测定Cu2+: 2Cu2+ + 4I - = 2CuI + I2 (E θ Cu2+ /Cu+=0.16V, E θ I 2 /I=0.53V) CuI沉淀的生成,使Cu2+可氧化碘化物。 返回