
反应等温方程 反应A.G9 市四律 经验平衡常数 化学平合 平衡常数测定 温度对Ke影响 其它因素的影响 平衡组成计算 习题课
习题课 平衡组成计算 其它因素的影响 温度对K影响 平衡常数测定 经验平衡常数 反应rGm 反应等温方程

动画 偏摩尔量和化学势 热力学系统大多是单组分系统,或是组成不变的系 统,只需用两个变量就可以描述系统的状态。 多组分系统:两种或两种以上物质所形成的系统称 为多组分系统。 对于多组分均相体系,描述它的状态,除两个基本 的状态性质(T和p)外,还需要体系中各物质的量或 浓度。 体系的某些热力学性质并不等于各物质在纯态时该 热力学量的简单加和。 山庆东理工大学 陀合l等温方程△,GeK,K K⊙测定温度影响 其他因素计算示例习题课
等温方程 rGm Kp Kx K测定 温度影响 其他因素 计算示例 习题课 动画 山东理工大学 热力学系统大多是单组分系统,或是组成不变的系 统,只需用两个变量就可以描述系统的状态。 多组分系统:两种或两种以上物质所形成的系统称 为多组分系统。 对于多组分均相体系,描述它的状态,除两个基本 的状态性质(T和p)外,还需要体系中各物质的量或 浓度。 体系的某些热力学性质并不等于各物质在纯态时该 热力学量的简单加和。 偏摩尔量和化学势

动画 多组分系统与单组分系统的差别 单组分系统的广度性质具有加和性 若1mol单组分B物质的体积为 m.B 则2mol单组分B物质的体积为 2× m.B 而1mol单组分B物质和1mol单组分C物质混合, 得到的混合体积可能有两种情况: ()V=1mol×B+1mol×Wmc 形成了混合物 (2)'≠1mol×+1mol×c 形成了溶液 山庆理工大学 合>等温方程△,GK,KKe测定温度影响其他因素计算示例习题课
等温方程 rGm Kp Kx K测定 温度影响 其他因素 计算示例 习题课 动画 山东理工大学 单组分系统的广度性质具有加和性 * 若1 mol单组分B物质的体积为 Vm,B * 则2 mol单组分B物质的体积为 2 Vm,B 而1 mol单组分B物质和1 mol单组分C物质混合, 得到的混合体积可能有两种情况: * * m,B m,C (1) 1 mol 1 mol V V V = + * * m,B m,C (2) 1 mol 1 mol V + V V 形成了混合物 形成了溶液 多组分系统与单组分系统的差别
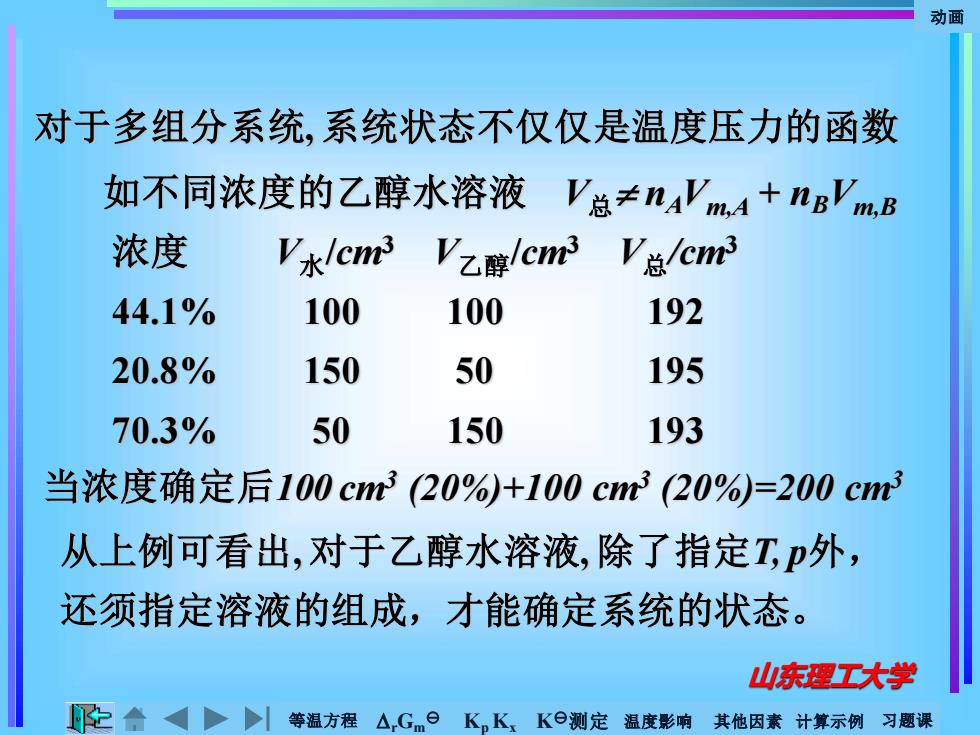
动画 对于多组分系统,系统状态不仅仅是温度压力的函数 如不同浓度的乙醇水溶液 V总≠na'mA+nB'VmB 浓度 V水lcr3Vz醇/cm3V点/cr3 44.1% 100 100 192 20.8% 150 50 195 70.3% 50 150 193 当浓度确定后100cm3(20%)+100cm3(20%=200ct3 从上例可看出,对于乙醇水溶液,除了指定T,p外, 还须指定溶液的组成,才能确定系统的状态。 山庆理工大学 等温方程△,G.日 K,K,Ke测定 温度影响 其他因素计算示例习题课
等温方程 rGm Kp Kx K测定 温度影响 其他因素 计算示例 习题课 动画 山东理工大学 对于多组分系统, 系统状态不仅仅是温度压力的函数 如不同浓度的乙醇水溶液 浓度 V水/cm3 V乙醇/cm3 V总/cm3 44.1% 100 100 192 20.8% 150 50 195 70.3% 50 150 193 从上例可看出, 对于乙醇水溶液, 除了指定T, p外, 还须指定溶液的组成,才能确定系统的状态。 V总 nAVm,A + nBVm,B 当浓度确定后100 cm3 (20%)+100 cm3 (20%)=200 cm3

动画 偏摩尔量的定义 在多组分系统中,每个热力学函数的变量就 不止两个,还与组成系统各物的物质的量有关 设系统中有1,2,3,.,k个组分 系统中任一容量性质Z(代表V,U,H,S, A,G等)除了与温度、压力有关外,还与各 组分的数量有关,即 Z=Z(T,p,n,n2,nk) 如果温度、压力和组成有微小的变化,则 系统中任一容量性质Z的变化为: 山东理工大学 合等温方程△,GK,KKe测定温度影响其他因素计算示例习题课
等温方程 rGm Kp Kx K测定 温度影响 其他因素 计算示例 习题课 动画 山东理工大学 偏摩尔量的定义 在多组分系统中,每个热力学函数的变量就 不止两个,还与组成系统各物的物质的量有关 1 2 k Z Z T p n n n = ( , , , , , ) 系统中任一容量性质Z(代表V,U,H,S, A,G等)除了与温度、压力有关外,还与各 组分的数量有关,即 设系统中有 1,2,3, ,k 个组分 如果温度、压力和组成有微小的变化,则 系统中任一容量性质Z的变化为: