
碱金属 碱土金属 单质及化合物 离子晶体盐类的溶解性 钠等元素与人体的关系 本章要求
碱金属 碱土金属 通 性 单 质 及 化 合 物 作 业 本 章 要 求 离 子 晶 体 盐 类 的 溶 解 性 钠 等 元 素 与 人 体 的 关 系

概述 碱金属和碱土金属是 A族包括锂、钠、钾、铷、 们的氧化物溶于水呈强碱性 ⅡA族包括铍、镁、钙 素。由于钙、锶、钡的氧A 和“土性”(以前把粘土的 之间,所以称为碱土金属, 在内。钫和镭是放射性元素 地壳内蕴藏较丰富,它们 1807年,戴维电解K0H 同样的方法从NaOH中得到 戴维,H
碱金属和碱土金属是周期表IA族和IIA族元素。 IA族包括锂、钠、钾、铷、铯、钫六种金属元素。它 们的氧化物溶于水呈强碱性,所以称为碱金属。 IIA族包括铍、镁、钙、锶、钡、镭六种金属元 素。由于钙、锶、钡的氧化物在性质上介于“碱性” 和“土性”(以前把粘土的主要成分Al2O3称为“土”) 之间,所以称为碱土金属,现习惯上把铍和镁也包括 在内。钫和镭是放射性元素。钠、钾、钙、镁和钡在 地壳内蕴藏较丰富,它们的单质和化合物用途较广泛。 1807年,戴维电解KOH得到金属K(Potassium),用 同样的方法从NaOH中得到金属Na(Sodium)。 概述

概述 1808年, 按3:1的比例 混合,放在白 汞齐,并制得 了钙。不久他 重晶石(BaSO4) 和苦土MgO) 素单质一锶、 钡(Barium)和 钫Franc B衰变并放出 粒子后得到的 铍(Beryl 多艺的化学家 维勒用他电解 维勒,F
1808年,戴维把潮湿的石灰和氧化汞按3:1的比例 混合,放在白金皿中进行电解得到了钙汞齐,并制得 了钙。不久他又从菱锶矿石(SrCO3 )、重晶石(BaSO4 ) 和苦土(MgO)中到得了三个新的金属元素单质——锶、 钡(Barium)和镁。 钫(Francium)是由法国的佩里从锕衰变并放出 粒子后得到的。 铍(Beryllium)是1845年德国的多才多艺的化学家 维勒用他电解发现铝的方法制得的。 概述

概述 碱金属的基本性质 元素 Li Na K Rb Cs 性质 原子半径pm 152 153.7 227.2 247.5 265.4 离子半径pm 68 97 133 147 167 第一电离势 kJ/ 521 499 421 405 371 第二电离势 mol 7295 4591 3088 2675 2436 电负性 0.98 0.93 0.82 0.82 0.79 标准电极电势(酸) -3.045 -2.711 -2.923 -2.925 -2.923 M(g)水合热 519 406 322 293 264 /kJ.mol-1
概述 元素 性质 Li Na K Rb Cs 原子半径/pm 152 153.7 227.2 247.5 265.4 离子半径/pm 68 97 133 147 167 第一电离势 kJ/ mol 521 499 421 405 371 第二电离势 7295 4591 3088 2675 2436 电负性 0.98 0.93 0.82 0.82 0.79 标准电极电势(酸) -3.045 -2.711 -2.923 -2.925 -2.923 M+ (g)水合热 /kJ·mol-1 519 406 322 293 264 碱金属的基本性质
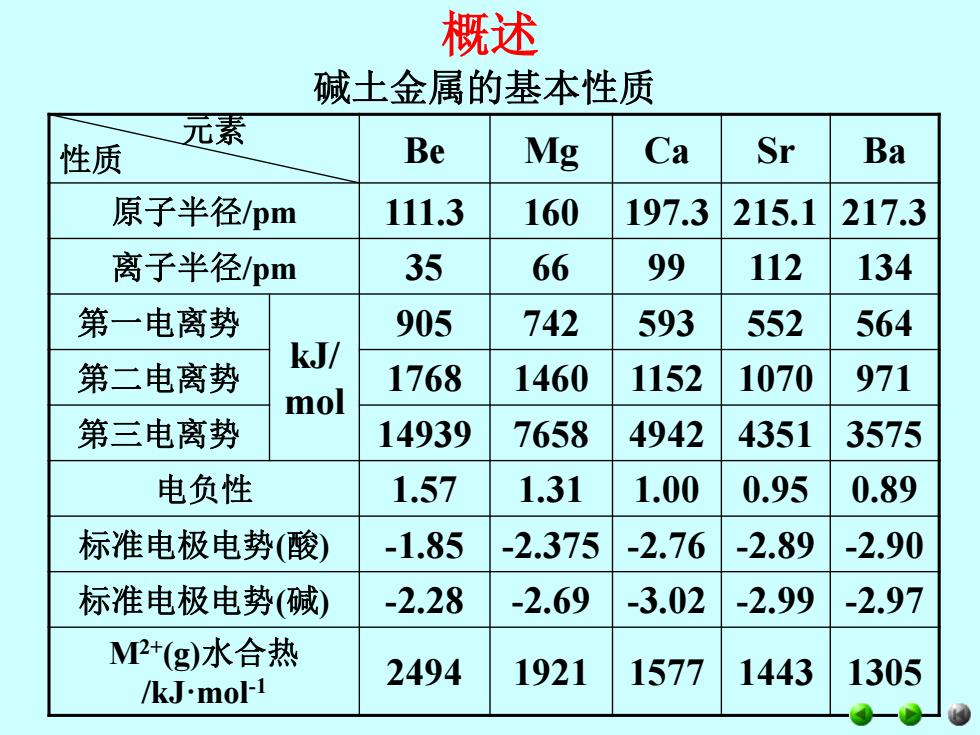
概述 碱土金属的基本性质 元素 性质 Be Mg Ca Sr Ba 原子半径pm 111.3 160 197.3 215.1 217.3 离子半径pm 35 66 99 112 134 第一电离势 905 742 593 552 564 第二电离势 kJ/ 1768 1460 1152 1070 971 mol 第三电离势 14939 7658 4942 4351 3575 电负性 1.57 1.31 1.00 0.95 0.89 标准电极电势(酸) -1.85 -2.375 -2.76 -2.89 -2.90 标准电极电势(碱) -2.28 -2.69 -3.02 -2.99 -2.97 MP+(g)水合热 2494 1921 1577 1443 1305 /kJ.mol-1
概述 元素 性质 Be Mg Ca Sr Ba 原子半径/pm 111.3 160 197.3 215.1 217.3 离子半径/pm 35 66 99 112 134 第一电离势 kJ/ mol 905 742 593 552 564 第二电离势 1768 1460 1152 1070 971 第三电离势 14939 7658 4942 4351 3575 电负性 1.57 1.31 1.00 0.95 0.89 标准电极电势(酸) -1.85 -2.375 -2.76 -2.89 -2.90 标准电极电势(碱) -2.28 -2.69 -3.02 -2.99 -2.97 M2+(g)水合热 /kJ·mol-1 2494 1921 1577 1443 1305 碱土金属的基本性质