10.3.2硼酸盐、硼酸和硼的氢化物 (1)硼酸盐:全世界硼酸钠盐的年耗量约占总硼消耗量的80%.其中 一半以上用于玻璃、陶瓷和搪瓷工业,其他应用领域包 括洗涤剂组分(过硼酸盐)、微量元素肥料、加入防冻剂 中做抗腐蚀剂、金属的焊剂和纤维素材质的阻燃剂. 硼砂:Na,B,O210H,O,实际上结构为Na2B,Os(OH48HO 2、 OH ●结构 B-OH HO
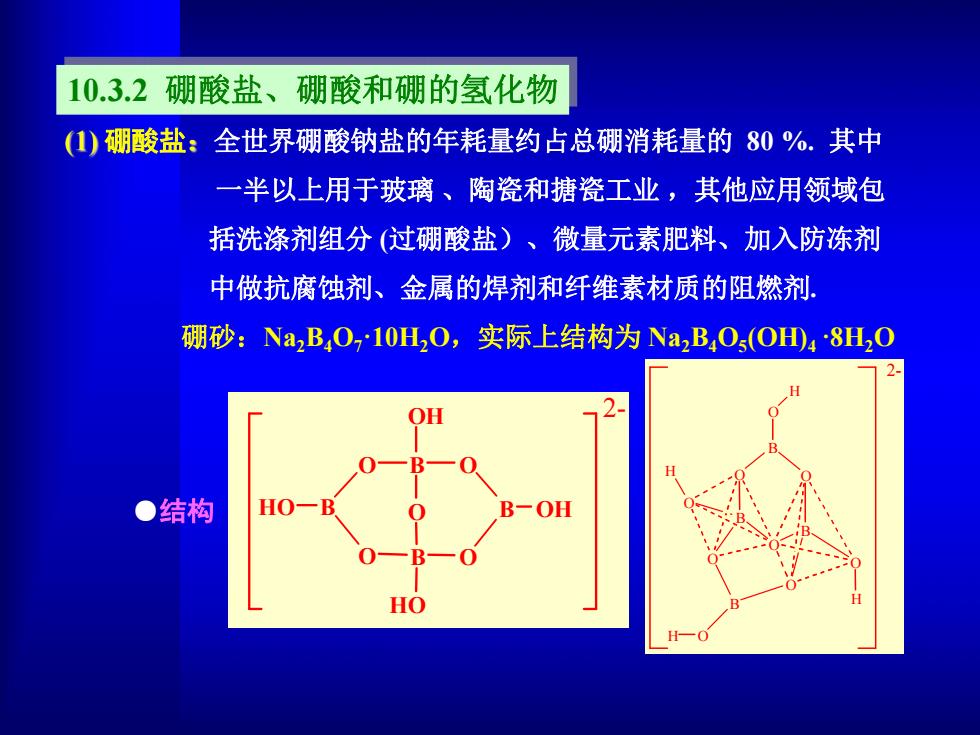
10.3.2 硼酸盐、硼酸和硼的氢化物 硼酸盐 全世界硼酸钠盐的年耗量约占总硼消耗量的 80 %. 其中 一半以上用于玻璃 、陶瓷和搪瓷工业 ,其他应用领域包 括洗涤剂组分 (过硼酸盐)、微量元素肥料、加入防冻剂 中做抗腐蚀剂、金属的焊剂和纤维素材质的阻燃剂. 硼砂:Na2B4O7·10H2O,实际上结构为 Na2B4O5(OH)4 ·8H2O ●结构 B O H O O B O H O B H O B O O O H 2- B O O B O O O OH HO HO B B OH 2-

●性质:①易溶于水,水解呈碱性 [BOs(OH4l2-+5H20=4HB03+2OH=2H3B03+2B(OH3 构成缓冲溶液pH=9.24(20℃) ②与酸反应制HBO3 Na2BO7+H2SO+5H2O4 H3BO3+Na2SO ③脱水 风化脱水→Na2B,O,体积膨胀 受热脱水→硼砂玻璃 Na2B3O7+CoO-Co(BO2)3 2NaBO2 (蓝色 NazB,O,+NiO→Ni(BO2)3·2NaBO2(棕色) ●制备:工业上通过酸法或碱法将钙和镁的硼酸盐转化, ●用途:在实验室用做标定标准酸溶液的基准物: Na2B,0,10H20+2HC1=4H3B03+2NaCl+5H2O
● 性质: ① 易溶于水,水解呈碱性 ② 与酸反应制 H3BO3 Na2B4O7 + H2SO4 + 5H2O → 4 H3BO3 + Na2SO4 ③ 脱水 风化脱水 → Na2B4O7体积膨胀 受热脱水 → 硼砂玻璃 Na2B4O7 + CoO → Co(BO2)3 · 2NaBO2 (蓝色) Na2B4O7 + NiO → Ni(BO2)3 · 2NaBO2 (棕色) ● 制备:工业上通过酸法或碱法将钙和镁的硼酸盐转化. ● 用途:在实验室用做标定标准酸溶液的基准物: Na2B4O7 · 10H2O + 2 HCl == 4 H3BO3 + 2 NaCl + 5 H2O [B4O5(OH)4] 2- + 5 H2O 4 H3BO3 + 2 OH- 2 H3BO3 + 2 B(OH)3 构成缓冲溶液 pH = 9.24 (20℃)

(2)硼酸少见的固体酸.不像分子式B(O田3所暗示的那样,HBO3在 水中是一元酸.其质子转移平衡与原子的缺电子性质密切相关: B(O田3(aq+2H0①=HO(aq+[B(OH4(aq)pK9=9.2 pK。值表明H3BO的酸性极弱,不能直接用NaOH滴定.多基 化合物(如甘露醇、甘油等)与HBO3反应生成稳定的配合物并使 显示强酸性,从而使滴定法可用于测定硼含量: OH HO-CH2 HO+HO CH- C(OH)H H3O++H2O OH HO-CH, 浓H2SO4存在下HBO3与甲醇或乙醇反应生成挥发性硼酸酯硼 酸酯燃烧时发出的绿色火焰用来鉴定硼酸根的存在, 3 C,HOH+H3BO3=B(OC2Hs)3+3 H2O
值表明 H3BO3的酸性极弱,不能直接用 NaOH 滴定. 多基 化合物(如甘露醇、甘油等)与 H3BO3反应生成稳定的配合物并使 显示强酸性,从而使滴定法可用于测定硼含量: θ pKa 硼酸 少见的固体酸. 不像分子式 B(OH)3所暗示的那样,H3BO3在 水中是一元酸. 其质子转移平衡与B原子的缺电子性质密切相关: p 9.2 θ B(OH)3(aq) + 2 H2O(l) H3O Ka +(aq) + [B(OH)4]-(aq) 浓 H2SO4存在下 H3BO3与甲醇或乙醇反应生成挥发性硼酸酯硼 酸酯燃烧时发出的绿色火焰用来鉴定硼酸根的存在. 3 C2H5OH + H3BO3 B(OC2H5)3 + 3 H2O OH HO—CH2 O—CH2 HO—B + HO—CH O B C(OH)H + H3O+ + H2O OH HO—CH2 O—CH2

HBO3在冷水中溶解度很小,在热水中却是易溶的.这意味着: 一是可通过水溶液中重结晶的方法提纯;二是说明它含有氢键, 硼酸晶体的片层结构
H3BO3在冷水中溶解度很小,在热水中却是易溶的. 这意味着: 一是可通过水溶液中重结晶的方法提纯;二是说明它含有氢键. 硼酸晶体的片层结构

Ques 1、H3BO3为什么是一元酸? 2、HBO3为什么在冷水中溶解度小,在热水中却是易 溶的?
1、H3BO3为什么是一元酸? 2、H3BO3为什么在冷水中溶解度小,在热水中却是易 溶的? Question 3