
例2:配平 (g)+NaOH(aq)-A>NaCl(aq)+NaCIO;(aq) C12+2e=2C1 ① Cl2+120H=2C103+6H0+10e ② ①×5+②得: 6C1,+120H=10C1+2C103+6H,0 化简得: 3C12+60H=5C1+C103+3H2O 3C1,+6NaOH=5NaCl+NaClO+3H,O
例 2 :配平 Cl (g) NaOH(aq) NaCl(aq) NaClO (aq) 3 Δ 2 + ⎯→ + ① ×5+ ②得: ①② 3Cl 2 + 6NaOH = 5NaCl + NaClO 3 + 3H 2 O 3Cl 2 + 6OH = 5Cl + ClO 3 + 3H 2 O − − − 6Cl 2 +12OH = 10Cl + 2ClO 3 + 6H 2 O − − − Cl 12OH 2ClO 6H O 10e 2 + = 3 + 2 + − − − Cl + 2e = 2Cl 解: 2 化简得:

例:配平方程式 As2S3(s)+HNO3 (aq)>H;AsO(aq)+H2SOa(aq)+NO(g) 解:As2S3+NO3→H3AsO4+SO+NO ① NO+4H*+3e=NO+2H,O As2S3+20H2O=2H;AsO,+3SO;+34H*+28e ② ①×28+②×3得 28NO3+3As2S3+4H2O+10H =6H3As04+9SO2+28NO 3As,S3+28HNO 3+4H,O =6H3AsO4+9H,S04+28NO
As S (s) HNO (aq) H AsO (aq) H SO (aq) NO(g) 2 3 + 3 → 3 4 + 2 4 + ①×28+②×3得 ② ① 例:配平方程式 6H AsO 9H SO 28NO 3As S 28HNO 4H O 3 4 2 4 2 3 3 2 = + + + + 6H AsO 9SO 28NO 28NO 3As S 4H O 10H 2 3 4 4 3 2 3 2 = + + + + + − − + − + − As S + 20H O = 2H AsO + 3SO + 34H + 28e 2 2 3 2 3 4 4 NO3 + 4H + 3e = NO + 2H2 O − + − As S N O H AsO SO N O 2 2 3 + 3 → 3 4 + 4 + 解: − −

例4:配平方程式 Cr(OH):(s)+Br2(1)+KOHK2CrO+KBr 解:Cr(OH(S)+B,()→CrO}+Br Br,(1)+2e=2Br ① Cr(OH):(s)+50H CrO2 +4H2O+3e ①×3+②×2得: 2Cr(OH)(s)+3Br(1)+100H =2CrO+6Br +8H,O 2Cr(OH):(s)+3Br (1)+10KOH =2K,CrO+6KBr+8H,O
解: = 2K2CrO4 + 6KBr+8H2O 2CrO 6Br 8H2O 2 4 = + + − − ①×3+②×2得: KOH K CrO KBr 2 4 Cr(OH) (s) Br (l)+ + 3 2 + CrO Br 2 4 + − − Br (l) 2 Cr(OH) (s) 3 + + 2e = 2Br ① − − Br (l) 2 5OH CrO2 4 + = +4H2O+3e − − Cr(OH) (s) 3 +10OH− Cr(OH) (s) 2 3 Br (l) +3 2 2Cr(OH)3 (s) +3Br2 (l) +10KOH 例4:配平方程式

小结: 酸性介质: 多n个O+2n个H+,另一边+n个H,0 碱性介质: 多n个O+n个H,0,另一边+2n个OH
酸性介质: 多n个O+2n个H+,另一边 +n个H2O 碱性介质: 多n个O+n个H2O,另一边 +2n个OH- 小结:
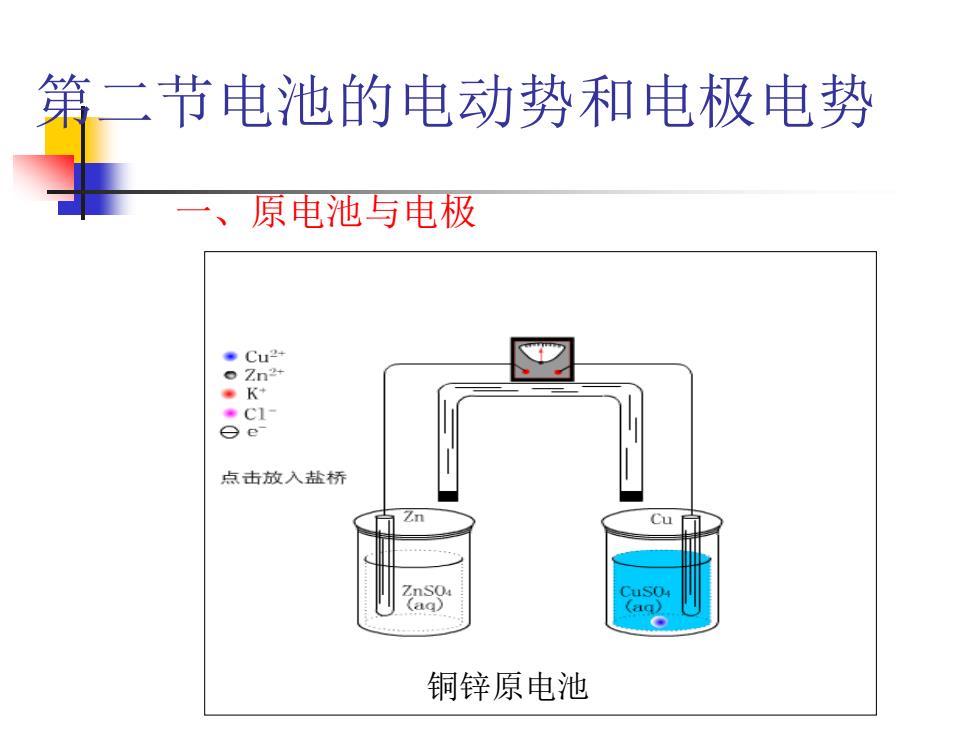
第二节电池的电动势和电极电势 一、 原电池与电极 。Cu24 。Zn24 K' C1- ee 点击放入盐桥 Cu aq (aa) 铜锌原电池
第二节电池的电动势和电极电势 一、原电池与电极 铜锌原电池