
第9章 沉淀-溶解平衡 和沉淀滴定 Chapter 9 Precipitation -dissolution equilibrium and precipitation titration
沉淀-溶解平衡 和沉淀滴定 第9 章

本章教学要求 1.了解沉淀的溶解度和溶度积常数。 2.掌握微溶化合物溶解度的计算。 3.熟悉影响条件溶度积和沉淀溶解度的因素。 4.熟悉几种重要的银量法的原理、特点和应用。 上页 下页 目录 返回
本章教学要求 1. 了解沉淀的溶解度和溶度积常数 。 2. 掌握微溶化合物溶解度的计算。 3. 熟悉影响条件溶度积和沉淀溶解度的因素。 4. 熟悉几种重要的银量法的原理、特点和应用

本章内容 9.1 沉淀-溶解平衡 Precipitation-dissolution equilibrium 9.2 沉淀滴定法 Precipitation titration 上页 下页 目录返回
9.1 沉淀-溶解平衡 Precipitation – dissolution equilibrium 9.2 沉淀滴定法 Precipitation titration

9.1沉淀一溶解平 Precipitation-dissolution equilibrium 9.1.1 溶度积常数和溶解度 Solubility- product constant and solubility 9.1.2 离子积:沉淀形成与沉淀溶解的 判据Ion product:a criterion of formation of deposit and dissolution of deposit 9.1.3 沉淀一溶解平衡的移动 Shift of precipitation dissolution equilibrium 上页 下页 目录 返回
9.1.1 溶度积常数和溶解度 Solubility- product constant and solubility 9.1.2 离子积: 沉淀形成与沉淀溶解的 判据 Ion product: a criterion of formation of deposit and dissolution of deposit 9.1.3 沉淀-溶解平衡的移动 Shift of precipitation - dissolution equilibrium 9.1 沉淀-溶解平衡 Precipitation – dissolution equilibrium
9.1.1溶度积常数和溶解度 1.溶解度 物质的溶解度(solubility)是指在一定温度和压力下,固 液达到平衡状态时,饱和溶液里的物质浓度。常表示为 160 gdm3或mol/dm3。 1 140 CaC1·2H,0 H H 120 OH 110 H 100 KNO KBr H 90 6H0 70 NH.CI- 50 KCI 30 Nas90.-10H.OS KCIO K2SO Cez(S0ah·9H0 10 20 30 4050 60 708090100 上页 下页 目录返回
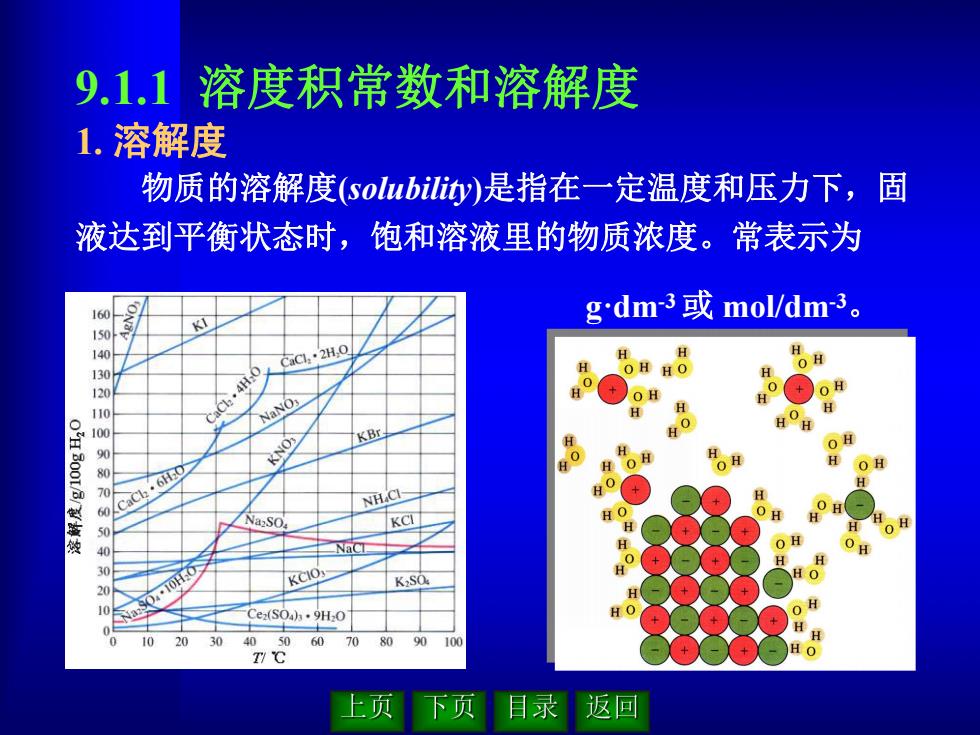
9.1.1 溶度积常数和溶解度 1. 溶解度 物质的溶解度(solubility)是指在一定温度和压力下,固 液达到平衡状态时,饱和溶液里的物质浓度。常表示为 g·dm-3或 mol/dm-3