
5.状态方程(equationofstate)系统状态函数之间的定量关系式称为状态方程对于一定量的单组分均匀系统,状态函数p,V,T之间有一定量的联系。经验证明,只有两个是独立的它们的函数关系可表示为:V = f(T,P)T = f(p,V)p= f(T,V)是与系统性质有关的函数例如,理想气体的状态方程可表示为:pV = nRT对于多组分系统,系统的状态还与组成有关,如:T= f(p, V, n, nz..)
系统状态函数之间的定量关系式称为状态方程 对于一定量的单组分均匀系统,状态函数 p, V,T 之间有一定量的联系。经验证明,只有两个是独立的, 它们的函数关系可表示为: 例如,理想气体的状态方程可表示为: 5.状态方程(equation of state) T f p V = ( , ) p f T V = ( , ) V f T p = ( , ) 对于多组分系统,系统的状态还与组成有关,如: pV nRT = 1 2, T f p V n n = ( , , , ) 是与系统性质有关的函数
6.过程和途径简单状态变化过程相变化过程(1)过程(process)化学变化过程在一定的环境条件下,系统发生了一个从始态到终态的变化,称为系统发生了一个热力学过程(path)(2)途径从始态到终态的具体步骤称为途径
(1)过程 从始态到终态的具体步骤称为途径。 在一定的环境条件下,系统发生了一个从始态 到终态的变化,称为系统发生了一个热力学过程 (process) (2)途径 (path) 6. 过程和途径 •简单状态变化过程 •相变化过程 •化学变化过程
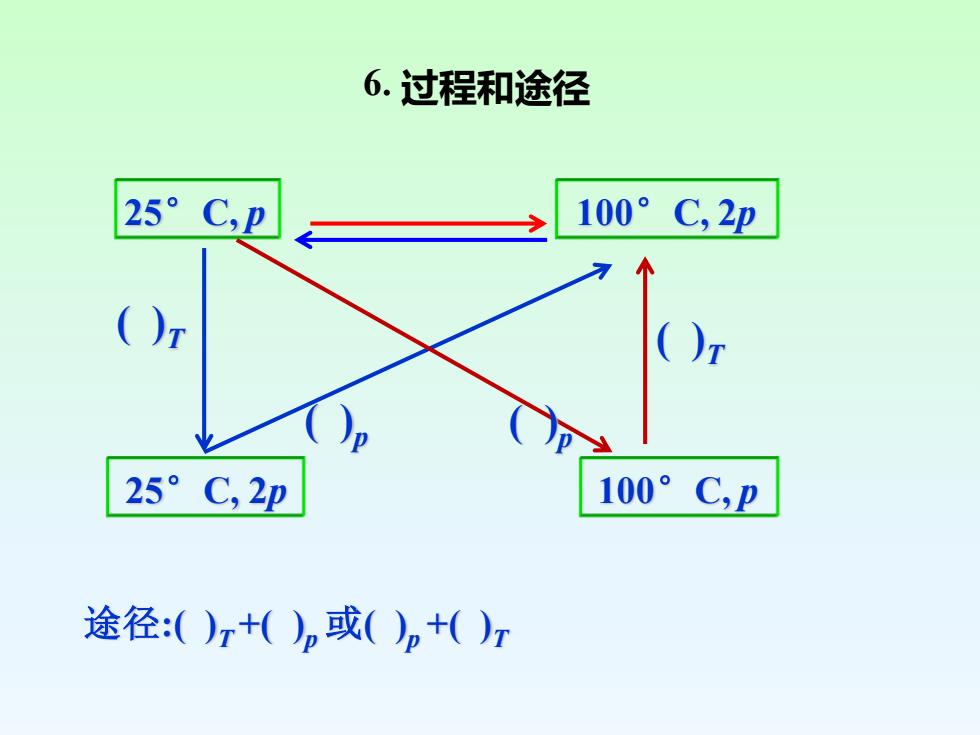
6.过程和途径25°100°C,pC,2p()r()T25°100°C, 2pC,p途径:()μ+(),或(),+()
25°C, p 100°C, 2p 25°C, 2p 100°C, p ( )T ( )T ( )p ( )p 途径:( )T +( )p 或( )p +( )T 6. 过程和途径

常见的变化过程有:T, = T, = T环=常数(1)等温过程P= P2= P环=常数(2)等压过程dV=0(3)等容过程Q=0(4)绝热过程(5)环状过程fdU=0(循环过程)UU指热力学能,是状态函数
(1)等温过程 (2)等压过程 (3)等容过程 (4)绝热过程 (5)环状过程 (循环过程) T T T 1 2 = = 环 =常数 p p p 1 2 = = 环 =常数 d 0 V = Q = 0 d 0 U = 常见的变化过程有: U指热力学能,是状态函数

7.热和功(1)热(heat )系统与环境之间因温差而传递的能量称为热,用符号Q表示。Q的取号:系统放热,Q<0系统吸热,Q>0热的本质是分子无规则运动强度的一种体现计算热一定要与系统与环境之间发生热交换的过程联系在一起,系统内部的能量交换不可能是热
系统吸热,Q>0 系统放热,Q<0 (1)热(heat) 系统与环境之间因温差而传递的能量称为热,用 符号Q 表示。 7. 热和功 Q的取号: 热的本质是分子无规则运动强度的一种体现 计算热一定要与系统与环境之间发生热交换的过程 联系在一起,系统内部的能量交换不可能是热