
2.02化学性质 氧化性(主要),配位性(生物体中重要) (1)氧化性 00(02/H20)=1.23V,p0(02/0H)=0.40V Fe Fe3O4,FeO,Fe2O3 S S02(g) HS S或S02(g) 02+NH3 → H20+N2或NO HI 12 CHa C02、C0或C
(1) 氧化性 φØ (O2 /H2O) = 1.23 V, φØ (O2 /OH- ) = 0.40 V Fe Fe3O4 ,FeO, Fe2O3 S SO2 (g) H2S S 或 SO2 (g) O2 + NH3 → H2O + N2或 NO HI I2 CH4 CO2、CO 或 C 2. O2化学性质 氧化性(主要),配位性(生物体中重要)

(2)配位性质 人血红蛋白中的血红素Hb是卟啉衍生物与Fe(四 形成的配合物,具有与0,络合的功能: 肺 HbFe四+O2二HbFe四←-02(氧合血红蛋白) 人体各组织
人血红蛋白中的血红素Hb是卟啉衍生物与Fe(II) 形成的配合物,具有与O2络合的功能: 肺 HbFe(II) + O2 HbFe(II) ←O2 (氧合血红蛋白) 人体各组织 (2) 配位性质

单线态与三线态02 02:(o1s)2(o1s)2(2)P(2s)2(2)P(2p)2(2)2(2p)'(m2) 激发:个 单线态102 154.8kJ.mol 创 92.0kJ.mol 基态:个↑ 三线态 (S=2s+1) 光敏化剂(基态)加 光敏化剂(激发态) 光敏化剂激)+302 能量传递光敏化剂(基)+102
单线态与三线态O2 激发:↑ ↓ ↑↓ 单线态 1O2 光敏化剂(基态) hν 光敏化剂 (激发态) 基态: ↑ ↑ 三线态 (S=2s+1) 154.8kJ.mol 92.0kJ.mol 光敏化剂(激)+ 3O2 能量传递 光敏化剂(基) + 1O2 O2 : (σ1s) 2 (σ1s * ) 2 (σ2s) 2 (σ2s * ) 2 (σ2px ) 2 (π2py ) 2 (π2pz ) 2 (π* 2py ) 1 (π* 2pz ) 1

2-4 臭氧 有鱼腥味的淡蓝色气体。 (1)03的分子结构 1.278A 1.278A 03分子电偶极矩0,→3个0原 子不在同一直线上; 键角∠000=116.8°,→中心0 原子sp杂化。 116.8° 127.8pmO 臭氧中,0-0键长为127.8pm,大于0=0,小于0-0键长
(1) O3的分子结构 O3 分子电偶极矩μ≠0, → 3个O原 子不在同一直线上; 键角∠OOO = 116.8 º ,→ 中心O 原子sp2杂化。 臭氧中,O-O键长为127.8 pm,大于O=O,小于O-O键长。 2-4 臭氧 有鱼腥味的淡蓝色气体
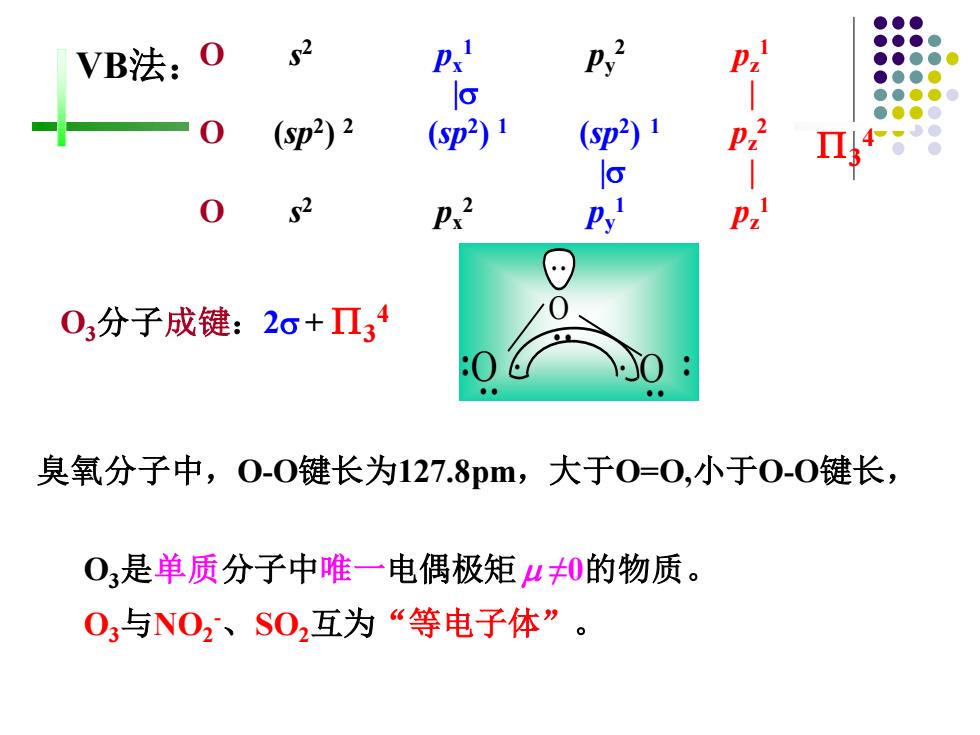
VB法:O s2 2 6 (p2)2 2)1 (sp2) s2 03分子成键:2o+Π34 臭氧分子中,0-0键长为127.8pm,大于0=0,小于0-0键长, 03是单质分子中唯一电偶极矩40的物质。 03与N02、S02互为“等电子体
VB法:O s 2 px 1 py 2 pz 1 | | O (sp2 ) 2 (sp2 ) 1 (sp2 ) 1 pz 2 | | O s 2 px 2 py 1 pz 1 O3是单质分子中唯一电偶极矩 ≠0的物质。 O3与NO2 -、SO2互为“等电子体”。 臭氧分子中,O-O键长为127.8pm,大于O=O,小于O-O键长, O3分子成键:2 + 3 4 : : . . O : O: : O . . 3 4