
生 第7章晶体结构 7.1分子晶体和分子间作用力 7.2离子晶体和离子键 7.3离子极化
第7章 晶体结构 7.1 分子晶体和分子间作用力 7.2 离子晶体和离子键 7.3 离子极化

化学键:如果两个原子(或原子团)之间的作用力 强得足以形成稳定的、可被化学家看做独立物种的 聚集体,它们之间就存在化学键。简单地说,化学 键是指分子内部原子之间的强相互作用。 化学键形成的标志:当聚集体的能量低于原来原子 或离子的能量大约40kJmo1以上时,就认为形成了 化学键。 化学键的基本类型:离子键、共价键、金属键
化学键:如果两个原子(或原子团)之间的作用力 强得足以形成稳定的、可被化学家看做独立物种的 聚集体,它们之间就存在化学键。简单地说,化学 键是指分子内部原子之间的强相互作用。 化学键形成的标志:当聚集体的能量低于原来原子 或离子的能量大约40kJmol-1以上时,就认为形成了 化学键。 化学键的基本类型:离子键、共价键、金属键
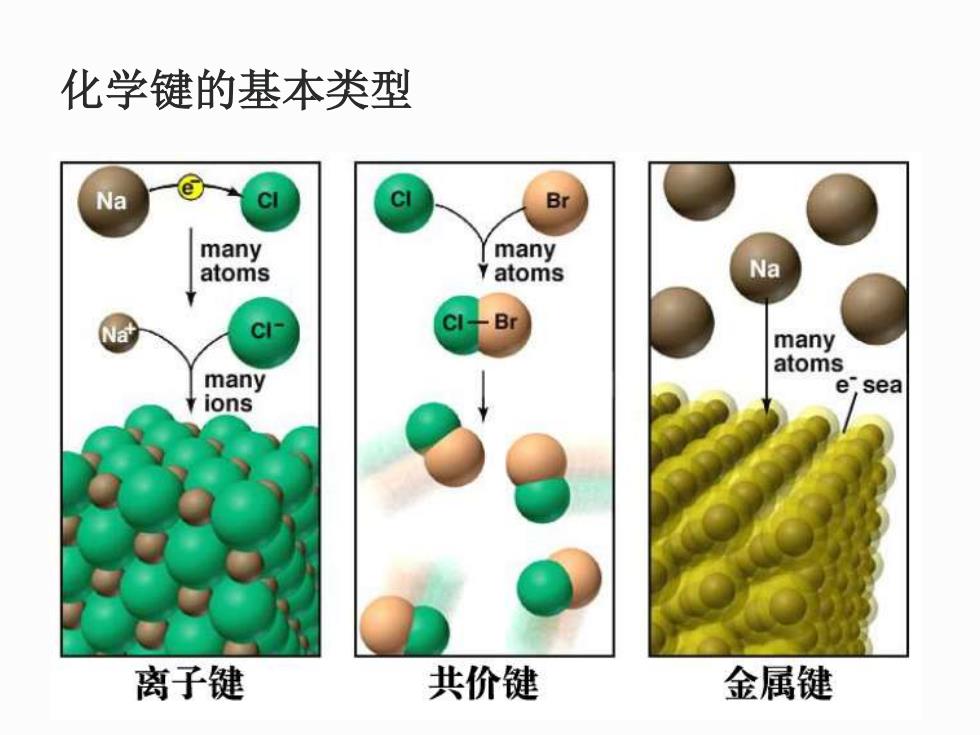
化学键的基本类型 Na Br many many atoms Y atoms Na CI- B many atoms many e sea ions 离子键 共价键 金属键
化学键的基本类型

7.1分子晶体和分子间作用力 分子之间以分子间作用力结合成的晶体称为分 子晶体。 分子间作用力是一种弱相互作用,远小于化学 键的结合强度。 因此,分子晶体一般来说要在较低的温度下才 能形成,而在常温时这些物质多以气体形式存在。 分子晶体导电性能一般较差,因为电子从一个 分子传导到另一个分子很不容易
7.1 分子晶体和分子间作用力 分子之间以分子间作用力结合成的晶体称为分 子晶体。 分子间作用力是一种弱相互作用,远小于化学 键的结合强度。 因此,分子晶体一般来说要在较低的温度下才 能形成,而在常温时这些物质多以气体形式存在。 分子晶体导电性能一般较差,因为电子从一个 分子传导到另一个分子很不容易

7.1.1键的极性与分子的极性 一、键的极性 假设一个共价键的正负电荷可以集中在一个 点上时,形成相应的“正(负)电荷重心”。此正 (负)电荷重心为电偶极子的两极。 偶极矩μ=偶极子电量q×偶极子两极的距离1 1.偶极矩为矢量,方向从正电中心指向负电中心。 2.单位为德拜,数量级常在1030℃·m
7.1.1 键的极性与分子的极性 一、键的极性 假设一个共价键的正负电荷可以集中在一个 点上时,形成相应的“正(负)电荷重心” 。此正 (负)电荷重心为电偶极子的两极。 偶极矩μ = 偶极子电量 q×偶极子两极的距离l 1.偶极矩为矢量,方向从正电中心指向负电中心。 2.单位为德拜,数量级常在10-30C·m