
酸性水解的讨论 1.酸在反应中的作用有二: ①活化羧基 ②使OH、OR形成链盐而更易离去。 2在酯(RCOOR')中,R有吸电子基团虽能活化 羧羰基,但会使关键中间体正离子能量升高,R 为给电子基团亦有两种相反的作用,故表现不出 明显的影响
1. 酸在反应中的作用有二: ①活化羧基 ②使OH、OR形成 盐而更易离去。 2 在酯 (RCOOR’)中,R有吸电子基团虽能活化 羧羰基,但会使关键中间体正离子能量升高,R 为给电子基团亦有两种相反的作用,故表现不出 明显的影响。 酸性水解的讨论 金羊

3.酯的酸性水解和酯化反应互为逆反应,平衡的 移动取决于反应的条件。体系中有大量水存在, 发生酯的水解。若有大量醇存在,并采取去水 措施,则有利于酯化反应。 U
3. 酯的酸性水解和酯化反应互为逆反应,平衡的 移动取决于反应的条件。体系中有大量水存在, 发生酯的水解。若有大量醇存在,并采取去水 措施,则有利于酯化反应

4.在RCOOR1中, R对速率的影响是:一级>二级>三级 R对速率的影响是:三级>一级>二级 CHCOOR1在盐酸中,于25OC时水解的相对速率v的 实验数据如下: RI: CH3 C2Hs CH(CH3)2 C(CH3)3 V: 1 0.97 0.53 1.15(机理不同)
4. 在RCOOR1中, R对速率的影响是: 一级 > 二级 > 三级 R1对速率的影响是: 三级 > 一级 > 二级 CH3COOR1在盐酸中,于25OC时水解的相对速率v的 实验数据如下: R1: CH3 C2H5 CH(CH3 )2 C(CH3 )3 v: 1 0.97 0.53 1.15(机理不同)

*3酯的酸性水解和碱性水解的异同点 相同点 1都是经过加成消除机理进行的,增大空阻,对反应不利。 2都发生酰氧键断裂 不同点 1催化剂用量不同。碱大于1ol,酸只需要催化量。 2碱催化反应是不可逆的,酸催化反应是可逆的。 3吸电子取代剂对碱性催化有利。对酸性催化没有明显的影响。 4碱性催化:1ROH>2ROH>3ROH 酸性催化:3ROH>1ROH>2ROH 3ROH的水解只能用新的机理来解释
*3 酯的酸性水解和碱性水解的异同点 不 同 点 1 催化剂用量不同。碱大于1 mol,酸只需要催化量。 2 碱催化反应是不可逆的,酸催化反应是可逆的。 3 吸电子取代剂对碱性催化有利。对酸性催化没有明显的影响。 4 碱性催化:1 oROH > 2oROH > 3oROH 酸性催化:3 oROH > 1oROH > 2oROH 相同点 1 都是经过加成消除机理进行的,增大空阻,对反应不利。 2 都发生酰氧键断裂 3 oROH的水解只能用新的机理来解释
*43醇酯的酸性水解历程 反应式 CH3CO18-C(CH3)3+H2O 其CH,COOH+(CH3C-OH 0 OH 反应机 cn o cicu cmeo cicu 关键 OH CH3C+-01CCH3)3 ≥CH3C0180H (CH3)3C+ 间 体 H20 (CH3)3COH +H+ (CH3)C3COH2 通过同位素跟踪可以证明上述反应机制
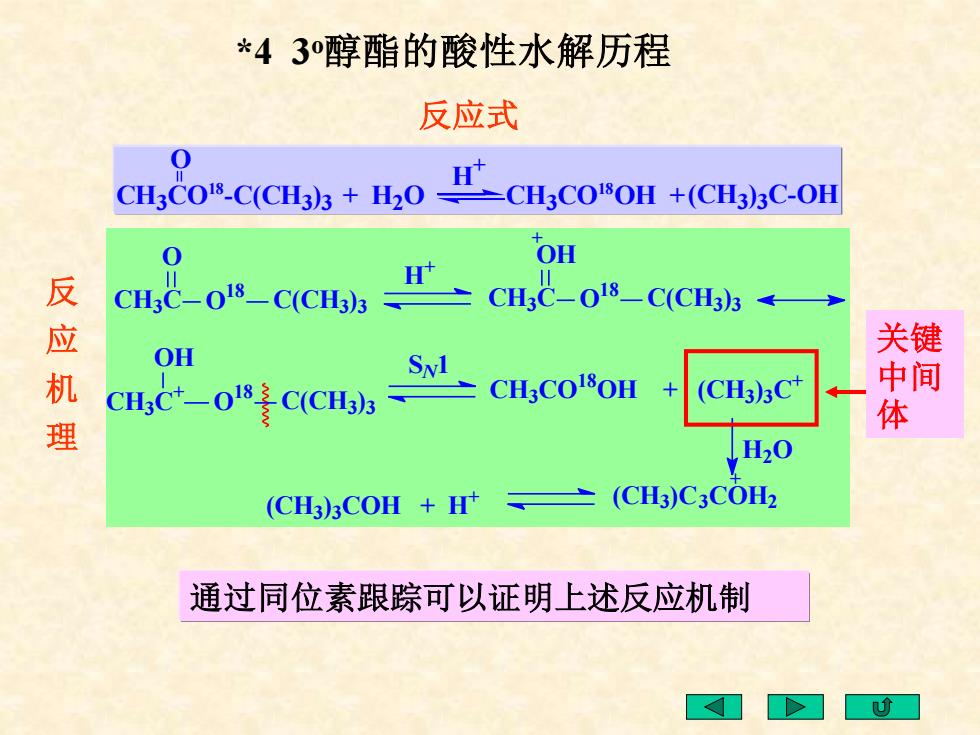
*4 3o醇酯的酸性水解历程 通过同位素跟踪可以证明上述反应机制 反应式 CH3CO18 -C(CH3 )3 O H + + H2O CH3CO18OH +(CH3 )3C-OH 反 应 机 理 CH3C O 18 O C(CH3) 3 H + CH3C O 18 OH C(CH3 ) 3 CH3C + O 18 C(CH3 ) 3 OH SN1 CH3CO 18 OH + (CH3) 3C + H2O (CH3)C3COH2 + + (CH3) 3COH + H + 关键 中间 体