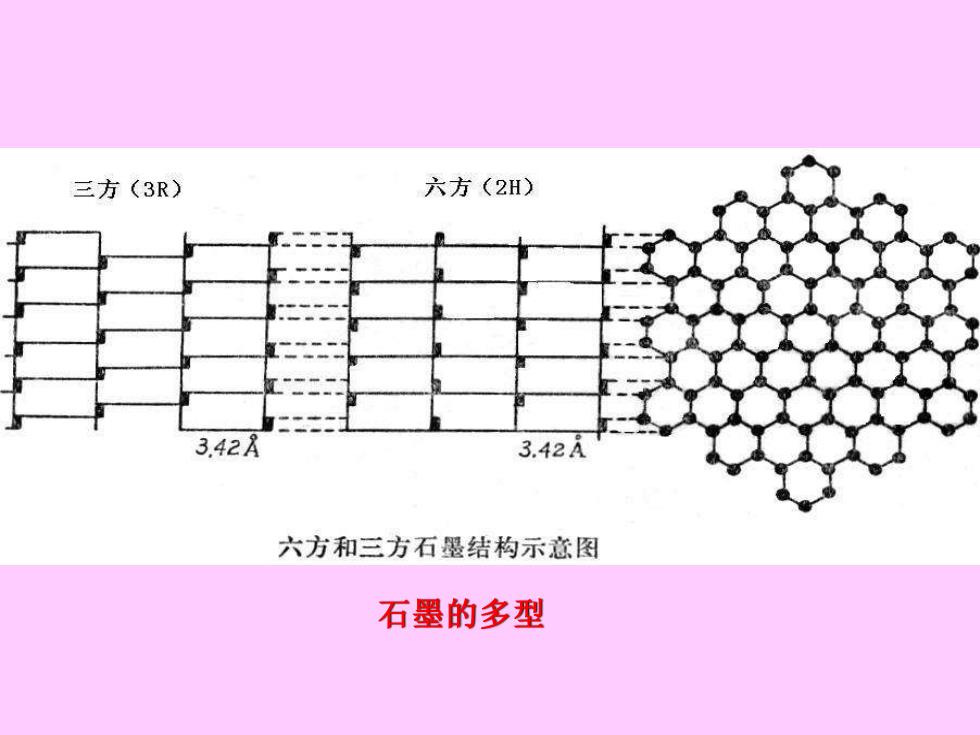
三方(3R) 六方(2H) 3.42A 3.42A 六方和三方石墨结构示意图 石墨的多型
石墨的多型
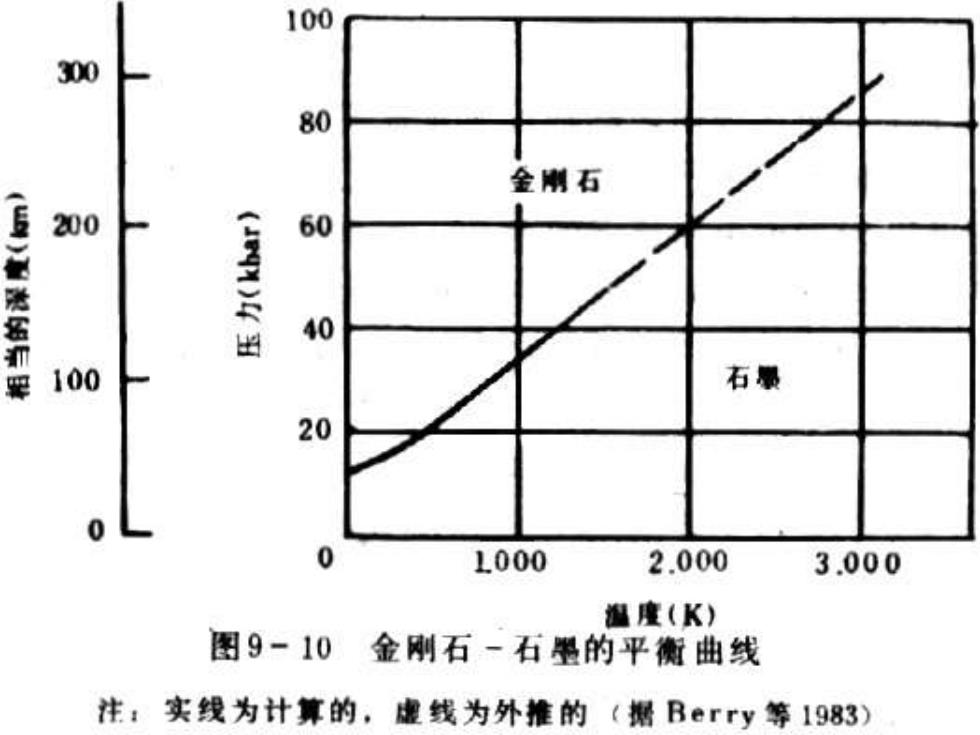
100 300 80 金刚石 200 60 40 100 石最 20 0 0 1000 2.000 3.000 温度(K) 图9一10金刚石-石墨的平衡曲线 注:实线为计算的,虚线为外推的(据Berry等1983)

键型:层内为共价键,层间为分子键 性质:碳原子有一个电子可以在层内移动,平行于层的方向 具有良好的导电性。石墨的硬度低,熔点高,导电性 好。 石墨与金刚石属同质多像变体。 2.4 氯化铯型结构 晶体化学:CsCI 晶体结构:立方晶系,a=0.411nm Z=1 空间格子:CsC是原始格子
键型:层内为共价键,层间为分子键 性质:碳原子有一个电子可以在层内移动,平行于层的方向 具有良好的导电性。石墨的硬度低,熔点高,导电性 好。 石墨与金刚石属同质多像变体。 2.4 氯化铯型结构 晶体化学:Cs Cl 晶体结构:立方晶系,a=0.411nm Z=1 空间格子:Cs Cl是原始格子
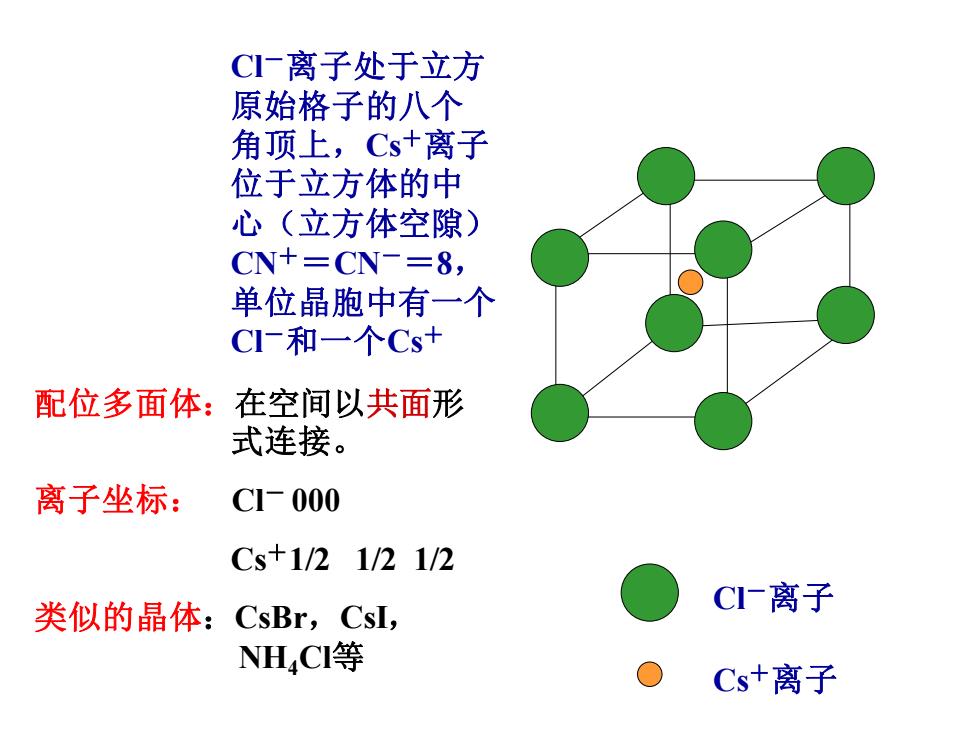
C一离子处于立方 原始格子的八个 角顶上,Cs+离子 位于立方体的中 心(立方体空隙) CN+=CN-=8, 单位晶胞中有一个 CI一和一个Cs+ 配位多面体:在空间以共面形 式连接。 离子坐标: C1-000 Cs+1/21/21/2 CI离子 类似的晶体:CsBr,CsI, NH4CI等 Cs+离子
Cl -离子 Cs +离子 配位多面体:在空间以共面 形 式连接。 离子坐标: Cl - 000 Cs +1/2 1/2 1/2 类似的晶体 :CsBr ,CsI , NH 4Cl 等 Cl -离子处于立方 原始格子的八个 角顶上,Cs +离子 位于立方体的中 心(立方体空隙) CN + =CN - = 8 , 单位晶胞中有一个 Cl -和一个Cs +