
第十章离子化合物的结构化学 (课堂讲授0学时) 1.离子键和点阵能 2.离子半径 3.离子配位多面体及其连接方式 4.若干典型离子化合物的结构 *5.硅酸盐的结构化学
第十章 离子化合物的结构化学 (课堂讲授0学时) 1. 离子键和点阵能 2. 离子半径 3. 离子配位多面体及其连接方式 4. 若干典型离子化合物的结构 *5. 硅酸盐的结构化学

第十章离子化合物 教学目标 通过本章学习,掌握典型离子晶体结构、离子半径比 与离子极化对晶体晶型的影响。 学习要点 二元典型离子晶体NaCl、CCl、ZnS、CaF2、Ti02结构。 (2) 离子半径比与配位多面体 (3) 离子极化对晶型的影响 () Pauling规刚与多元离子化合物。 学时安排 学时-2学时
第十章 离子化合物 教学目标 学习要点 学时安排 通过本章学习,掌握典型离子晶体结构、离子半径比 与离子极化对晶体晶型的影响。 ⑴ 二元典型离子晶体NaCl、CsCl、ZnS、CaF2、TiO2结构。 ⑵ 离 子 半 径 比 与 配 位 多 面 体 。 ⑶ 离 子 极 化 对 晶 型 的 影 响 。 ⑷ Pauling 规则与多元离子化合物。 学时- 2学时

第10章.离子化合物的结构化学 10.1离子晶体的若干简单结构型式 1.离子化合物: 由正负离子结合在一起形成的化合物, 它一般由电负性较小的金属元素与电负性较 大的非金属元素生成。正负离子之间由静电 力作用结合在一起,这种化学键称为离子键。 以离子键结合的化合物倾向于形成晶体,以 使每个离子周围配位尽可能多的异性离子, 降低体系能量
第10章.离子化合物的结构化学 由正负离子结合在一起形成的化合物, 它一般由电负性较小的金属元素与电负性较 大的非金属元素生成。正负离子之间由静电 力作用结合在一起,这种化学键称为离子键。 以离子键结合的化合物倾向于形成晶体,以 使每个离子周围配位尽可能多的异性离子, 降低体系能量。 10.1 离子晶体的若干简单结构型式 1.离子化合物:

2离子晶体的若王简单结构型式: 许多离子晶体的结构可按密堆积 结构来理解。当负离子的半径较大时, 一般会把负离子看作等径圆球进行密 堆积,而正离子有序地填在空隙之中。 当正离子的半径较大时,也可以把正 离子看作等径圆球进行密堆积,负离 子作填隙原子。前一种情况出现得比 较多
许多离子晶体的结构可按密堆积 结构来理解。当负离子的半径较大时, 一般会把负离子看作等径圆球进行密 堆积,而正离子有序地填在空隙之中。 当正离子的半径较大时,也可以把正 离子看作等径圆球进行密堆积,负离 子作填隙原子。前一种情况出现得比 较多。 2.离子晶体的若干简单结构型式:
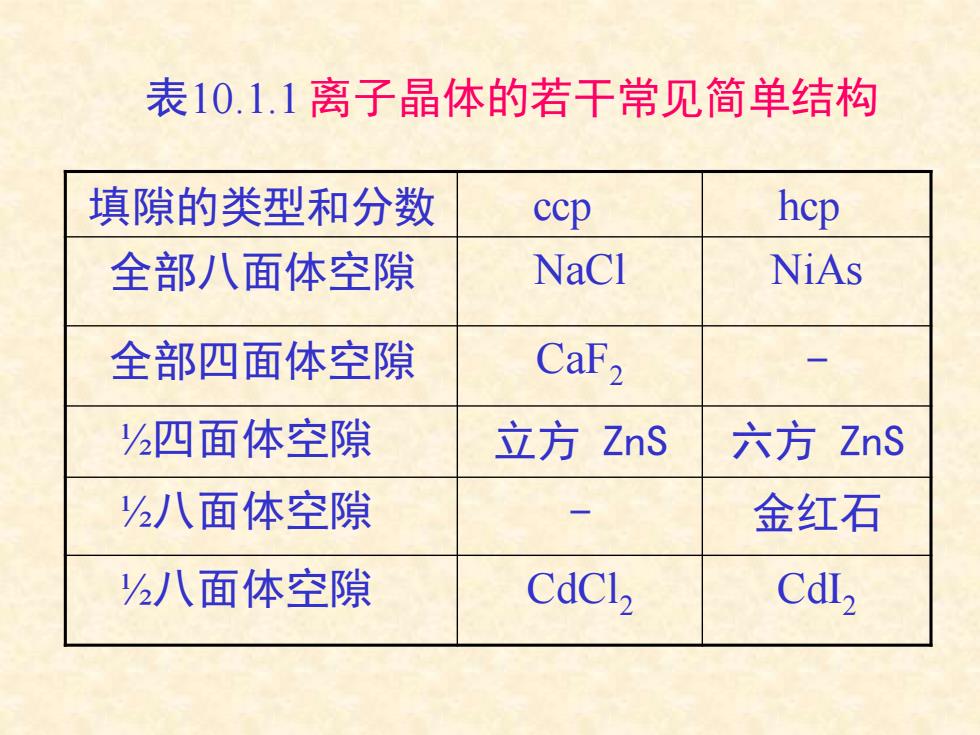
表10.1.1离子晶体的若干常见简单结构 填隙的类型和分数 ccp hcp 全部八面体空隙 NaCl NiAs 全部四面体空隙 CaF2 四面体空隙 立方ZnS 六方ZnS 八面体空隙 金红石 八面体空隙 CdCl2 CdI
表10.1.1 离子晶体的若干常见简单结构 填隙的类型和分数 ccp hcp 全部八面体空隙 NaCl NiAs 全部四面体空隙 CaF2 - ½四面体空隙 立方 ZnS 六方 ZnS ½八面体空隙 - 金红石 ½八面体空隙 CdCl2 CdI2