
7.6.4化学反应动力学与扩散共同控制范围:V.≈V。 7.6.4.1 Doraiswamy和Tamhankar对两种固相反应物形成连续 固溶体体系的处理 C* AO B203 AO B203 =0 =0 1→ (→ t=0 t>0 (a)无反应发生 (b)反应区形成,但无产物层 产物区反应区 产物区反应区 C C* AO B203 AO B203 =0 =0 → t>0 t>0 (c)产物区域、反应区域同时存在, (产物区域、反应区域同时存在, 产物区没有扩散阻力 产物区有扩散阻力
7.6.4 化学反应动力学与扩散共同控制范围 : V R ≈ V D 7641 . . . Doraiswamy Doraiswamy 和Tamhankar Tamhankar对两种固相反应物形成连续 对两种固相反应物形成连续 固溶体体系的处理 C* AO B 2 O 3 AO B 2 O 3 C l=0 l → t = 0 l=0 l → t 0 t>0 (a) 无反应发生 反应区 产物区 反应区 (b) 反应区形成,但无产物层 产物区 AO B 2 O 3 AO B 2 O 3 C* C* Cp Cp l p l → l → l=0 l p l=0 l r l r l → t>0 l → t>0 (c) 产物区域、反应区域同时存在, 产物区没有扩散阻力 (d) 产物区域、反应区域同时存在, 产物区有扩散阻力

7.6.4化学反应动力学与扩散共同控制范围:V.≈V。 A)产物层 假设扩散系数与组成无关,则Fick第二定律可写作 02c at Do ay2 D,为产物层中所讨论组份的扩散系数。 上式的初始条件和边界条件为: t=O时,在y<0处C=C°,在y>0处C=0;t>0时,在y<0处C=C,在y=y处C=C。 (其中C为产物层末端处组份浓度:y%产物层厚度。) 如果反应物颗粒尺寸比产物层厚度大得多,则应满足的初始/边界条件为:0时,在y=∞处C=O。 则方程的解为: C=C"erfc2(Dp) 令:0=总2=兰日=芒,L为反应物颗粒的长度。则: w=erfc20172 上式中的变量均为无量纲变量。产物层末端的无量纲浓度为: Zp ω=erf 2817=1-erf Zp 01/2 f
7.6.4 化学反应动力学与扩散共同控制范围 : V R ≈ V D A) 产物层 假设扩散系数与组成无关,则Fick第二定律可写作 上式中的变量均为无量纲变量。产物层末端的无量纲浓度为:
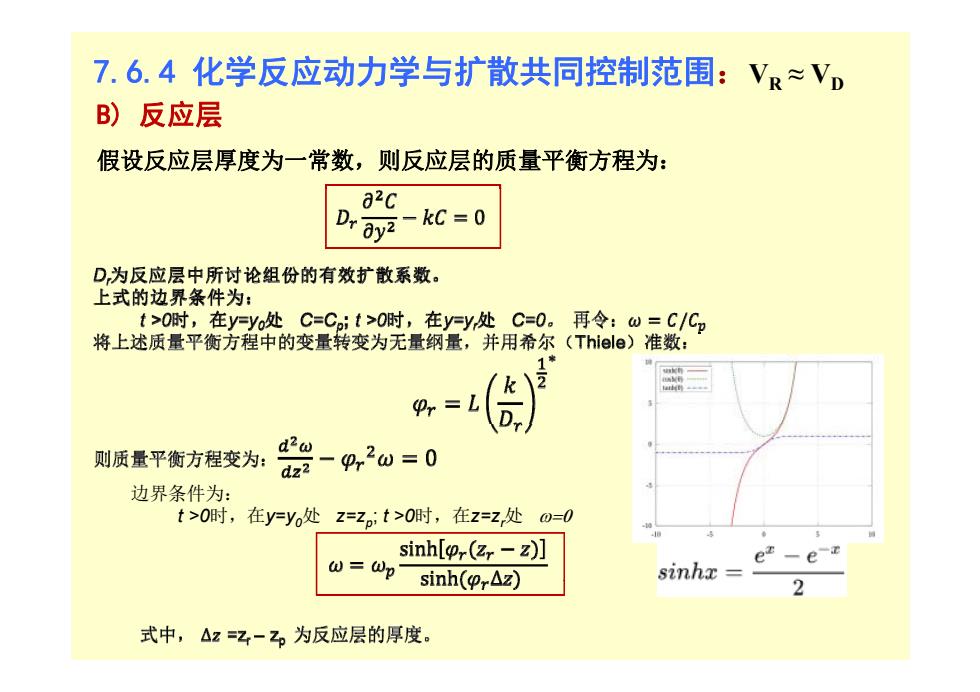
7.6.4化学反应动力学与扩散共同控制范围:V≈VD B)反应层 假设反应层厚度为一常数,则反应层的质量平衡方程为: 82C D,0y2 -kC=0 D,为反应层中所讨论组份的有效扩散系数。 上式的边界条件为: t>0时,在yyo处C=C:t>0时,在yy处C=0。再令:w=C/C2 将上述质量平衡方程中的变量转变为无量纲量,并用希尔(Thiele)准数: * k 2 Pr= d2w 则质量平衡方程变为: z2-4,2w=0 边界条件为: t>0时,在y=y处z=z:t>0时,在z=z处 0=0 W=Wp sinh[opr(zr-z)] ez-e-z sinh(pr△z) sinhx= 式中,△z=2-2为反应层的厚度
7.6.4 化学反应动力学与扩散共同控制范围 : V R ≈ V D B) 反应层 假设反应层厚度为一常数,则反应层的质量平衡方程为: 边界条件为: t >0时,在y=y0 处 z=zp; t >0时,在z=zr 处

7.6.4.2经验公式 有一些经验公式可以处理由化学反应和扩散共同控制的固-固反应。 A)塔曼(Taman)公式: y=krInt 式中,k,为常数,与温度、扩散系数、反应物颗粒接触状况有关。 B)泰普林(Tapline)公式: 对于粉料的固-固反应, dy d(ta=ke(1-By)m 式中,α是与过程的控制步骤有关的参数,m为反应级数,B为常数, k为常数
7.6.4.2 经验公式 有一些经验公式可以处理由化学反应和扩散共同控制的固-固反应。 A) 塔曼(Taman)公式: 式中, kr 为常数 与温度 扩散系数 反应物颗粒接触状况有关 为常数,与温度、扩散系数、反应物颗粒接触状况有关。 B) 泰普林(Tapline)公式: 对于粉料的固-固反应, 式中, 是与过程的控制步骤有关的参数,m 为反应级数,为常数, kt 为常数

7.7影响固相反应的因素 、反应物化学组成与结构的影响 反应物结构状态质点间的化学键性质、各种缺陷的多少都 会影响反应速率。 利用多晶转变、热分解、脱水反应等过程引起晶格效应来 提高生产效率。 如:Al203+Co0-→CoAl204 常用轻烧A1203而不用较高温度死烧A1203作原料,原因为轻烧 A1203中有Y-Al203→a一A1203(900-1000℃)转变,提高了 AI203的反应活性。其反应速度相差近十倍,表明轻烧AI03具有 高得多的反应活性。这被称为Hedval I(赫特华尔)效应
7.7 影响固相反应的因素 一 、反应物化学组成与结构的影响 反应物结构状态质点间的化学键性质、各种缺陷的多少都 会影响反应速率。 利用多晶转变、热分解、脱水反应等过程引起晶格效应来 提高生产效率。 如:Al2O3+CoOCoAl2O4 常用轻烧Al2O3而不用较高温度死烧 而不用较高温度死烧Al2O3作原料 原因为轻烧 作原料,原因为轻烧 Al2O3中有- Al2O3 - Al2O3 ( 900-1000C)转变,提高了 Al2O3的反应活性。其反应速度相差 其反应速度相差近十倍,表明轻烧Al2O3具有 高得多的反应活性。这被称为Hedvall(赫特华尔)效应