
2.2.4紫外可见光谱基本原理 2.π→π*跃迁-一K带 never forget how to dream π→π* 跃迁能小于 吸收 紫外区至可见光区 电子跃迁 0→0* (入max>160nm) 跃迁 π→π*跃迁的特点: △E n π 1).允许跃迁,吸收强度强 2).孤立双键的π→π*跃迁大多在约200nm左右有吸收,>104 3).共轭双键的π→π*跃迁的吸收>200nm,e>104(Lmo1.cm-) 由共轭体系的π一→π*跃迁所产生的吸收带称为K(德语“共轭的”)带 如T→T*跃迁: 极性溶剂的加入会使吸收波长怎样变化? CH2=CH2:入max为165nm; 16 CH2=CH-CH=CH2:217nm 22紫外-可见光潜
16 2. π→π*跃迁-—K带 π→π* 电子跃迁 跃迁能小于 σ→σ* 跃迁 紫外区至可见光区 (λmax>160nm) 吸收 如 π→π* 跃迁: CH2=CH2 :λmax为165nm ; CH2=CH-CH=CH2 :217nm π→π* 跃迁的特点: 1). 允许跃迁, 吸收强度强 2). 孤立双键的π→π* 跃迁大多在约200nm左右有吸收, ε>104 3). 共轭双键的π→π* 跃迁的吸收>200nm, ε>104(Lmol-1cm-1) 由共轭体系的π→π* 跃迁所产生的吸收带称为K(德语“共轭的”)带 s p * s * n p E 2.2 紫外-可见光谱 2.2.4 紫外-可见光谱基本原理 极性溶剂的加入会使吸收波长怎样变化?

2.2.4紫外可见光谱基本原理 never forget how to dream 3.n→π*跃迁--R带 nπ* 跃迁能 吸收 电子跃迁 较小 近紫外光(入max:200-400nm) 产生n→π*跃迁的条件: 1).分子中有含杂原子的双键(C=0,C=S). 2).杂原子上的孤电子对与碳原子上的π电子形成印- π共轭(CH2CH-OCH3). n→π*跃迁的特点: △E 吸收强度很弱,£<100(Lmo1-1.cm) 例如:HCH0的n一T所产生的吸收带入max为310nm 17 极性溶剂的加入会使吸收波长怎样变化? 22紫外-可见光潜
17 3. n→π*跃迁---R带 n→π* 电子跃迁 跃迁能 较小 近紫外光(λmax:200-400nm) 吸收 例如: HCHO的 n→π*所产生的吸收带λmax为310nm 产生 n→π*跃迁的条件: 1). 分子中有含杂原子的双键(C=O, C=S). 2). 杂原子上的孤电子对与碳原子上的π电子形成p- π共轭( CH2=CH-OCH3). n→π* 跃迁的特点: 吸收强度很弱, ε<100(Lmol-1 cm-1) s p * s * n p E 2.2 紫外-可见光谱 2.2.4 紫外-可见光谱基本原理 极性溶剂的加入会使吸收波长怎样变化?
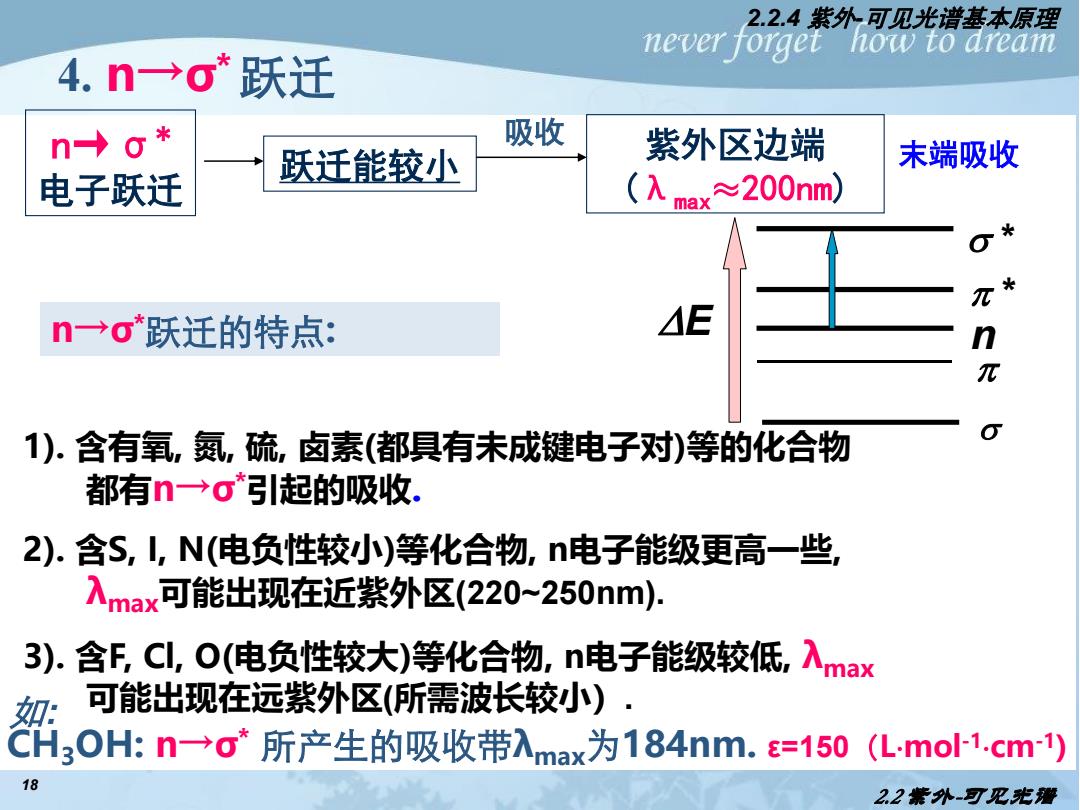
2.2.4紫外-可见光谱基本原理 never forget how to dream 4.n→o*跃迁 n→0* 吸收 跃迁能较小 紫外区边端 末端吸收 电子跃迁 (入max≈200nm) n→σ*跃迁的特点: △E n π 1).含有氧,氮,硫,卤素(都具有未成键电子对)等的化合物 都有→σ*引起的吸收. 2).含S,1,N(电负性较小)等化合物,n电子能级更高一些, 入max可能出现在近紫外区(220-250nm). 3).含F,CL,O(电负性较大)等化合物,n电子能级较低,入max 如 可能出现在远紫外区(所需波长较小)· H30H:n→o所产生的吸收带入max为184nm.=150(L-mo1.cm) 18 22紫外-可见光潜
18 4. n→σ*跃迁 如: CH3OH: n→σ* 所产生的吸收带λmax为184nm. ε=150(Lmol-1cm-1) n→σ*跃迁的特点: 1). 含有氧, 氮, 硫, 卤素(都具有未成键电子对)等的化合物 都有n→σ*引起的吸收. 2). 含S, I, N(电负性较小)等化合物, n电子能级更高一些, λmax可能出现在近紫外区(220~250nm). 3). 含F, Cl, O(电负性较大)等化合物, n电子能级较低, λmax 可能出现在远紫外区(所需波长较小). n→σ* 电子跃迁 跃迁能较小 紫外区边端 (λmax ≈200nm) 吸收 末端吸收 s p * s * n p E 2.2 紫外-可见光谱 2.2.4 紫外-可见光谱基本原理
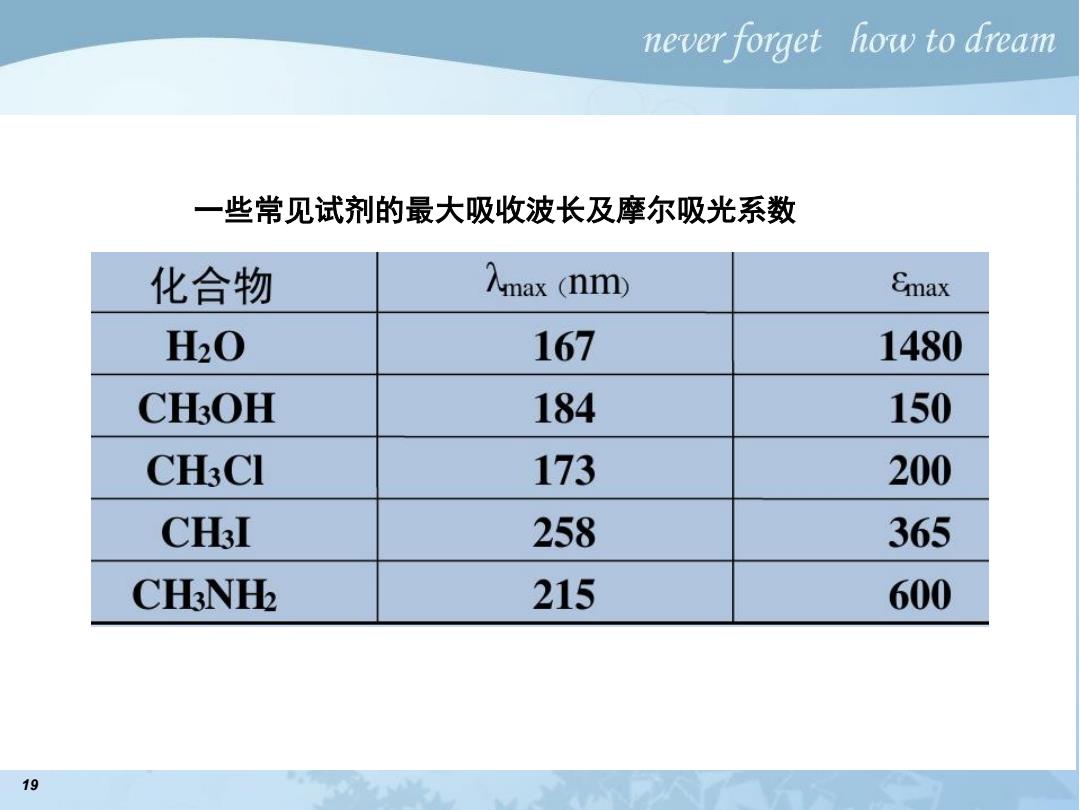
never forget how to dream 一些常见试剂的最大吸收波长及摩尔吸光系数 化合物 入max (nm Emax H20 167 1480 CH3OH 184 150 CH:CI 173 200 CH3I 258 365 CHNH五 215 600 19
19 一些常见试剂的最大吸收波长及摩尔吸光系数
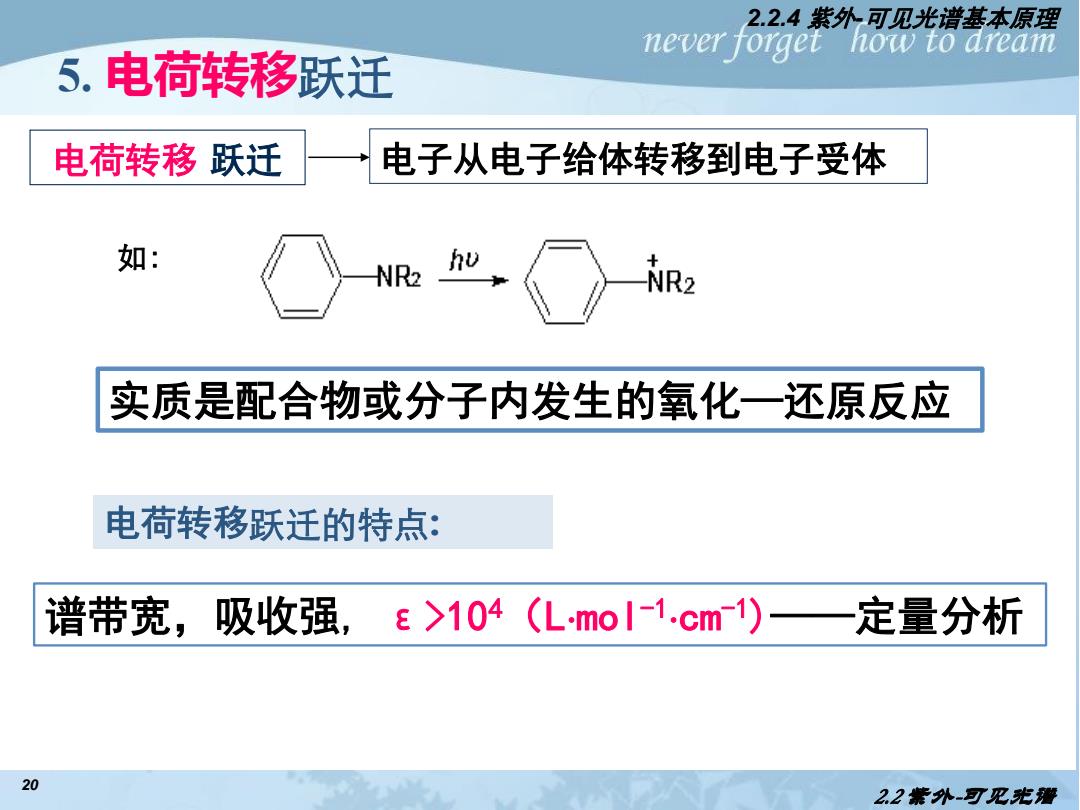
2.2.4紫外可见光谱基本原理 never forget how to dream 5.电荷转移跃迁 电荷转移跃迁 电子从电子给体转移到电子受体 如: NR2 hu NR2 实质是配合物或分子内发生的氧化一还原反应 电荷转移跃迁的特点: 谱带宽,吸收强,e>104(Lmo1-1.cm) —定量分析 20 22紫外-可见光潜
20 5. 电荷转移跃迁 电荷转移 跃迁 电子从电子给体转移到电子受体 2.2 紫外-可见光谱 2.2.4 紫外-可见光谱基本原理 如: 实质是配合物或分子内发生的氧化—还原反应 电荷转移跃迁的特点: 谱带宽,吸收强, ε>104(Lmol-1 cm-1)——定量分析