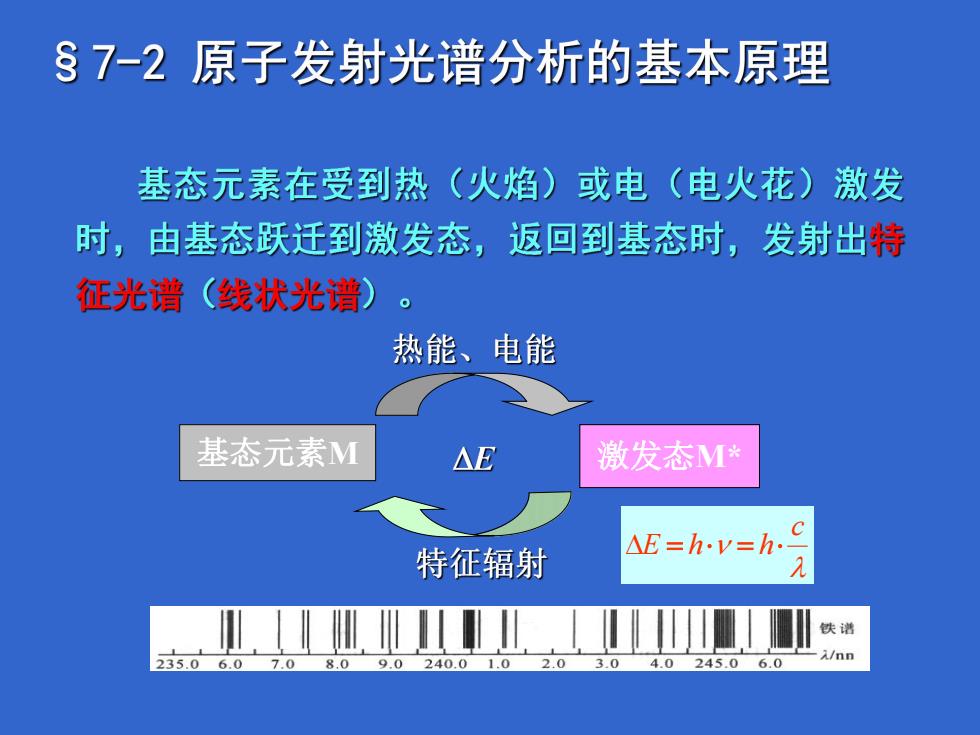
§7-2原子发射光谱分析的基本原理 基态元素在受到热(火焰)或电(电火花)激发 时,由基态跃迁到激发态,返回到基态时,发射出特 征光谱(线状光谱) 热能、电能 基态元素M △E 激发态M 特征辐射 AE=h.v=h.c 铁谱 235.0 45.0 6.0 入/nn
基态元素M 激发态M* c E h h
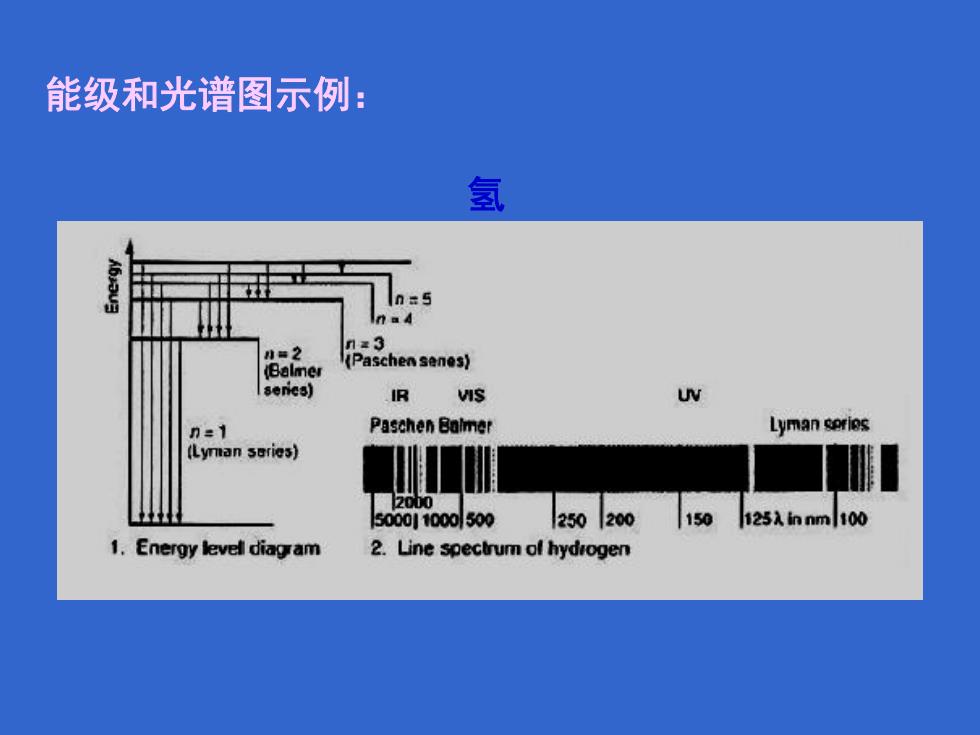
能级和光谱图示例: 氢 升2 13 (Paschen senes) (Balmer 8enes) R VIS UV n1 Paschen Balmer Lyman sories 化yman saries) 2000 500011000500 250200 150 1.Energy levell diagram 2.Line spectrum of hydrogen
能级和光谱图示例: 氢

通过测量物质的激发态原子发射光谱线的波 长和强度进行定性和定量分析的方法叫(原子) 发射光谱分析法。 发射光谱法有许多技术如电弧、火花、等离 子炬等作为激发源,使被测物质原子化并激发气 态原子或离子的外层电子,使其发射特征光谱, 其波长范围一般在190~900nm

原子中某一外层电子由基态激发到高能级所 需要的能量称为微发电位。原子光谱中每一条谱 线的产生各有其相应的激发电位。 由(第一)激发态向基态跃迁所发射的谱线 称为(第一)共振线。共振线具有最小的激发电 位,因此最容易被激发,为该元素最强的谱线。 同样,离子也可能被激发,其外层电子跃迁 也发射光谱,产生离子线。由于离子和原子具有 不同的能级,所以离子线与原子线不一样。 原子光谱主要由原子线组成,也包含某些离 子线,其表示方法如何?

在原子谱线表中,罗马数I表示中性原子发射光 谱的谱线,Ⅱ表示一次电离离子发射的谱线,Ⅲ表示 二次电离离子发射的谱线.例如MgI285.21nm为原 子线,MgⅡ280.27nm为一次电离离子线。 发射光谱分析的基本依据: 从识别元素的特征光谱来鉴别元素的存在(定性 分析);而这些谱线的强度又与试样中该元素的含量 有关,因此又可利用这些谱线的强度来测定元素的含 量(定量分析)