7.3高温氧化还原反应的自发性及埃灵罕姆图(spontaneity of redox reactions at high temperature and the diagram of Ellingham) Ellingham图对一个具体反应而言,如果将一定温度区间内反应 的焓变和熵变近似地看作常数,由△G=△H9+T△S知,以 △G对T作图应该得到斜率为一△S的直线.△G9-T图又叫埃灵罕 姆图,可十分方便地用于讨论高温下的某些氧化还原过程 △G9(C0,C02) Ag.o (reaction c, +250 gas consumed) Cuo △.GeM,MO) (reaction d, co/cO. gas consumed) Zno Feo 司 -500 △Ge(C,Co2 (reaction b. T02 C/CO no net gas Al.O. formation) -1000 Mgo △.Ge(C,cO) Cao (reaction a, gas formed) 500 100015002000 2500 Temperature TemperatureFC 16 页 节首 节尾
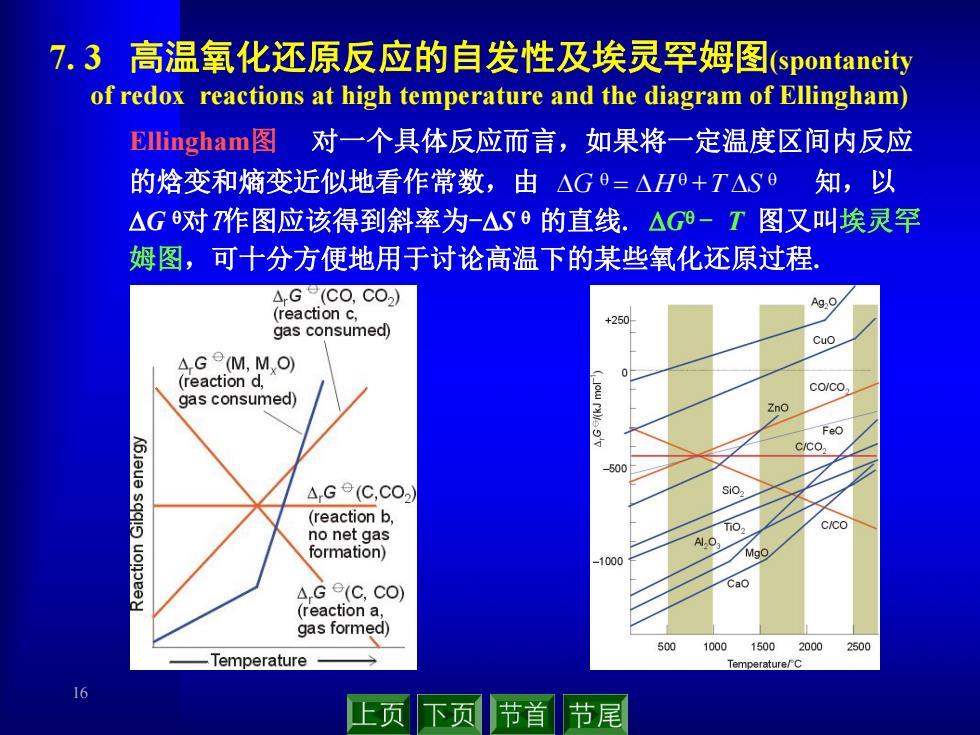
16 Ellingham图 对一个具体反应而言,如果将一定温度区间内反应 的焓变和熵变近似地看作常数,由 知,以 G q对T作图应该得到斜率为-S q 的直线. Gq - T 图又叫埃灵罕 姆图,可十分方便地用于讨论高温下的某些氧化还原过程. G q H q +T S q 7. 3 高温氧化还原反应的自发性及埃灵罕姆图(spontaneity of redox reactions at high temperature and the diagram of Ellingham)

从图中可以看出 C(s)+02(g)=CO2(g) △G(C,CO2),△S9≈0 ① 2C(S)+02(g=2C0(g) △G9(C,CO), △S9>0 ② 2C0s)+02(g)=2C02(g) △G(CO,C02) ③ (2/x)M(s或1)+O2g △G9M,MO) =(2x)MO,(S) 若△G9M,MO)>0,则金属氧化物在该温度下分解 用①~③分别减去④得 C(S)+(2x)MO.(s)=(2/x)M0+CO2(g 2C(S)+(2/x)MO.(S)=(2/x)MI)+2CO(g) 2CO(g)+(2/x)MO,(s)=(2/x)MI)+2CO2(g) 上页下页 节首节尾
17 若Gq (M,MOx) >0,则金属氧化物在该温度下分解. Gq (C,CO2 C(s) +O2(g) = CO2(g) ),Sq ≈ 0 ① Gq 2C(s) +O2(g) = 2CO (g) (C,CO), Sq > 0 ② Gq (CO,CO2 2CO(s) +O2(g) = 2CO2 (g) ) ③ Gq (M,MOx (2/x)M(s或1) +O2(g) ) ④ = (2/x) MOx (s) Sq < 0 从图中可以看出 用①~③分别减去④得 C(s) + (2/x)MOx(s) = (2/x)M(l) + CO2 (g) 2C(s) + (2/x)MOx(s) = (2/x)M(l)+2CO (g) 2CO(g) + (2/x)MOx(s) = (2/x)M(l)+2CO2 (g)

则 △9=△G9C,CO)-△G(M,MO,》 △G9=△G(C,CO)-△G(M,MO) △G9=△G(CO,CO2)-△G(M,MO) 显然,只要在给定的温度区间内金属氧化反应的线段处于C和C0 氧化反应的任一线段上方,相应的热还原反应在热力学上才是允许 的同理也适用于非碳还原剂的还原反应.如果用金属M’代替C或CO ,应该得到: △G<0 △G9=△9M,MPO,)-△9(M,MO) 这意味着只要△G(M,MO)的线段处于△GM,MPO)线段 上方,金属M就可用来还原金属M的氧化物 18 上页 下页 节首 节尾
18 显然,只要在给定的温度区间内金属氧化反应的线段处于C和CO 氧化反应的任一线段上方,相应的热还原反应在热力学上才是允许 的同理也适用于非碳还原剂的还原反应.如果用金属M’代替C或CO ,应该得到: Gq = Gq(M’ , M’ Ox) – Gq( M, MOx) 这意味着只要 Gq( M, MOx) 的线段处于Gq(M’ , M’ Ox)线段 上方,金属M’就可用来还原金属M的氧化物 Gq <0 Gq = Gq(C,CO) – Gq( M, MOx) Gq = Gq(CO,CO2 ) – Gq( M, MOx) 则 Gq = Gq(C,CO2) – Gq( M, MOx)

Example 7 MgO被C还原的最低温度是多少?写出总反应方程式 Solution MgO的线段在1800℃附近上升至C→CO线段以上,这个温度 就是MgO被C还原的最低温度 C和Mg的氧化反应分别为 2C(s)+O2(g)=2CO(g〉 2Mg(s)+02(g)=2MgO(s) 相减即得 2C(s)+2MgO(s)=2Mg (s)+CO(g) 简 化 C(s)+MgO(s)=Mg (s)+CO(g) 上页下页节首 节尾
19 MgO被C还原的最低温度是多少?写出总反应方程式. MgO的线段在1800℃附近上升至C → CO线段以上,这个温度 就是MgO被C还原的最低温度 相减即得 简 化 2C(s) + O2(g) = 2CO(g) 2Mg(s) + O2(g) = 2MgO(s) 2C(s) + 2MgO (s) = 2Mg (s) + CO(g) C(s) + MgO (s) = Mg (s) + CO(g) C和Mg的氧化反应分别为 Example 7 Solution

7.4 水溶液中氧化还原反应的自发性和电极电势(spontaneity of redox reactions in aqueous solutions and electrode potential 7.4.1氧化还原与化学电池(redox and galvanic cells) (1)铜锌原电池,亦叫Daniell电池 Salt bridg 1.10 Voltmeter (5%r) Salt bridge rous disk 工作状态的化学电池同时发生三个过程: 。两个电极表面分别发生氧化反应和还原反应 ●电子流过外电路 ●离子流过电解质溶液 20 上页下页 节首 节尾
20 7. 4 水溶液中氧化还原反应的自发性和电极电势 (spontaneity of redox reactions in aqueous solutions and electrode potential ) 7. 4. 1 氧化还原与化学电池 (redox and galvanic cells) (1) 铜锌原电池,亦叫 Daniell 电池 工作状态的化学电池同时发生三个过程: ● 两个电极表面分别发生氧化反应和还原反应 ● 电子流过外电路 ● 离子流过电解质溶液