
3.3理想间歇反应器中的均相可逆 反应 化学化工学院 化学反应工程 1王红军
化学化工学院 化学反应工程 1王红军 3.3理想间歇反应器中的均相可逆 反应

3.3.1可逆反应的特点 ad+bBcC 吉 净反应速率等于正反应和逆反应速率之差 (-r)=kCaCh-kzCc, a,B,y分别为正反应和逆反应级数。 当反应达到平衡时,净反应速率为零。 k2ce“CB 若反应物和产物对正反应和逆反应 速率都有影响,则 不( -)=kC4CRC-kCCC 化学化工学院 化学反应工程 2王红军
化学化工学院 化学反应工程 2王红军 1 2 1 2 1 2 ( ) , , , ( ) k k A A B C e Ae Be A A B C A B C aA bB cC r k C C k C C c C r k C C C k C C C + − = − = − = − 1 2 净反应速率等于正反应和逆反应速率之差 分别为正反应和逆反应级数。 当反应达到平衡时,净反应速率为零。 k k 若反应物和产物对正反应和逆反应 速率都有影响,则 3.3.1 可逆反应的特点
C-Y k2 从热力学分析可知,如系统为气体混合物, ☒无法显示该图 则平衡常数K为 K= CheCke 假设 =K,则 k2 Cr-r ca-a ,m为任意常数 Ae CaeC 化学反应工程 化工原理教研室
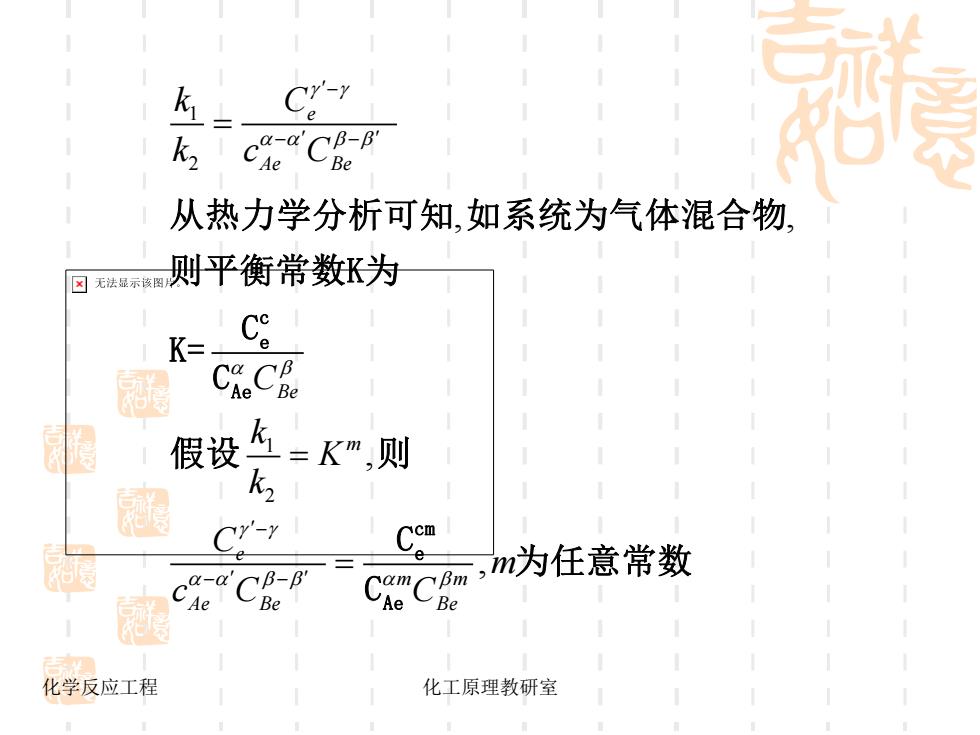
化学反应工程 化工原理教研室 1 2 1 2 , , , , e Ae Be Be m e m m Ae Be Be k C k c C C k K k C m c C C − − − − − − = = = c e Ae cm e Ae 从热力学分析可知 如系统为气体混合物 则平衡常数K为 C K = C 假设 则 C 为任意常数 C

a-a_(B-1_-y2=m a b 表明可逆反应中对任何反应组分而言的反应级数 之差与该反应的化学计量系数之比为定值。该式 可以作为验证可逆反应动力学方程测定结果的判定。 化学平衡常数与正逆反应速率常数的K=1关系,只 k 有在m=1时才是正确的。 化学反应工程 化工原理教研室
化学反应工程 化工原理教研室 2 ( ) ( ) ( ) m a b c k − − − = = = 1 表明可逆反应中对任何反应组分而言的反应级数 之差与该反应的化学计量系数之比为定值。该式 可以作为验证可逆反应动力学方程测定结果的判定。 k 化学平衡常数与正逆反应速率常数的K= 关系,只 有在m=1时才是正确的

对一级反应 A台R 5=-=C,kC即为: dt Ta=k C4o(1-X)-k2C40X 当达到平衡时,r4=0,即为: kCe-kCc=O,由此可见 K h=CReC4-CA k2 Che Che 1-XAe 该式表明:可逆反应的反应程度受平衡条件的限制,平 衡常数与反应温度和热效应间满足范霍夫方程。 化学反应工程 化工原理教研室
化学反应工程 化工原理教研室 对一级反应 1 2 1 0 2 0 1 2 Re 1 Re 0 2 , (1 ) 0, 0, 1 A A A R A A A A A A Ae A A Ae Ae Ae Ae A R dC r k C k C dt r k C x k C x r k C k C k C C C x K k C C x = − = − = − − = − = − = = = = − 即为: 当达到平衡时, 即为: 由此可见 该式表明:可逆反应的反应程度受平衡条件的限制,平 衡常数与反应温度和热效应间满足范霍夫方程