
14-2-2卤素的制备和用途 大量的碘还来源于自然界的碘酸钠,因此, 要用还原剂使O3离子还原为L。最常用的还 原剂为NaHSO3,其离子反应式为: 2IO2+5HSO,==5SO2+H,0+3H+ 实际的做法是先用适量的亚硫酸氢盐将碘 酸盐还原成碘化物; I03+3HS03==+3S0,2-+3HH 再将所得的酸性碘化物溶液与适量的碘酸盐 溶液作用便有碘析出: 1O+5+6Ht==3I,+3H,0 在酸性溶液中1O3可将氧化成L2,而且纯的 碘酸钠可作基准物质,在分析化学中利用此反 应来制备碘的标准溶液
14-2-2 卤素的制备和用途 大量的碘还来源于自然界的碘酸钠,因此, 要用还原剂使IO3 -离子还原为I2。最常用的还 原剂为NaHSO3,其离子反应式为: 2IO3 -+5HSO3 -==5SO4 2-+H2O+3H++I2 实际的做法是先用适量的亚硫酸氢盐将碘 酸盐还原成碘化物; IO3 -+3HSO3 -==I-+3SO4 2-+3H+ 再将所得的酸性碘化物溶液与适量的碘酸盐 溶液作用便有碘析出: IO3 -+5I-+6H+==3I2+3H2O 在酸性溶液中IO3 -可将I -氧化成I2,而且纯的 碘酸钠可作基准物质,在分析化学中利用此反 应来制备碘的标准溶液
14-3氟氯溴碘的化合物 14-3-1卤化氢和氢氟酸 一、 卤化氢和氢氟酸的物理性质 性质 H亚 HCI HBr HI 熔点/℃ -83.1 -114.8 -88.5 -50.8 沸点/℃ 19.54 -84.9 -67 -35.38 /(kJ.mol-1) -271.1 -92.307 -36.4 26.48 键能/(kJ.mol-1) 568.6 431.8 365.7 298.7 △/(kJmol-1) 30.31 16.12 17.62 19.77 分子偶极矩(10-30cm 6.40 3.61 2.65 27 表观解离度 (0.1molL-1,18℃)/% 10 93 93.5 溶解度/g(100gH2O)1 35.3 42 49
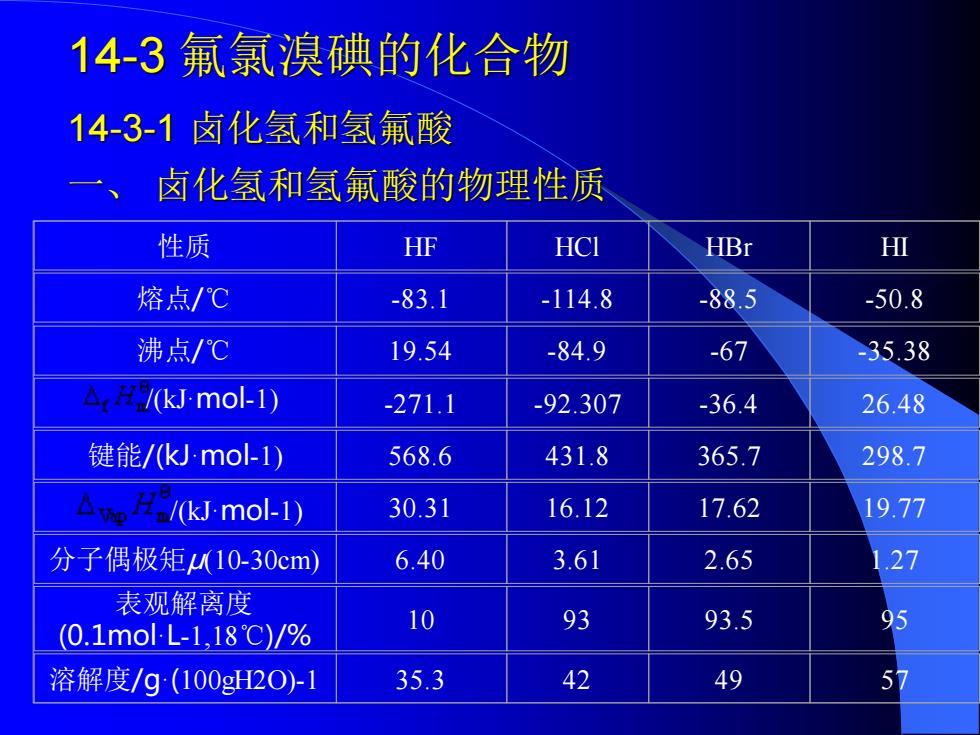
14-3 氟氯溴碘的化合物 14-3-1 卤化氢和氢氟酸 性质 HF HCl HBr HI 熔点/℃ -83.1 -114.8 -88.5 -50.8 沸点/℃ 19.54 -84.9 -67 -35.38 -271.1 -92.307 -36.4 26.48 键能/(kJ·mol-1) 568.6 431.8 365.7 298.7 30.31 16.12 17.62 19.77 分子偶极矩μ(10-30cm) 6.40 3.61 2.65 1.27 表观解离度 (0.1mol·L-1,18℃)/% 10 93 93.5 95 溶解度/g·(100gH2O)-1 35.3 42 49 57 /(kJ·mol-1) /(kJ·mol-1) 一、 卤化氢和氢氟酸的物理性质