乙二胺四乙酸:EDTA EDTA(乙二胺四乙酸)结构 H 两个氨氮 OOCH>C H H世CH,CO0 四个羧氧 HiY 6Y2 —CH,一CH N 四元酸 +2H 六元酸 HOOCH,C CH>COOH 双极离子 H6Y2+ 四元酸 +2H 六元酸 “EDTA” > EDTA的物理性质:H,Y2+ 0 水中溶解度小,难溶于酸和有机溶剂; 易溶于NaOH或NH,溶液一Na2H2Y2H,0,pH=4.5 龙边理2大舞 CHANGSHA UNIVERSITY OF SCIENCE TECHNOLOGY
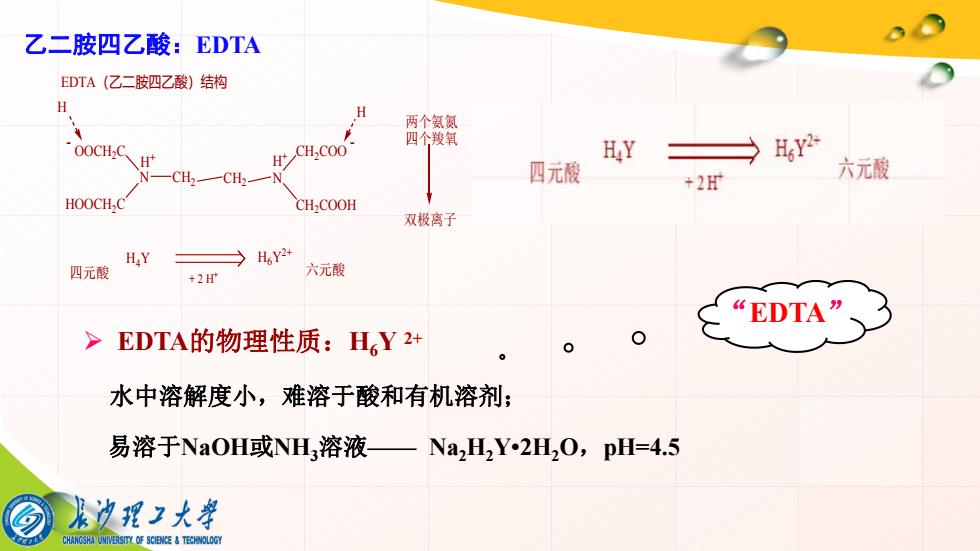
乙二胺四乙酸:EDTA Ø EDTA的物理性质:H6Y 2+ 水中溶解度小,难溶于酸和有机溶剂; 易溶于NaOH或NH3溶液—— Na2H2Y•2H2O,pH=4.5 “EDTA” N CH2 CH2 N CH2COOH CH2COO - H + H + HOOCH2C - OOCH2C H H EDTA(乙二胺四乙酸)结构 H4Y H6Y 2+ + 2 H 四元酸 + 六元酸 两个氨氮 四个羧氧 双极离子

胺羧试剂的特点: a.配位能力强;反应速度快,无色的金属离子与EDTA 反应生成无色配合物; b.多元弱酸;EDTA可获得两个质子,生成六元弱酸; c.与大多数金属离子1:1配位,计算方便; M+Y ±MY d.与金属离子能形成多个多元环,配合物的稳定性高; lgK稳=10.69(CaY) 右图为NiY结构 最冲理2大举 CHANGSHA UNIVERSITY OF SCENCE TECHNOLOG
胺羧试剂的特点: a. 配位能力强;反应速度快,无色的金属离子与EDTA 反应生成无色配合物; b. 多元弱酸;EDTA可获得两个质子,生成六元弱酸; c.与大多数金属离子1∶ 1配位, 计算方便; d. 与金属离子能形成多个多元环,配合物的稳定性高; lgK稳=10.69(CaY) 右图为 NiY 结构

问题二: EDTA是二钠盐,为什么pH值 等于4.5,在酸性范围?
问题二: EDTA是二钠盐,为什么pH值 等于4.5,在酸性范围?

乙二胺四乙酸:EDTA >EDTA的离解平衡: H,Y2+产Ht+HYt √水溶液中七种存在型体 HsY+ H++HY HY H++H Y- √各型体浓度取决于溶液pH值 HY. H+H,Y2- pH<1强酸性溶液→H,Y2+ H2Y2.= H+HY3- HY3. H++Y4 pH2.67~6.16→主要H2Y2 EDTA各种存在形式在不同pH时的分布曲线 pH>10.26碱性溶液→Y4 1 .9 H.Y2 HY 最佳配位型体 M+Y MY 123456789101112 张边理2大¥ pH 高等化登教号骑店。 ©0⊙-8-@ CHANGSHA UNIVERSITY OF SCIENCE TECHNOLOGY
Ø EDTA的离解平衡: ü 各型体浓度取决于溶液pH值 pH < 1 强酸性溶液 → H6Y2+ pH 2.67~6.16 → 主要H2Y2- pH > 10.26 碱性溶液 → Y4- H6Y2+ H+ + H5Y+ H5Y+ H+ + H4Y H4Y H+ + H3Y- H3Y- H+ + H2Y2- H2Y2- H+ + HY3- HY3- H+ + Y4- ü 水溶液中七种存在型体 乙二胺四乙酸:EDTA 最佳配位型体

问题三: MgY;Cu(NH3) 金属离子和配合剂是如何进行配合的呢? 平衡常数(稳定常数)的重要性: 飞稳 Kai Kbi Kw
问题三: 平衡常数(稳定常数)的重要性: K稳; Ka;Kb;Kw MgY; Cu(NH3) 4 金属离子和配合剂是如何进行配合的呢?