(①LDA,THF,.-78C 9 CHa(CH24 COCH(②CHI CH3(CH2)3CHCOCH3 CH3 5.环酮的氧化 CH3 0 0 CF3COOH HNaOH,CzHsOH CHCH(CH24COH OH 练习 cH,o-〈○cHo·-cH0○cHcN CH3O CHCO2H OH HOCH2(CH2)4COOH HOCH2(CH2)4COOC2H5
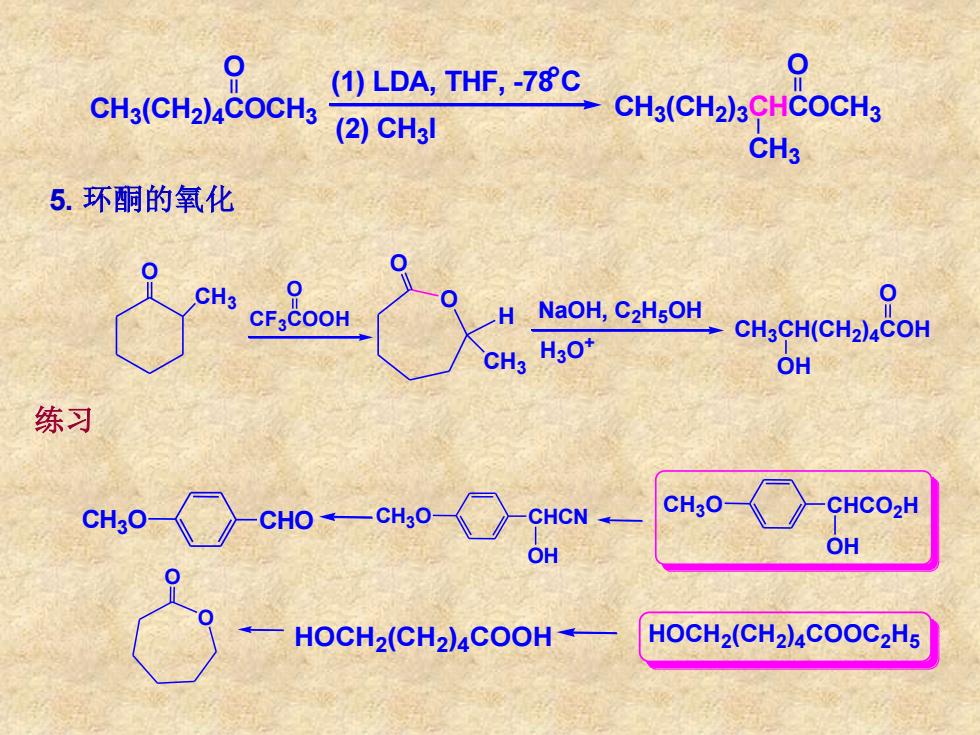
5. 环酮的氧化 O CH3 CF3COOH O CH3O CHCN OH CH3O CHO HOCH2(CH2) 4 COOH O O CH3(CH2) 4 COCH3 O (1) LDA, THF, -78°C (2) CH3I CH3(CH2) 3 CHCOCH3 O CH3 O O H CH3 NaOH, C2H5OH H3O + CH3CH(CH2) 4COH OH O CH3O CHCO2H OH HOCH2(CH2) 4 COOC2 H5 练习
二.醇酸的性质和反应 1.酸性:醇酸含有羟基和羧基两种官能团,由于羟基具有吸电子效 应并能生成氢键,醇酸的酸性较母体羧酸强,水溶性也较大。羟基 离羧基越近,其酸性越强。 CH3CH2COOH CH3CHCOOH CH2CH2COOH OH OH pKa: 4.86 3.87 4.51 2.脱水反应 1).-醇酸:两分子相互酯化,生成六元环交酯 CH3CHOH HO-C=0 o-c-OH HGH-0-C=0+2H0 HO-CHCH3 O-c-o-CHCH3
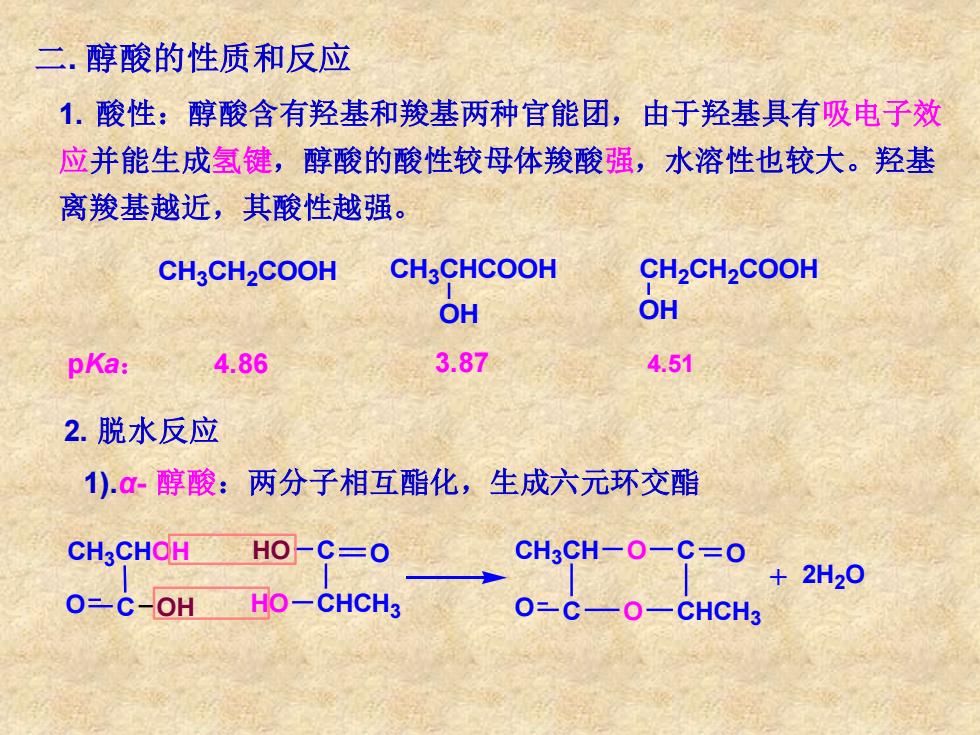
二. 醇酸的性质和反应 1. 酸性:醇酸含有羟基和羧基两种官能团,由于羟基具有吸电子效 应并能生成氢键,醇酸的酸性较母体羧酸强,水溶性也较大。羟基 离羧基越近,其酸性越强。 CH3 CH2 COOH CH3 CHCOOH OH CH2 CH2 COOH OH pKa: 4.86 3.87 4.51 2. 脱水反应 1).α- 醇酸:两分子相互酯化,生成六元环交酯 CH3 CHOH O C OH HO C O HO CHCH3 CH3 CH O C O O C O CHCH3 + 2H2 O