
诱导力 诱导力的大小与固有偶极和被诱导变形的分子 的极化率有关。 1.固有偶极越大,诱导能力越强,诱导力越大。 2.极化率越大,分子越易变形,诱导力越大
诱导力 诱导力的大小与固有偶极和被诱导变形的分子 的极化率有关。 1.固有偶极越大,诱导能力越强,诱导力越大。 2.极化率越大,分子越易变形,诱导力越大

分子间力的特点 1.是存在于分子之间的电性作用力。 2.比化学键(100-600kJmo1)小1-2个数量级,仅 几至几十kJmo1。 3.短程力,作用范围仅几百pm。 4.不具方向性和饱和性。 5.诱导力都很小,多数分子之间力以色散力为主,另 有极性很强的分子(H2O、NHL3等),取向力才占较 大比例。 6.分子间力越大,熔点(m.p.)、沸点(b.p.)越大
分子间力的特点 1.是存在于分子之间的电性作用力。 2. 比化学键(100-600kJ•mol-1)小1-2个数量级, 仅 几至几十kJ•mol-1 。 3.短程力,作用范围仅几百pm。 4.不具方向性和饱和性。 5.诱导力都很小,多数分子之间力以色散力为主,另 有极性很强的分子(H2O、NH3等),取向力才占较 大比例。 6.分子间力越大,熔点(m.p.)、沸点(b.p.)越大

分析三种情况的分子间力 1.非极性分子与非极性分子之间 2.非极性分子与极性分子之间 3.极性分子与极性分子之间
分析三种情况的分子间力 1.非极性分子与非极性分子之间 2.非极性分子与极性分子之间 3.极性分子与极性分子之间
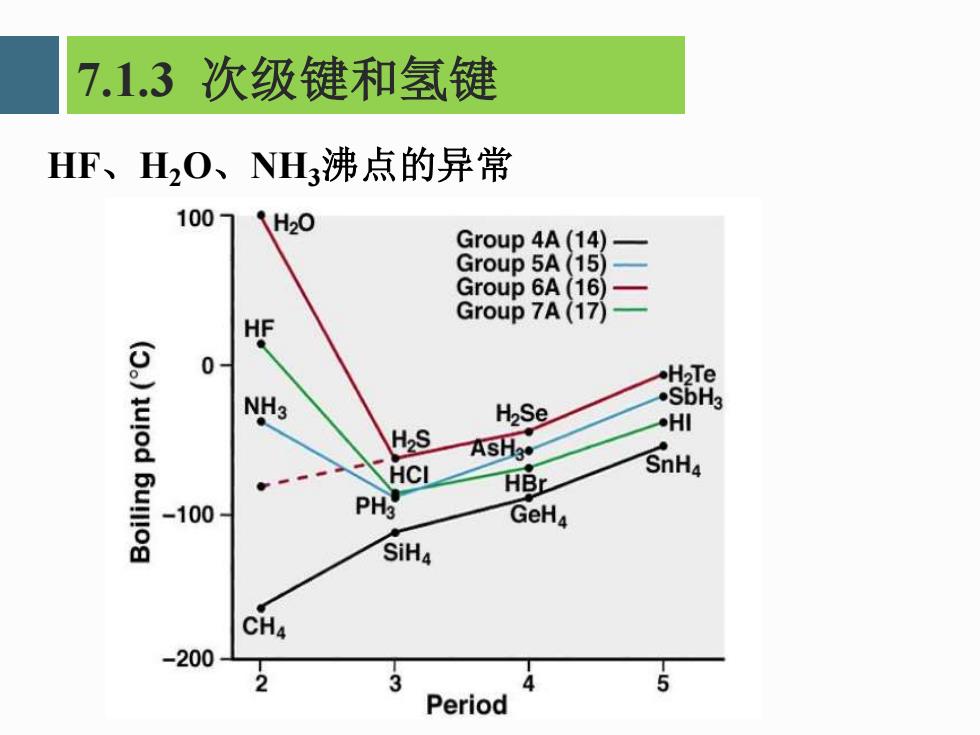
7.1.3次级键和氢键 HF、H2O、NH3沸点的异常 100 1H20 Group 4A(14) Group 5A(15) Group 6A(16) HF Group 7A(17)- 0- H2Te NH3 .SbH3 H2Se HI H2S ASHo HCL HBr SnH4 -100 PHg GeHa SiHa CH4 -200 2 3 5 Period
7.1.3 次级键和氢键 HF、H2O、NH3沸点的异常

氢键 由于氢原子和电负性大的X原子(如F、O、N 等)以共价键结合后,其电子云强烈偏向氟、氧、 氮原子,使氢原子几乎赤裸的质子。这个半径很小、 且带有正电荷的氢原子与另一个分子中含有孤对电 子对并带有部分负电荷的、电负性大的Y原子充分 靠近而产生的吸引力,称为氢键。 H A H H-O-H-O H-N-H-N H-O-H-N H H H H H H H H H -0 H-F-H-N H H H
氢键 由于氢原子和电负性大的X原子(如F、O、N 等)以共价键结合后,其电子云强烈偏向氟、氧、 氮原子,使氢原子几乎赤裸的质子。这个半径很小、 且带有正电荷的氢原子与另一个分子中含有孤对电 子对并带有部分负电荷的、电负性大的Y原子充分 靠近而产生的吸引力,称为氢键