氢化物(AH),A=Lit、Nat、Kt、Rut、Cst...;氧化物(AO),A=Sr2+、Ba2+、Ca2+、Ti2+、Sn2+、Pb2+..硫化物(AS),A=Pb2t、Ca2+、Mn2+、Ba2+、Mg2+..;硒化物(ASe),A=Pb2+、Ca2+、Mn2、Ba2+、Mg2+;碲化物(ATe),A=Ca2+、Sr2+、Ba2+、Ti.碳化物(AC),A=Ti、Zr、Hf、V、Nb、Ta、Th...;氮化物(AN),A=Sc、Y、Ti、Zr、V、Nb、Cr、Np、Pu、Th、U...;过渡金属元素的氧化物。(2)氯化(CsCI)型结构等轴晶系,空间群Oh-Pm3m,a=0.4110nm,Z=1。结构如图10-9所示。CsCI结构可以看成是由CI的立方原始点阵和Cs的立方原始点阵套叠而成,一套点阵位于另一套点阵的立方晶胞的中心,两种离子的配位数CN均为8。即如果原始点选在CI的中心,相当点位于立方晶胞的8个角顶,Cs位于晶胞体心:如果原?Cl-Os●Zn图10-9CsC1晶体结构图10-10闪锌矿(立方硫化锌)晶体结构始点选在Cs的中心,则相当点也位于立方晶胞的8个角顶,CI位于晶胞体心。等效点的坐标为CI:0,0,0:Cs:1/2,1/2,1/2。当AX型化合物中r/r>0.732时多为CsCI型结构。属于这种结构型的有CsBr、Csl、RbCl、ThCI、ThTe、TICl、TIBr、NH,CI、NH,Br、NHI等。在后三种晶体中,NH可看作是一个简单的阳离子。(3)闪锌矿(α-ZnS)型结构等轴晶系,空间群为T-F43m,a。=0.540nm,Z=4。图10-10所示为它的一个晶胞,S位于立方晶胞的8个角顶和每一个面的面心,若把单位晶胞分成8个小立方体,Zn2+占据其中相间四个的中心位置;闪锌矿结构也可以看成是s2-作立方最紧密堆积,Zn充填1/2的四面体空隙。结构与金刚石非常相似,将Zn、S换成C即为金刚石结构。2-和Zn2+各占据一组特殊等效位置,等效点的坐标为4s2:0,0,0;1/2,1/2,0;1/2,0,1/2:0,1/2,1/2;4Zn2+:1/4,1/4,1/43/4,3/4,168
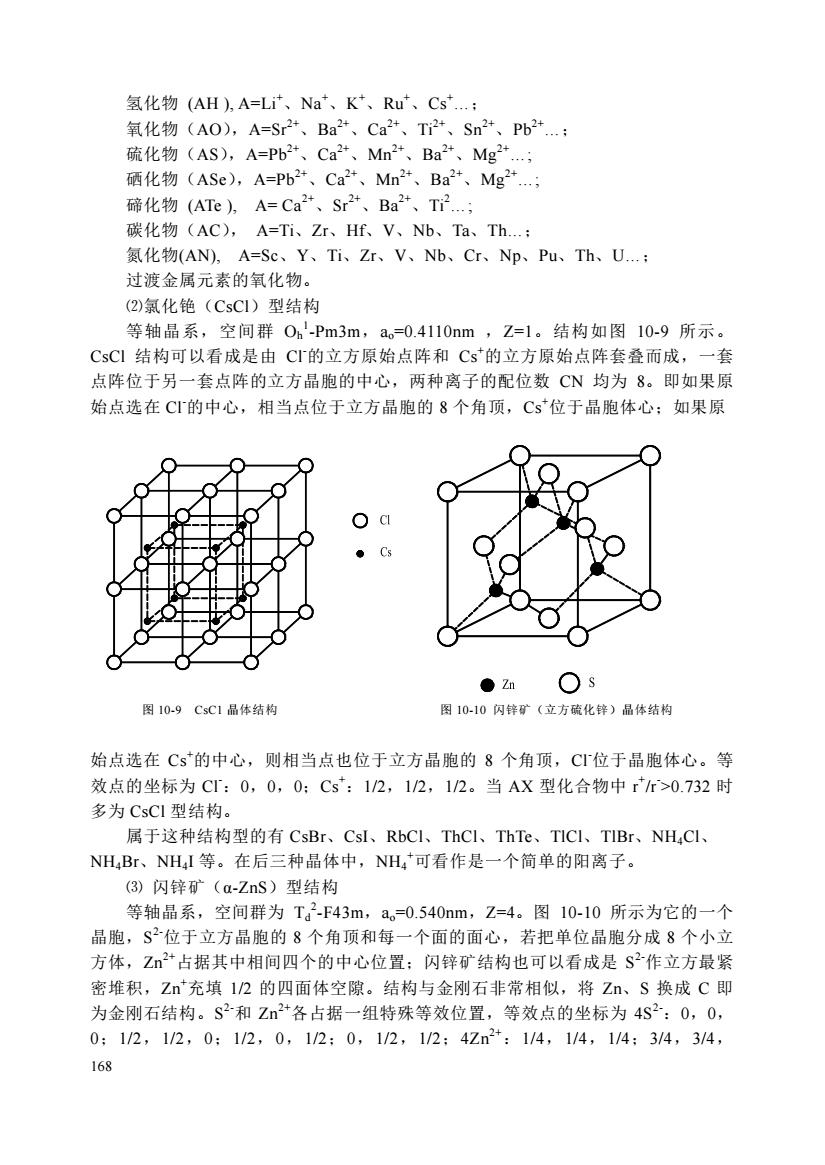
168 氢化物 (AH ), A=Li+、Na+、K +、Ru+、Cs+.; 氧化物(AO),A=Sr2+、Ba2+、Ca2+、Ti2+、Sn2+、Pb2+.; 硫化物(AS),A=Pb2+、Ca2+、Mn2+、Ba2+、Mg2+ .; 硒化物(ASe),A=Pb2+、Ca2+、Mn2+、Ba2+、Mg2+ .; 碲化物 (ATe ), A= Ca2+、Sr2+、Ba2+、Ti2 .; 碳化物(AC), A=Ti、Zr、Hf、V、Nb、Ta、Th.; 氮化物(AN), A=Sc、Y、Ti、Zr、V、Nb、Cr、Np、Pu、Th、U.; 过渡金属元素的氧化物。 ⑵氯化铯(CsCl)型结构 等轴晶系,空间群 Oh 1 -Pm3m,ao=0.4110nm ,Z=1。结构如图 10-9 所示。 CsCl 结构可以看成是由 Cl-的立方原始点阵和 Cs+的立方原始点阵套叠而成,一套 点阵位于另一套点阵的立方晶胞的中心,两种离子的配位数 CN 均为 8。即如果原 始点选在 Cl-的中心,相当点位于立方晶胞的 8 个角顶,Cs+位于晶胞体心;如果原 图 10-9 CsC1 晶体结构 图 10-10 闪锌矿(立方硫化锌)晶体结构 始点选在 Cs+的中心,则相当点也位于立方晶胞的 8 个角顶,Cl-位于晶胞体心。等 效点的坐标为 Cl-:0,0,0;Cs+:1/2,1/2,1/2。当 AX 型化合物中 r + /r- >0.732 时 多为 CsCl 型结构。 属于这种结构型的有 CsBr、CsI、RbCl、ThCl、ThTe、TlCl、TlBr、NH4Cl、 NH4Br、NH4I 等。在后三种晶体中,NH4 +可看作是一个简单的阳离子。 ⑶ 闪锌矿(α-ZnS)型结构 等轴晶系,空间群为 Td 2 -F43m,ao=0.540nm,Z=4。图 10-10 所示为它的一个 晶胞,S 2-位于立方晶胞的 8 个角顶和每一个面的面心,若把单位晶胞分成 8 个小立 方体,Zn2+占据其中相间四个的中心位置;闪锌矿结构也可以看成是 S 2-作立方最紧 密堆积,Zn+充填 1/2 的四面体空隙。结构与金刚石非常相似,将 Zn、S 换成 C 即 为金刚石结构。S 2-和 Zn2+各占据一组特殊等效位置,等效点的坐标为 4S2-:0,0, 0;1/2,1/2,0;1/2,0,1/2;0,1/2,1/2;4Zn2+:1/4,1/4,1/4;3/4,3/4

1/4;3/4,1/4,3/4;1/4,3/4,3/4。具有闪锌矿型结构的有CaF、CuCl、CuBr、Cul、BeV、BeS、CdS、HgS、BeSe、BeTe、ZnSe、ZnTe、CdTe、MgTe、AIP、GaP、AlAs、GaAs、AlSb、InSb、BaS、BN、SiC、BeB等。(4)纤锌矿(β-ZnS)型结构纤锌矿是闪锌矿的同质多像变体。六方晶系,空间群是C6v-P63mc,a=0.384nm;c=0.518nm,Z=6。如图10-11所示,结构中s2-成六方紧密堆积,Zn充填半数的四面体空隙。四面体共顶相连,阴阳离子的配位数均为4。若将单位晶胞分成六个相等的三方柱,硫离子位于三方柱的每一个角顶和相间的三方柱的中心,锌离子位于中心有硫离子的三方柱的三条棱的5/8处及中心线的1/8处。等效点的坐标:s2-为0,0,0:2/3,1/3,1/2;Zn2+为0,0,5/8:2/3,1/3,1/8。eZnO图10-11纤锌矿(六方ZnS)的品体结构2.AX,型化合物的晶体结构主要包括氧化物和氟化物等,典型的结构有两种:萤石(CaF2)型和金红石型。(1)萤石(CaF,)型结构萤石(又称氟石),等轴晶系,空间群O,-Fm3m,a。=0.545nm,Z=4。F为四面体配位,CN=4:Ca2为立方体配位,CN=8。或可以看成Ca2成立方紧密堆积,氟离子充填所有四面体空隙。图10-12所示为一个晶胞,Ca2离子位于立方面心格子的八个角顶和每一个面的中心,F位于单位晶胞所等分的八个小立方体的中心。等效点的坐标4Ca2+是0,0,0:1/2,1/2,0:1/2,0,1/2;0,1/2,1/2;8F为1/4,1/4,1/4;3/4,3/4,1/4;3/4,1/4,3/4;1/4,3/4,3/4;3/4,3/4,3/4;1/4,1/4,3/4;1/4,3/4,1/4;3/4,1/4,1/4。董石型结构的稳定范围为r/r>0.732。具有萤石型结构的晶体见表10-1。在萤石的晶体结构中,111!面网的面网间距虽非最大,但是在这个方向上存在着互相毗邻的同号负离子层,相互之间存在着静电斥力,致使晶体具有平行(111)的八面体的完全解理。天然萤石用作为生产玻璃的助熔剂、制取氢氟酸和提取氟的原料:人造萤石单晶体可作为红外和激光仪器的光学元件。169
169 1/4;3/4,1/4,3/4;1/4,3/4,3/4。 具有闪锌矿型结构的有 CaF、CuCl、CuBr、CuI、BeV、BeS、CdS、HgS、 BeSe、 BeTe 、 ZnSe 、 ZnTe、 CdTe、 MgTe、 AlP 、 GaP 、 AlAs、 GaAs、 AlSb 、 InSb、BaS、BN、SiC、BeB 等。 ⑷ 纤锌矿(β-ZnS)型结构 纤锌矿是闪锌矿的同质多像变体。六方晶系,空间群是 C6v 4 -P63mc , ao=0.384nm;co=0.518nm,Z=6。如图 10-11 所示,结构中 S 2-成六方紧密堆积, Zn2+充填半数的四面体空隙。四面体共顶相连,阴阳离子的配位数均为 4。若将单 位晶胞分成六个相等的三方柱,硫离子位于三方柱的每一个角顶和相间的三方柱的 中心,锌离子位于中心有硫离子的三方柱的三条棱的 5/8 处及中心线的 1/8 处。等 效点的坐标:S 2-为 0,0,0;2/3,1/3,1/2;Zn2+为 0,0,5/8;2/3,1/3,1/8。 图 10-11 纤锌矿(六方 ZnS)的晶体结构 ⒉ AX2 型化合物的晶体结构 主要包括氧化物和氟化物等,典型的结构有两种:萤石(CaF2)型和金红石 型。 ⑴ 萤石(CaF2)型结构 萤石(又称氟石),等轴晶系,空间群 Oh 5 -Fm3m,ao=0.545nm,Z=4。F -为四 面体配位,CN=4;Ca2+为立方体配位,CN=8。或可以看成 Ca2+成立方紧密堆积, 氟离子充填所有四面体空隙。图 10-12 所示为一个晶胞,Ca2+离子位于立方面心格 子的八个角顶和每一个面的中心,F -位于单位晶胞所等分的八个小立方体的中心。 等效点的坐标 4Ca2+是 0,0,0;1/2,1/2,0;1/2,0,1/2;0,1/2,1/2;8F-为 1/4,1/4,1/4;3/4,3/4,1/4;3/4,1/4,3/4;1/4,3/4,3/4;3/4,3/4,3/4; 1/4,1/4,3/4;1/4,3/4,1/4;3/4,1/4,1/4。 萤石型结构的稳定范围为 r + /r- >0.732。具有萤石型结构的晶体见表 10-1。 在萤石的晶体结构中,{111}面网的面网间距虽非最大,但是在这个方向上存 在着互相毗邻的同号负离子层,相互之间存在着静电斥力,致使晶体具有平行{111} 的八面体的完全解理。天然萤石用作为生产玻璃的助熔剂、制取氢氟酸和提取氟的 原料;人造萤石单晶体可作为红外和激光仪器的光学元件

0.1L2011O1411200,1$1/2O4O111/20.0, 1CaOF图10-12萤石结构(a)及其在(001)面上投影将CaF,中的阴阳离子位置颠倒,即得反董石型结构AX,阴阳离子的分布与萤石型结构正好相反,即当萤石型晶格中阳离子的位置上分布着阴离子,而原阴离子的位置上分布着阳离子,即构成反董石型晶格。阳离子的配位数为4,阴离子的配位数为8。具有反董石型结构的晶体主要是碱金属的氧化物、硫化物、硒化物、碲化物等。由于碱金属氧化物等的键力较弱,因此这类晶体的熔点都比较低,且晶胞越大熔点越低。(2)金红石(TiO2)型结构00b图10-13金红石的晶体结构170
170 图 10-12 萤石结构(a)及其在(001)面上投影 将 CaF2 中的阴阳离子位置颠倒,即得反萤石型结构 A2X,阴阳离子的分布与 萤石型结构正好相反,即当萤石型晶格中阳离子的位置上分布着阴离子,而原阴离 子的位置上分布着阳离子,即构成反萤石型晶格。阳离子的配位数为 4,阴离子的 配位数为 8。 具有反萤石型结构的晶体主要是碱金属的氧化物、硫化物、硒化物、碲化物 等。由于碱金属氧化物等的键力较弱,因此这类晶体的熔点都比较低,且晶胞越大 熔点越低。 ⑵ 金红石(TiO2)型结构 a b 图 10-13 金红石的晶体结构

四方晶系,空间群D4hl4-P42/mnm,a。=0.4594nm,c。=0.2959nm,Z=2。结构中氧离子成扭曲的六方紧密堆积,平面三角形配位,CN=3:钛离子位于半数的八面体空隙中,构成[TiO6]八面体配位,CN=6。图10-13a所示为一个晶胞,钛离子位于单位晶胞的角顶和体心,六个氧离子中有四个位于单位晶胞的上、下底面上,另外两个位于单位晶胞内。结构中[TiOl八面体共棱连接成平行c轴的链,链间通过共用[TiO6]八面体的角顶连接,其晶胞参数c。值恰好为[TiO6]八面体的棱长(图10-13b)。等效点的坐标为2Ti4是0,0,0;1/2,1/2,1/2;40是u,u,0;1-u,1-u,01/2+u,1/2+u,1/2:1/2-u,1/2+u,1/2。在金红石的晶格中u=0.31。金红石形结构的稳定范围是r/=0.732一0.380。金红石晶体具有很高的折射率和介电常数,常被用来作为陶瓷铀原料,也是无线电陶瓷的主要晶相之一。金红石型钛白粉和云母钛珠光颜料具有良好的耐侯性、化学稳定性及光学性能。属于金红石形结构的晶体见表10-1。表10-1具有CaFz型与TiO,型结构的AX,型化合物CaF2型TiO2型r*/r>0.732r*/r=0.732~0.380.990.720.590.60BaF2CeO2MnF2PbO2PbF20.88ThO20.68FeF20.59SnO20.51SrF20.660.590.490.83PrO2PdF2TiO20.65(BaCl2)(0.75)PbO2(CaCl2)(0.55)WO20.470.640.54CaF2ZnF20.46(0.73)UO2Os020.63(SrCl2)0.71NpO2CoF20.53Ir020.46PuO20.62NiF20.51RuO20.45(0.63)0.61VO20.43AmO2(CaBr2)(0.51)ZrO20.570.48CrO20.40MgF2HrO20.56MnO20.39GeO20.38(3)SiO2型结构SiO,中Si的4个sp3杂化轨道分别与4个O的p轨道形成4个键,构成[SiO4]四面体,四面体之间共角顶连接,Si的配位数CN=4,O的配位数CN=2。[SiO4]四面体的具体连接方式不同,会使晶体结构的对称性发生变化,形成不同的变体。SiO,有一系列同质多像变体,这些变体的形态和物理性质也有差异。α-石英为唯一使用的压电晶体,熔点为1750℃C,莫氏硬度为7。空间群D3P3,2(左形)或D,4-P322(右形),a。=0.4904nm,c。=0.5397nm。晶体在(0001)面上的投影如图10-14所示。171
171 四方晶系,空间群 D4h 14 -P42/mnm,ao=0.4594nm,co=0.2959nm ,Z=2。结构中 氧离子成扭曲的六方紧密堆积,平面三角形配位,CN=3;钛离子位于半数的八面 体空隙中,构成[TiO6]八面体配位,CN=6。图 10-13a 所示为一个晶胞,钛离子位于 单位晶胞的角顶和体心,六个氧离子中有四个位于单位晶胞的上、下底面上,另外 两个位于单位晶胞内。结构中[TiO6]八面体共棱连接成平行 c 轴的链,链间通过共 用[TiO6]八面体的角顶连接,其晶胞参数 co 值恰好为[TiO6]八面体的棱长(图 10- 13b)。等效点的坐标为 2Ti4+是 0,0,0;1/2,1/2,1/2;4O2-是 u,u,0;1-u,1- u,0;1/2+u,1/2+u,1/2;1/2-u,1/2+u,1/2。在金红石的晶格中 u=0.31。 金红石形结构的稳定范围是 r + /r- =0.732-0.380。 金红石晶体具有很高的折射率和介电常数,常被用来作为陶瓷铀原料,也是无 线电陶瓷的主要晶相之一。金红石型钛白粉和云母钛珠光颜料具有良好的耐侯性、 化学稳定性及光学性能。 属于金红石形结构的晶体见表 10-1。 表 10-1 具有 CaF2 型与 TiO2 型结构的 AX2 型化合物 CaF2 型 r + /r- >0.732 TiO2 型 r + /r- =0.732~0.38 BaF2 PbF2 SrF2 (BaCl2 ) CaF2 (SrCl2 ) 0.99 0.88 0.83 (0.75) (0.73) 0.71 (0.63) CeO2 ThO2 PrO2 PbO2 UO2 NpO2 PuO2 AmO2 ZrO2 HrO2 0.72 0.68 0.66 0.65 0.64 0.63 0.62 0.61 0.57 0.56 MnF2 FeF2 PdF2 (CaCl2 ) ZnF2 CoF2 NiF2 (CaBr2 ) MgF2 0.59 0.59 0.59 (0.55) 0.54 0.53 0.51 (0.51) 0.48 PbO2 SnO2 TiO2 WO2 OsO2 IrO2 RuO2 VO2 CrO2 MnO2 GeO2 0.60 0.51 0.49 0.47 0.46 0.46 0.45 0.43 0.40 0.39 0.38 ⑶ SiO2 型结构 SiO2 中 Si 的 4 个 sp 3 杂化轨道分别与 4 个 O 的 p 轨道形成 4 个 σ 键,构成 [SiO4]四面体,四面体之间共角顶连接,Si 的配位数 CN=4,O 的配位数 CN=2。 [SiO4]四面体的具体连接方式不同,会使晶体结构的对称性发生变化,形成不同的 变体。SiO2 有一系列同质多像变体,这些变体的形态和物理性质也有差异。 α-石英为唯一使用的压电晶体,熔点为 1750°C,莫氏硬度为 7。空间群 D3 4 - P312(左形)或 D3 4 -P322(右形),ao=0.4904nm,co=0.5397nm。晶体在(0001)面 上的投影如图 10-14 所示

当温度高于573°C时,α-石英变成β-石英。β-石英的空间群为D。-P642。对称性高于α-石英。β-石英在(0001)面上的投影见图10-15。当温度高于870C时,β-石英变为鳞石英(图10-16)。温度继续升高,鳞石英变为方英石。鳞石英与方英石的结构见图10-16。Osi原子在OCo高度si原子在2/3Ce高度●si原子在1/3Co高度图10-14a-石英晶体结构在(0001)面上的投影图0Osi原子在OCo高度si原子在2/3Co高度si原子在1/3Co高度图10-15β-石英晶体结构在(0001)面上的投影图172
172 当温度高于 573°C 时,α-石英变成 β-石英。β-石英的空间群为 D6 4 -P642。对称 性高于 α-石英。β-石英在(0001)面上的投影见图 10-15。 当温度高于 870°C 时,β-石英变为鳞石英(图 10-16)。温度继续升高,鳞石英 变为方英石。鳞石英与方英石的结构见图 10-16。 ○ si 原子在 0C0 高度 si 原子在 2/3C0 高度 ● si 原子在 1/3C0 高度 图 10-14 a-石英晶体结构在(0001)面上的投影图 ○ si 原子在 0C0 高度 si 原子在 2/3C0 高度 ●si 原子在 1/3C0 高度 图 10-15 β-石英晶体结构在(0001)面上的投影图