
2.3.2路易斯结构式 1.按原子的键合关系写出元素符号并将相邻原子用单 键连接。在大多数情况下,原子间的键合关系是已知 的,例如,NO,中的键合关系不是N一O一O,而是O N-O。 2.将各原子的价电子数相加,算出可供利用的价电子总 数。如果被表达的物种带有电荷,则价电子总数应减 去正、负电荷数。 3.扣除与共价单键相应的电子数(单键数×2)后,将 剩余的价电子分配给每个原子,使其占有适当数目 的非键合电子。 4.如果剩余的电子不够安排,可将一些单键改为双键 或叁键。 上页 下页 目录返回
上页 下页 目录 返回 2.3.2 路易斯结构式 1. 按原子的键合关系写出元素符号并将相邻原子用单 键连接。在大多数情况下,原子间的键合关系是已知 的, 例如, NO2中的键合关系不是N—O—O, 而是O— N—O。 2. 将各原子的价电子数相加, 算出可供利用的价电子总 数。如果被表达的物种带有电荷, 则价电子总数应减 去正、负电荷数。 3. 扣除与共价单键相应的电子数(单键数×2)后,将 剩余的价电子分配给每个原子, 使其占有适当数目 的非键合电子。 4. 如果剩余的电子不够安排,可将一些单键改为双键 或叁键
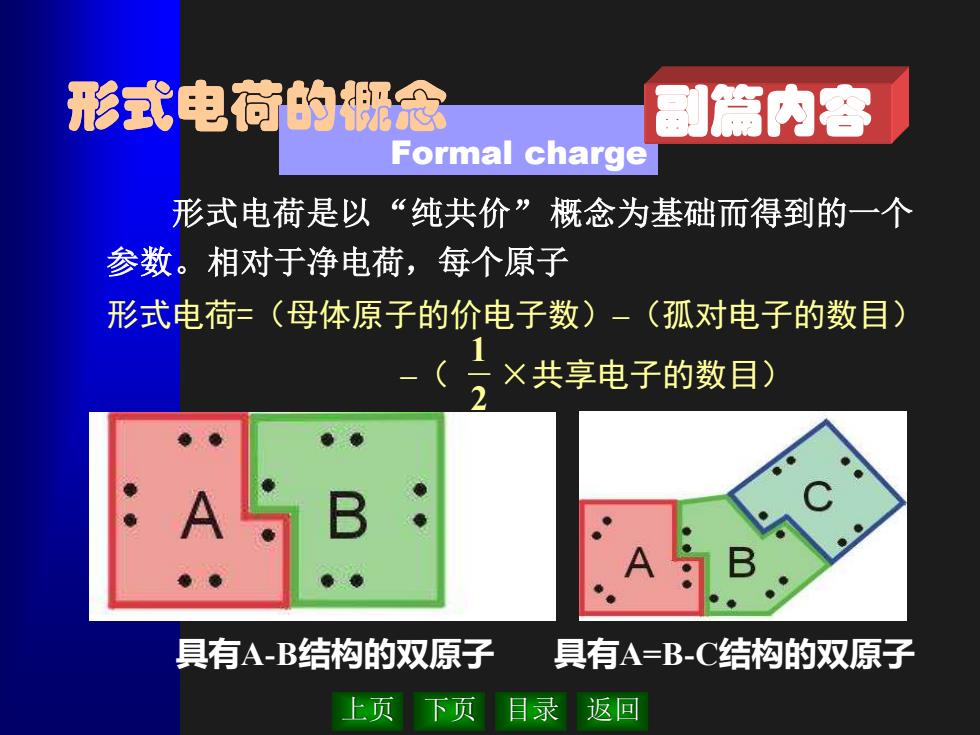
形式电荷的概念 副篇内容 Formal charge 形式电荷是以“纯共价”概念为基础而得到的一个 参数。相对于净电荷,每个原子 形式电荷=(母体原子的价电子数)一(孤对电子的数目) ×共享电子的数目) 具有A-B结构的双原子 具有A=B-C结构的双原子 上页 下页 目录 返回
上页 下页 目录 返回 形式电荷的概念 Formal charge 形式电荷是以“纯共价”概念为基础而得到的一个 参数。相对于净电荷,每个原子 具有A-B结构的双原子 具有A=B-C结构的双原子 形式电荷=(母体原子的价电子数)–(孤对电子的数目) –( ×共享电子的数目) 2 1 副篇内容

Que 3 写出氯酸根离子C10的路易斯 结构式。 Solution C原子的电负性小于0原子,意味着不存在0-0 之间的键合.合理的排布应该如下所示: CI03离子中价电子总数等于26,扣除3个单键的6 个电子,余下的20个电子以孤对方式分配给四个原子,使 它们均满足八隅律的要求。 上页 下页 目录 返回
上页 下页 目录 返回 写出氯酸根离子 的路易斯 结构式。 Cl 原子的电负性小于 O 原子,意味着不存在 O-O 之间的键合. 合理的排布应该如下所示: Cl O O O Cl O O O Question 3 Solution − ClO3 离子中价电子总数等于26,扣除3个单键的6 个电子,余下的20个电子以孤对方式分配给四个原子, 使 它们均满足八隅律的要求。 − ClO3

Que 4 写出NO离子的路易斯结构式。 Solution NO离子只可能有一种排布方式,见下图最左边一个: N-0 N-+=0+N=可 N三0:+ NO+离子中价电子总数等于10,扣除1个单键的2 个电子,余下的8个电子无论按上图中第二个那样以 孤对方式分配给两个原子,还是按上图中第三或第四个 那样将N~O单键改为双键,都不能使两个原子同时满 足八隅律的要求。这一要求只有将单键改为叁键才能满 足。 上页 页 目录 返回
上页 下页 目录 返回 写出 NO+ 离子的路易斯结构式。 NO+ 离子只可能有一种排布方式,见下图最左边一个: NO+离子中价电子总数等于10 ,扣除 1 个单键的 2 个电子, 余下的 8 个电子无论按上图中第二个那样以 孤对方式分配给两个原子,还是按上图中第三或第四个 那样将 N-O 单键改为双键,都不能使两个原子同时满 足八隅律的要求。这一要求只有将单键改为叁键才能满 足。 N O N O + + N O + N O + N O Question 4 Solution
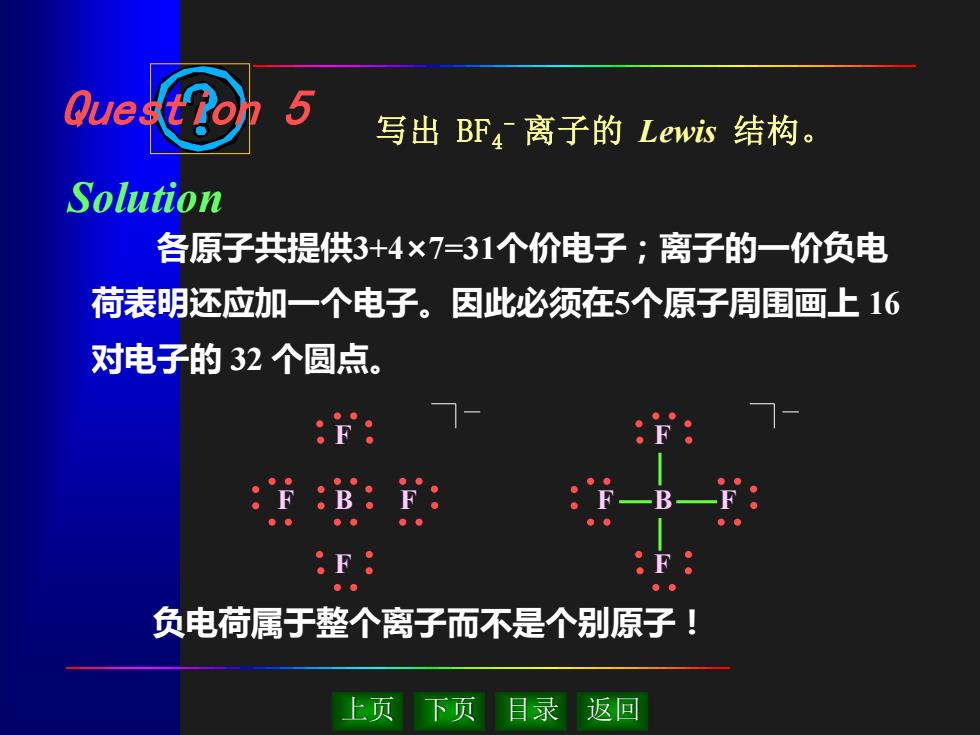
Que 写出BF4离子的Lewi心结构。 Solution 各原子共提供3+4×7=31个价电子;离子的一价负电 荷表明还应加一个电子。因此必须在5个原子周围画上16 对电子的32个圆点。 :F: 负电荷属于整个离子而不是个别原子! 上页下页 目录返回
上页 下页 目录 返回 各原子共提供3+4×7=31个价电子;离子的一价负电 荷表明还应加一个电子。因此必须在5个原子周围画上 16 对电子的 32 个圆点。 负电荷属于整个离子而不是个别原子! 写出 BF4 - 离子的 Lewis 结构。 F F B F F F F B F F Question 5 Solution