
第一章 第二章 -0 第三章 14 第四章 -1只 第五草 第六章一 -44 第七章 52 第八意一 -66 第九章一 -69 第十章一 -72 第一章物质的结构 1-1在自然界中氢有三种同位素,氧也有三种同位素,问:总共有种含不同核素的水分子? 由于太少,可以忽略不计,问:不计H时天然水中共有多少种同位素异构水分子? 1、3×C-9 1-2天然氟是单核素(℉)元素,而天然碳有两种稳定同位素(℃和℃),在质谱仪中, 每一质量数的微粒出现一个峰,氢预言在质谱仪中能出现几个相应于C℉的峰? 2、氢在质谱仪中能出现2个相应于C的峰, 1-3用质谱仪测得溴得两种天然同位素的相对原子质量和同位素丰度分别为Br789183 占50.54%,"Br80.9163占49.46%,求溴的相对原子质量(原子量) 3、溴的相对原子量为: 78×50.54%+80.9163X49.63%-79.9065 1-4铊的天然同位素0T1和T1的核素质量分别为202.97u和204.97u,己知铊的相 对原子质量(原子量)为204.39,求铊的同位素丰度。 4、设203T1的含量为%则205T1的含量为1x 即203T1的含量为30%而205T1的含量为70% 1-5等质量的银制成氯化银和碘化银,测得质量比m(AgC1):m(AgBr)=1.63810:1, 又测得银和氯得相对原子质量(原子量)分别为107.868和35.453,求碘得相对原子 质量(原子量)。 5、设I的相对原子量为x 107.868+35.453 1 1.13279 1-6表1-1中贝采里乌斯1826年测得的铂原子量与现代测定的铂的相对原子质量(原子 量)相比,有多大差别?
1 第一章-1 第二章-9 第三章-14 第四章-18 第五章-28 第六章-44 第七章-52 第八章-66 第九章-69 第十章-72 第一章物质的结构 1-1 在自然界中氢有三种同位素,氧也有三种同位素,问:总共有种含不同核素的水分子? 由于 3 H 太少,可以忽略不计,问:不计 3 H 时天然水中共有多少种同位素异构水分子? 1-2 天然氟是单核素(19F)元素,而天然碳有两种稳定同位素(12C 和 13C),在质谱仪中, 每一质量数的微粒出现一个峰,氢预言在质谱仪中能出现几个相应于 CF4 +的峰? 1-3 用质谱仪测得溴得两种天然同位素的相对原子质量和同位素丰度分别为 79Br 789183 占 50。54%, 81Br 80。9163 占 49。46%,求溴的相对原子质量(原子量)。 1-4 铊的天然同位素 203Tl 和 205Tl 的核素质量分别为 202。97u 和 204。97u,已知铊的相 对原子质量(原子量)为 204。39,求铊的同位素丰度。 1-5 等质量的银制成氯化银和碘化银,测得质量比 m(AgCl):m(AgBr)=1。63810:1, 又测得银和氯得相对原子质量(原子量)分别为 107。868 和 35。453,求碘得相对原子 质量(原子量)。 1-6 表 1-1 中贝采里乌斯 1826 年测得的铂原子量与现代测定的铂的相对原子质量(原子 量)相比,有多大差别?
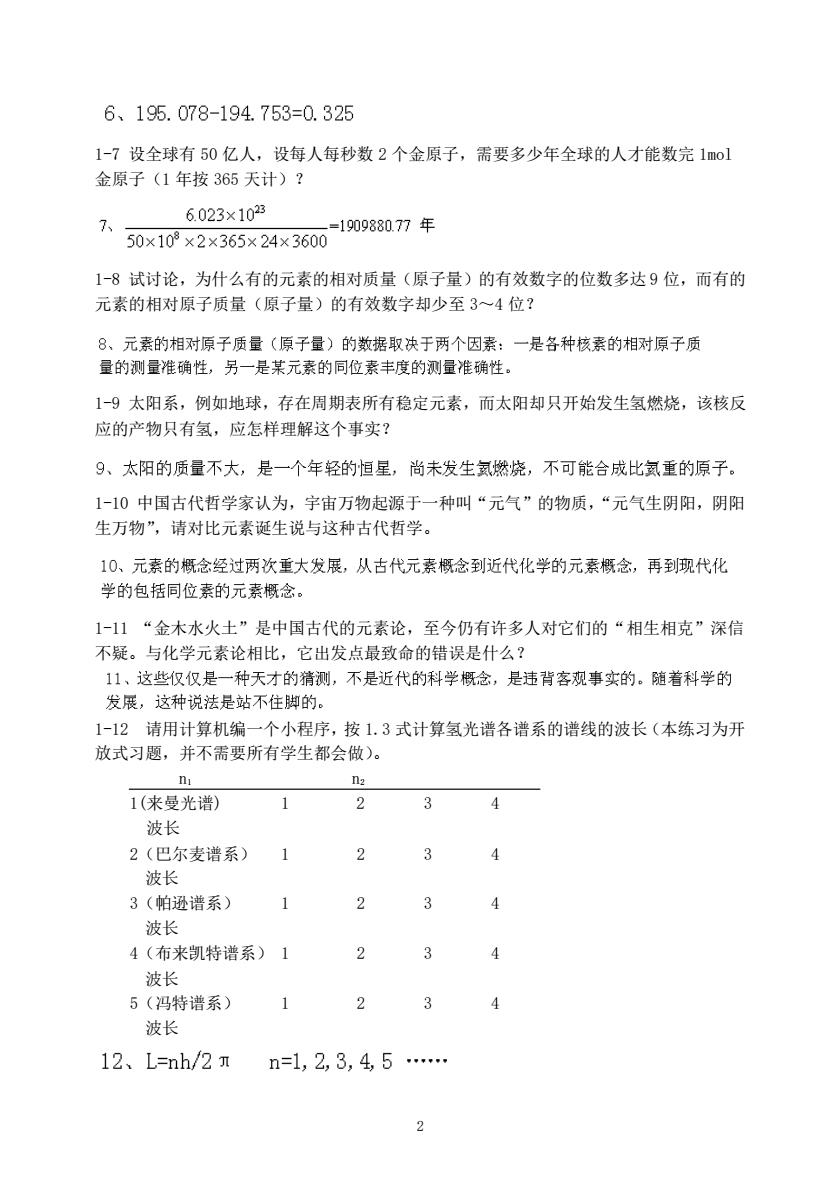
6、195.078-194753=0.325 1-7设全球有50亿人,设每人每秒数2个金原子,需要多少年全球的人才能数完1mol 金原子(1年按365天计)? 6.023×1023 150x10<2×365x24x360109807年 1-8试讨论,为什么有的元素的相对质量(原子量)的有效数字的位数多达9位,而有的 元素的相对原子质量(原子量)的有效数字却少至3~4位? 8、元素的相对原子质量(原子量)的数据取决于两个因素:一是各种核素的相对原子质 量的测量准确性,另一是某元素的同位素丰度的测量准确性。 19太阳系,例如地球,存在周期表所有稳定元素,而太阳却只开始发生氢燃烧,该核反 应的产物只有氢,应怎样理解这个事实? 9、太阳的质量不大,是一个年轻的恒星,尚未发生氨燃烧,不可能合成比氨重的原子。 1-10中国古代哲学家认为,宇宙万物起源于一种叫“元气”的物质,“元气生阴阳,阴阳 生万物”,请对比元素诞生说与这种古代哲学。 10、元素的概念经过两次重大发展,从古代元素概念到近代化学的元素概念,再到现代化 学的包括同位素的元素概念。 1-11“金木水火土”是中国古代的元素论,至今仍有许多人对它们的“相生相克”深信 不疑。与化学元素论相比,它出发点最致命的错误是什么? 11、这些仅仅是一种天才的猜测,不是近代的科学概念,是违背客观事实的。随着科学的 发展,这种说法是站不住脚的。 1-12请用计算机编一个小程序,按1.3式计算氢光谱各谱系的谱线的波长(本练习为开 放式习题,并不需要所有学生都会做)。 n n2 1(来曼光谱) 1 2 3 波长 2(巴尔麦谱系) 1 2 3 4 波长 3(帕逊谱系)》 1 波长 4(布来凯特谱系)1 3 波长 5(冯特谱系)》 3 波长 12、L=mh/2Tn=1,2,3,4,5. 2
2 1-7 设全球有 50 亿人,设每人每秒数 2 个金原子,需要多少年全球的人才能数完 1mol 金原子(1 年按 365 天计)? 1-8 试讨论,为什么有的元素的相对质量(原子量)的有效数字的位数多达 9 位,而有的 元素的相对原子质量(原子量)的有效数字却少至 3~4 位? 1-9 太阳系,例如地球,存在周期表所有稳定元素,而太阳却只开始发生氢燃烧,该核反 应的产物只有氢,应怎样理解这个事实? 1-10 中国古代哲学家认为,宇宙万物起源于一种叫“元气”的物质,“元气生阴阳,阴阳 生万物”,请对比元素诞生说与这种古代哲学。 1-11 “金木水火土”是中国古代的元素论,至今仍有许多人对它们的“相生相克”深信 不疑。与化学元素论相比,它出发点最致命的错误是什么? 1-12 请用计算机编一个小程序,按 1.3 式计算氢光谱各谱系的谱线的波长(本练习为开 放式习题,并不需要所有学生都会做)。 n1 n2 1(来曼光谱) 1 2 3 4 波长 2(巴尔麦谱系) 1 2 3 4 波长 3(帕逊谱系) 1 2 3 4 波长 4(布来凯特谱系) 1 2 3 4 波长 5(冯特谱系) 1 2 3 4 波长

1-13计算下列辐射的频率并给出其颜色:(1)氢-氖激发光波长633m:(2)高压汞灯辐 射之一435.8nm:(3)锂的最强辐射670.8nm。 13、(1)氦氖激光的频率为U-M-4.74X104也 (②高压灯辐射之一的频率为:=v八-6.884X104也 (3)锂的最3强辐射的频率为:D=v-4.47X104比 1-14Br,分子分解为Br原子需要的最低离解能为190KJ。mol,求引起溴分子解离需 要吸收的最低能量子的波长与频率。 14、190x703 502×10h-763x104也 =vh=3.0X104.763X104=6.298×10m-629.8m 1-15高压钠灯辐射589.6nm和589.0nm的双线,他们的能量差为多少KJ.mo11? 15、△E=h4-h 6626×104(30×102-30x10 3589.6x10589×10 =-3.434×1023 1-16当频率为1.0×10Hz的辐射照射到金属铯的表面,发生光电子效应,释放出的光 量子的动能为5.2×10°,求金属铯释放电子所需能量。 16、B-h- =6.626×1034×1.3×105-5.2×1019 =3.414×109J 1-17变色眼镜因光照引起玻璃中的氯化银发生分解反应一一AgC1-Ag+C1,析出的银微粒 导致玻璃变暗,到暗处该反应逆转。已知该反应的能量变化为310KJ.mol-1,问:引起 变色眼镜变暗的最大波长为多少? 17、 -310×10316.02X1023 E-3.86×10r'm-386nmhu/ 1-18光化学毒雾的重要组分之 一N02解离为N0和02需要的能量为305KJ.mo1-1, 引起这种变化的光最大波长多大?这种光属于哪一种辐射范围(可见,紫外,X光等等)? 已知射到地面的阳光的最短波长为320m,02气体在近地大气里会不会解离? 18、E-=305X10316.02X1023=hu12 =3.92X10'm=392nm>320nm 这种光属于紫外光,在进地大气会分解。 1-19氢原子核外电子光谱中的菜曼光谱中有一条谱线的波长为103nm,问:它相应于氢 原子核外电子的哪一个跃迁? 19、它相应于氢原子核外电子L→K跃迁
3 1-13 计算下列辐射的频率并给出其颜色:(1)氦-氖激发光波长 633nm;(2)高压汞灯辐 射之一 435。8nm;(3)锂的最强辐射 670。8nm。 1-14 Br2 分子分解为 Br 原子需要的最低离解能为 190KJ。mol-1 ,求引起溴分子解离需 要吸收的最低能量子的波长与频率。 1-15 高压钠灯辐射 589.6nm 和 589.0nm 的双线,他们的能量差为多少 KJ.mol-1 ? 1-16 当频率为 1.0×10-15Hz 的辐射照射到金属铯的表面,发生光电子效应,释放出的光 量子的动能为 5.2×10-19 ,求金属铯释放电子所需能量。 1-17 变色眼镜因光照引起玻璃中的氯化银发生分解反应——AgCl-Ag+Cl ,析出的银微粒 导致玻璃变暗,到暗处该反应逆转。已知该反应的能量变化为 310KJ.mol-1 ,问:引起 变色眼镜变暗的最大波长为多少? 1-18 光化学毒雾的重要组分之一——NO2 解离为 NO 和 O2 需要的能量为 305KJ.mol-1, 引起这种变化的光最大波长多大?这种光属于哪一种辐射范围(可见,紫外,X 光等等)? 已知射到地面的阳光的最短波长为 320nm,NO2 气体在近地大气里会不会解离? 1-19 氢原子核外电子光谱中的莱曼光谱中有一条谱线的波长为 103nm,问:它相应于氢 原子核外电子的哪一个跃迁?

1-20氢首先发现于日冕。1868年后30年间,太阳是研究氨的物理,化学性质的唯一源 泉。 (a)观察到太阳可见光谱中有波长为4338A,4540A,4858A,5410A,6558A 的吸收(1A=10"m来分析,这些吸收是由哪一种类氢原子激发造成的?是He,He'还是 He2”? (b)以上跃迁都是由n,=4向较高能级(n)的跃迁。试确定n值,求里德堡常数R”。 (c)求上述跃迁所涉及的粒子的电离能I(He”),用电子伏特为单位。 (d)已知I(He)/I(He)=2.180。这两个电离能的和是表观能A(He),即从He 得到He2"的能量。A(He”)是最小的能量子。试计算能够引起He电离成He”所需要的最 低能量子。在太阳光中,在地球上,有没有这种能量子的有效源泉? (c=2.997925×10msh=6.626×10Js:1eV=96.486KJ.mol-1=2.4180×10z) 1-21当电子的速度达到光速的20.0%时,该电子的德布罗意波长多大?锂原子(质量 7.02au)以相同速度飞行时,其德布罗意波长多大? 21、乃=m-0.2×9.1x10-31×3.0x108 -5.46×102kgms 1=P1-6.626X1034/5.46×1023-1.214X1011m 乃=mv=7.02×0.2x3.0x10x10316.02×1028-2.53x10-”kgm 32=P2=1.214X10”m 1-22垒球手投掷出速度达152Km.h质量为142g的垒球,求德布罗意波长。 22、P-mv-142x103x152×103/3600-5.996kg5 =h/P-6.626×102*5.996-1.105×10-34m 1-23处于K、L、M层的最大可能数目各为多少? 23、K2,L8,M18 1-24以下哪些符号是错误的?(a)6s(⑥)1p(c)4d(d)2d(e)3p(f)3f 24、错误的有:1p,2d,3f 1-25描述核外电子空间运动状态的下列哪一套量子数是不可能存在的? n m n 1 n l m n 1 m 200 11021-1655 25、第二组是不可能存在的 1-26以下能级的角量子数多大?(a)1s(b)1p(c)4d(d)2d(e)3n(f)3f 4
4 1-20 氦首先发现于日冕。1868 年后 30 年间,太阳是研究氦的物理,化学性质的唯一源 泉。 (a)观察到太阳可见光谱中有波长为 4338A,4540A,4858A,5410A,6558A 的吸收(1A=10-10 m 来分析,这些吸收是由哪一种类氢原子激发造成的?是 He,He +还是 He2+ ? (b)以上跃迁都是由 ni=4 向较高能级(nf)的跃迁。试确定 nf 值,求里德堡常数 RHe i+。 (c)求上述跃迁所涉及的粒子的电离能 I(Hej+),用电子伏特为单位。 (d)已知 I(He+)/ I(He)=2.180。这两个电离能的和是表观能 A(He2+),即从 He 得到 He2+的能量。A(He2+)是最小的能量子。试计算能够引起 He 电离成 He2+ 所需要的最 低能量子。在太阳光中,在地球上,有没有这种能量子的有效源泉? (c=2.997925×108 ms -1 ;h=6.626×10-34Js;1eV=96.486KJ.mol-1=2.4180×1014Hz) 1-21 当电子的速度达到光速的 20.0%时,该电子的德布罗意波长多大? 锂原子(质量 7.02amu)以相同速度飞行时,其德布罗意波长多大? 1-22 垒球手投掷出速度达 152Km.h-1 质量为 142g 的垒球,求德布罗意波长。 1-23 处于 K﹑L﹑M 层的最大可能数目各为多少? 1-24 以下哪些符号是错误的?(a)6s (b)1p (c)4d (d)2d (e)3p (f)3f 1-25 描述核外电子空间运动状态的下列哪一套量子数是不可能存在的? n l m n l m n l m n l m 2 0 0 1 1 0 2 1 -1 6 5 5 1-26 以下能级的角量子数多大?(a)1s (b)1p (c)4d (d)2d (e)3p (f)3f

26、1s角量子数为0 4p角量子数为1 5d角量子数为2 6s角量子数为0 5f角量子数为3 5g角量子数为4 1-274s、5p、6d.7f、5g能级各有几个轨道? 27、4s能级有1个轨道 5印能级有3个轨道 6d能级有5个轨道 7F能级有7个轨道 5g能级有9个轨道 1-28根据原子序数给出下列元素的基态原子的核外电子组态: (a)K (b)Al (c)Cl (d)Ti(Z=22)(e)Zn(Z=30)(f)As(Z=33) 28、a:1s22s22p3s23p4s1 b: c:1g22s22p3s23p3 d 1s2222p3g23p3d4s2 e:1s22s2p33p3d04s2 f:1s222p33p3d4s24p 1-29若构造原理对新合成的及未合成的人造元素仍有效,请预言第118和166号元素在 周期表中的位置(注:1999年美国宣布合成了118号元素及其衰变产物116号元素,但 2001年因不能重复而收回该报道)。 29、第118号元素位于第七周期0族 第166号元素位于第八周期VI族 1-30给出下列基态原子或离子的价电子层电子组态,并用方框图表示轨道,填入轨道的 电子则用箭头表示。(a)Be(b)N(c)F(d)CI(e)Ne(f)Fe"(g)As 30、(a)1s282(b)1s22s22p'(c)1s2s22p(d)1s2822p3s23p(e)1s2s 2p'(f)[Ar]3d(g)[Ar]4s? 1-31下列哪些组态符合洪特规则? 1s 2s 2p 3s 3p ↑↓↑↓↑↓↓↓ ↑↓↑↓↑↓↑↓↑↓↑↑↑1 31、第一组符合
5 1-27 4s﹑5p﹑6d﹑7f﹑5g 能级各有几个轨道? 1-28 根据原子序数给出下列元素的基态原子的核外电子组态: (a)K (b)Al (c)Cl (d)Ti(Z=22) (e)Zn(Z=30) (f)As(Z=33) 1-29 若构造原理对新合成的及未合成的人造元素仍有效,请预言第 118 和 166 号元素在 周期表中的位置(注:1999 年美国宣布合成了 118 号元素及其衰变产物 116 号元素,但 2001 年因不能重复而收回该报道)。 1-30 给出下列基态原子或离子的价电子层电子组态,并用方框图表示轨道,填入轨道的 电子则用箭头表示。(a)Be (b)N (c)F (d)Cl- (e)Ne+ (f)Fe3+ (g)As3+ 1-31 下列哪些组态符合洪特规则? 1s 2s 2p 3s 3p ↑↓ ↑↓ ↑↓ ↓↓ ↑↓ ↑↓ ↑ ↑ ↑ ↑↓ ↑↓ ↑↓ ↑↓↑↓ ↑↑↑↑