12.2 羧酸的结构(略) 12.3羧酸的制法 12.3.1羧酸的工业制合成 1、由烷基苯氧化制备 CHCHCHCH KMI/TCOOH 2、由伯醇、醛的氧化制备: CH(CHaACH2OH KMHCH(CH)COOH CH(CHACHO KMH CHs(CH)COOH
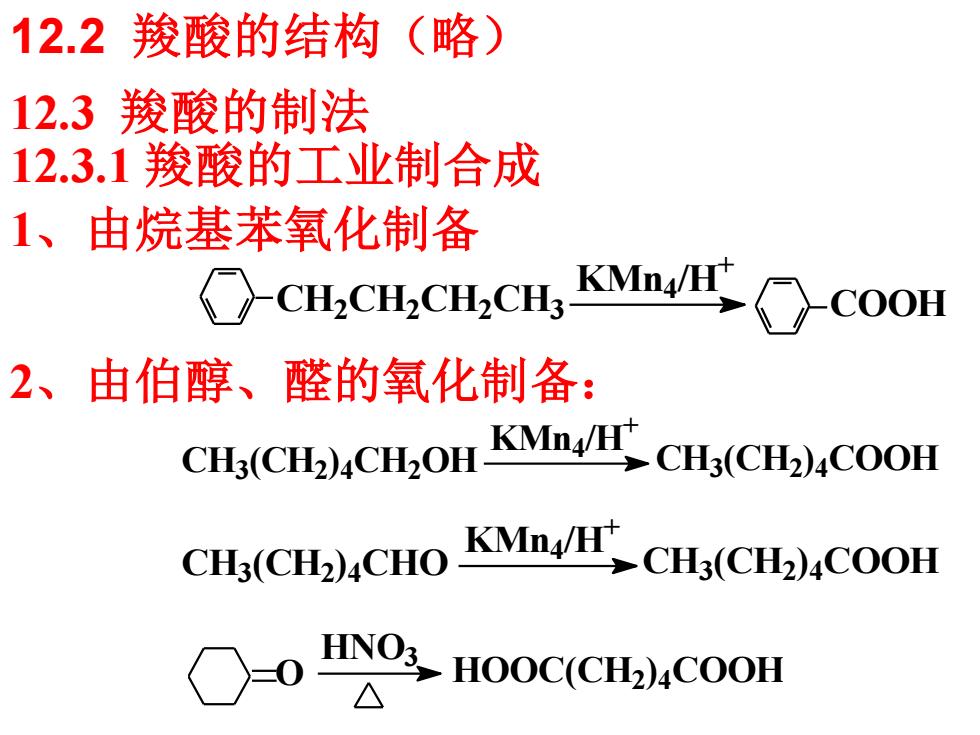
12.3 羧酸的制法 12.3.1 羧酸的工业制合成 12.2 羧酸的结构(略) 1、由烷基苯氧化制备 CH2 CH2 CH2 CH3 KMn4 /H + COOH 2、由伯醇、醛的氧化制备: CH3 (CH2 ) 4 CH2 OH KMn4 /H + CH3(CH2) 4 COOH CH3 (CH2 ) 4 CHO KMn4 /H + CH3(CH2) 4 COOH HOOC(CH2) 4 COOH HNO3 O
3、由碘仿反应制备: CH3(CH2)4CCH3 L/NaOH CHa(CH2)4COOH △ 4、由腈的水解制备: CH(CH2)CN H2O/HCH(CH2COOH △ 5、用Grignard试剂与CO2反应制备 RCHMEX+CO回液 RCH2COMEX H2O/H RCH2COOH Br Mg 乙醚 MgBr ②H0
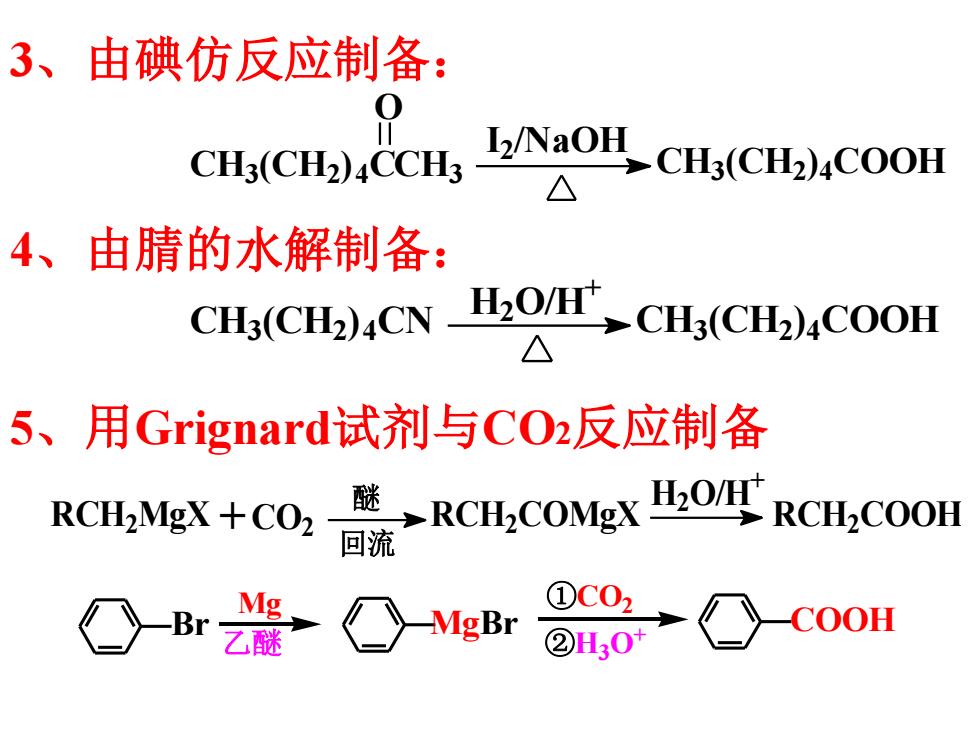
Br Mg 乙醚 MgBr ①CO2 ②H3O+ COOH 4、由腈的水解制备: 3、由碘仿反应制备: CH3(CH2) 4 CCH3 CH3(CH2) 4 COOH O I2/NaOH CH3(CH2) 4 CN CH3 (CH2 ) 4 COOH H2 O/H + 5、用Grignard试剂与CO2反应制备 RCH2MgX +CO2 回流 RCH2 COMgX H2 O/H + RCH2 COOH 醚
6、Kolbe-Schmitt反应制备酚酸 ONa OH +C02 150℃ COONa COOH 90% 0.5MPa OK OH OH 180~250℃ +C02 2.02MPa COOK COOH 12.4羧酸的物理性质 R-c -H-0 C-R 0-H-0 两个羧酸分子间 羧酸与H2O分子 形成的氢键 形成的氢键
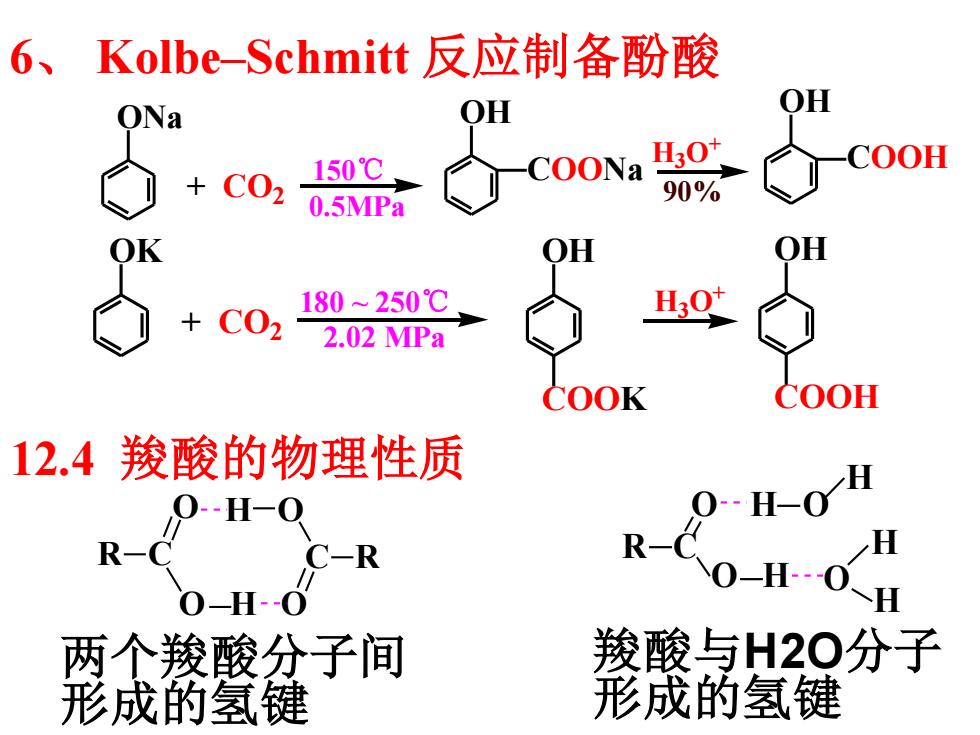
6、 Kolbe–Schmitt 反应制备酚酸 OK + CO2 180 ~ 250℃ 2.02 MPa OH COOK H3O+ OH COOH ONa + CO2 150℃ 0.5MPa OH COONa H3O + 90% OH COOH 12.4 羧酸的物理性质 两个羧酸分子间 形成的氢键 羧酸与H2O分子 形成的氢键 O O R C O H H O C R O R C O H O H H H O H

12.5羧酸的波谱性质 羧酸的IR特征:Vc=o1760~1710cm-l Vo-H3550~3300cm-1 羧酸的NMR特征:羧基氢质子δ=9~12.5ppm 12.6羧酸的化学性质 12.6.1羧酸的酸性和极化效应 ()羧酸的酸性 RCOOH NaOH->RCOONa +H2O RCOOH NaHCO>RCOONa +CO2+H2O RCOONa HCI->RCOOH +NaCI 两个反应合用用作羧酸的鉴别和分离
羧酸的IR特征:νC=O 1760~1710cm-1 νO-H 3550~3300cm-1 羧酸的NMR特征:羧基氢质子δ=9~12.5ppm 12.5 羧酸的波谱性质 12.6 羧酸的化学性质 12.6.1 羧酸的酸性和极化效应 (1) 羧酸的酸性 RCOOH + NaOH RCOO Na + H2O RCOOH + NaHCO3 RCOO Na + CO2 + H2 O RCOONa + HCl RCOOH + NaCl 两个反应合用用作羧酸的鉴别和分离
RCOOH H2CO3 CHOH H2O> pka:4~5 6.38 10 15.74 RCH,OH RNH2 16~19 ~34 (2)羧酸的结构与酸性的关系 3)影响羧酸酸性的因素 羧酸α-碳上的氢被吸电子原子或基团 取代后,酸性增强,而且α-碳上吸电子 原子或基团越多,酸性越强
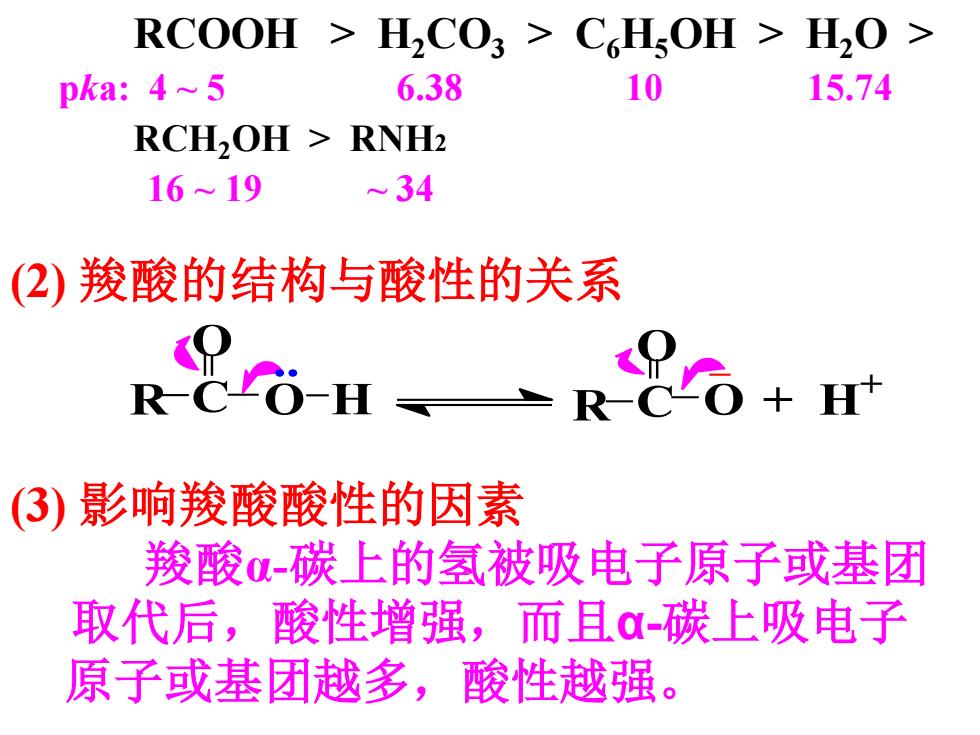
RCOOH > H2CO3 > C6H5OH > H2O > pka: 4 ~ 5 6.38 10 15.74 RCH2OH > RNH2 16 ~ 19 ~ 34 (2) 羧酸的结构与酸性的关系 R O H R O + H + C O C O . (3) 影响羧酸酸性的因素 羧酸α-碳上的氢被吸电子原子或基团 取代后,酸性增强,而且α-碳上吸电子 原子或基团越多,酸性越强