
固相反应动力学:Diffusion coefficients 1.K+in B-Al2O3 2.0inCa0.14Zr0.s601.86 3.Co in Co1s0 (air) 1720390145980830730630 4. Oin Y2O3 -6 5.Cr in Cr2O3 6.Oin Co1s0 (air) 7.Nin UN 8.Co in Co1s0(Po2=10-14 Bar) 9.Al in a-Al2O3 .10 10.Na in NaCl 11.0inU02.00 12 12.O in a-Al2O3 (polycrystalline) 13.O in a-Al,O3 (single crystalline 14.C in graphite .14 15.O in Cr2O3 16.Uin UO2 0.4 06 0810 214 1/T103(K- 17.0 in SiO,(glass)
固相反应动力学:Diffusion coefficients 1 K+ . in -Al2O3 2. O in Ca0.14Zr0.86O1.86 3. Co in Co1-O (air) 1- ( ) 4. O in Y2O3 5. Cr in Cr2O3 6. O in Co1-O (air) 7. N in UN 8 Co in Co O (P = 10 8. Co in Co -14 Bar) 1-O (PO2= 10 14 Bar) 9. Al in -Al2O3 10. Na in NaCl 11. O in UO2.00 12. O in -Al2O3 (polycrystalline) 13. O in -Al2O3 (single crystalline) 14. C in graphite 15. O in Cr O in Cr2O3 16. U in UO2 17. O in SiO2 (glass)

固相反应热力学:驱动力 ©化学势或电化学势梯度:一种固相反应,总伴随有晶 体物相中物质(原子或离子)的局部输运。扩散前后 原子或离子的电子构型有明显变化,这种变化是与原 子或离子的化学势或电化学势变化有关的。 4,=G,=( ∂G n; Vi=V(u。+kTIna+zep) 1:=4,+3,F 矿其它驱动力:温度、外电场、表面张力等。 -温度:固溶体的分离现象(demiⅸ)。 -外电场:离子晶体在外电场下的电解。 表面张力:固相烧结
固相反应热力学:驱动力 化学势或电化学势梯度:一种固相反应,总伴随有晶 体物相中物质(原子或离子)的局部输运。扩散前后 原子或离子的电子构型有明显变化,这种变化是与原 子或离子的化学势或电化学势变化有关的。 ) G μ G ( P,T,n n i i j i 其它驱动力:温度、外电场、表面张力等。 η μ z F n i i i , , i j i 其它驱动力:温度、外电场、表面张力等。 - 温度:固溶体的分离现象(demix)。 - 外电场: 离子晶体在外电场下的电解。 - 表 力 相烧结 表面张 力:固相烧结

固相反应热力学 固相反应绝大多数在等温等压下进行,因此用△G判别反应方 向及其限度。 ●如果可能发生几个反应,生成几种产物(AA2A3A), 且4G1<4G2<4G3.<4Gn,则最终产物为A相。但当4G1,4G均 是负值时,这些反应均可进行,而且生成这些相的顺序并不完 全由G值的相对大小而定,而是与动力学(即反应速率)相关。 反应速率越大,反应进行的可能越大。 ●对于反应物和生成物都是固相的纯固相反应,总是往放热 (H<0)的方向进行,这称为范特霍夫规则。 ●一般认为,为了在固相间进行反应,固相反应的放热大于1 kca/mol就够了;而大多数硅酸盐反应的反应热为几十到几百 kca/mol,所以热力学上没问题,主要受动力学因素限制。 ● 当固相反应中有液相或气相参与时,范特霍夫规则不适用
固相反应热力学 固相反应绝大多数在等温等压下进行,因此用 G判别反应方 向及其限度。 如果可能发生几个反应,生成几种产物( 如果可能发生几个反应,生成几种产物( A 1 、 A 2 、 A 3.A n), 且 G1 <G2 <G3.<Gn,则最终产物为 A 1相。但当 G1 . Gn 均 是负值时,这些反应均可进行,而且生成这些相的顺序并不完 全由 G值的相对大小 定 是与动力学(即反应速率)相关 值的相对大小 而定, 而是与动力学(即反应速率)相关 。 反应速率越大,反应进行的可能越大。 对于反应物和生成物都是固相的纯固相反应,总是往放热 ( H<0)的方向进行,这称为范特霍夫规则 。 一般认为,为了在固相间进行反应,固相反应的放热大于1 kcal/mol 就够了;而大多数硅酸盐反应的反应热为几十 到几百 kcal/mol,所以热力学上没问题,主要受动力学因素限制 所以热力学上没问题 主要受动力学因素限制 。 当固相反应中有液相或气相参与时,范特霍夫规则不适用
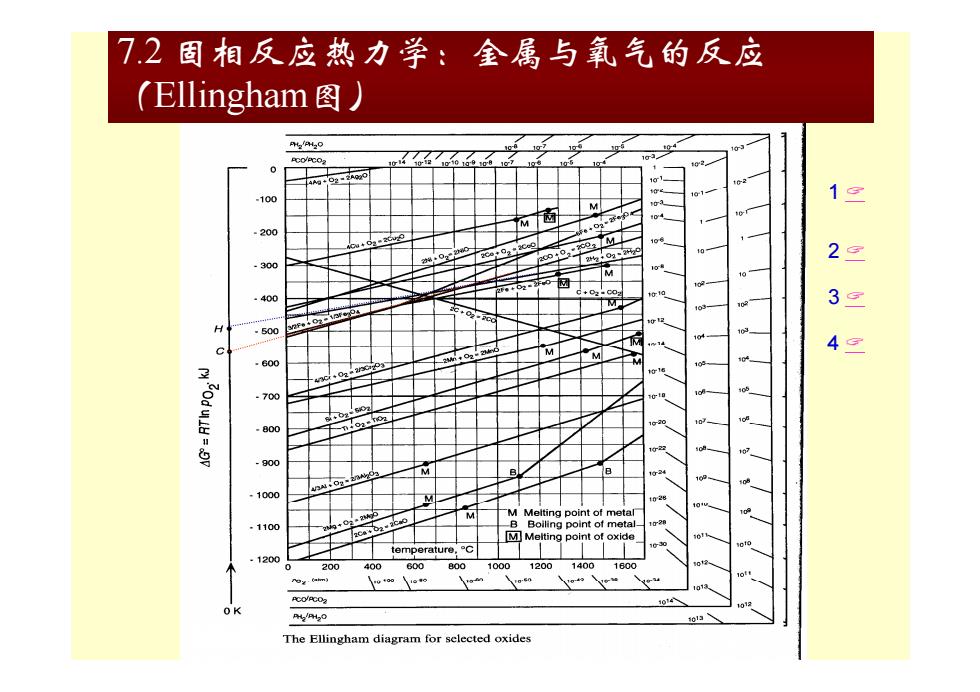
72固相反应热力学:全属与氧气的反应 (Ellingham图) 42420 100 1 200 30 400 3 50 4© 03 70 100( 1100 temperature.C 120X 200 400 600 The Ellingham diagram for selected oxides
7.2 固相反应热力学:金属与氧气的反应 (Ellingham图) 1 ( g 图) 1 2 3 4

Ellingham diagram H/H,Oratio 0 10 cO/Co ratio 10 4fe0+0=6fe 2Co+02o0 10 4c+0*20u0 26+020 0 2+00 10 00 10* 有C+0=00 2Mn+0,=2n0 10 258+0,=2540 2n+0*20 2+0,=1,0 10 +0202 2ca+0.-2Ca0 10y 10 10 600 100126040 16001w69300220022 Temperature ('C) CO/CO,ratio 10 10 H/H,Oratio 0 10 0 109 10 0
Ellingham diagram