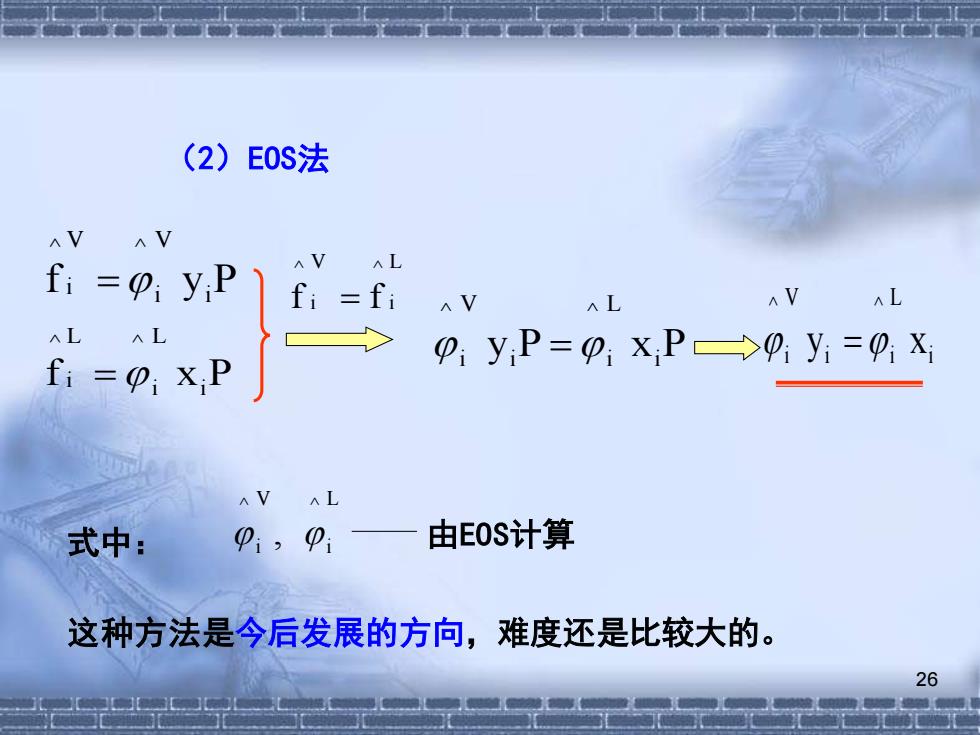
(2)E0S法 AV AV fi y;P fi =fi 入V AV AL AL fi=0:xP i yP=0:xP0yi=0x AV AL 式中: P1,01 由E0S计算 这种方法是今后发展的方向,难度还是比较大的。 26
26 L i V ^ i ^ f = f (2)EOS法 f yi P V i V ^ i ^ = f xi P L i ^ L i ^ = y P xi P L i ^ i V i ^ = i L i ^ i V i ^ y = x 这种方法是今后发展的方向,难度还是比较大的。 L i V ^ i ^ 式中: , 由EOS计算

(3)Y法 活度系数法是将汽液两相都用活度系数来表示 AL L相: fi=yx;fo AV V相: fi=y fov VLE时 ry fov x fo YVyPSexp ry;exp 27
27 活度系数法是将汽液两相都用活度系数来表示 0V i i V i ^ V f y f V i 相: = 0L i i L i ^ L f x f L i 相: = (3)γi法 = 0V i i y f V i 0L i i x f L i P P V i S i S i i V i S i V dP RT 1 y P exp P p L i s i s i i L i s i V dP RT 1 x P exp P P V i i V i S i V dP RT 1 y exp P p L i i L i s i V dP RT 1 x exp VLE时 = =

二.低压下VLE的计算 ·1.完全理想体系(物理化学讲过) 2.化学体系 ·对于低压高温的体系,当其组成体系的各组分的分子 结构差异较大时,汽相可以看作是理想气体,但其液 相由于分子间作用力差异较大,因而不能看作是理想 溶液。对于这类体系,称为化学体系。 28
28 二.低压下VLE的计算 ▪ 1.完全理想体系(物理化学讲过) ▪ 2.化学体系 ▪ 对于低压高温的体系,当其组成体系的各组分的分子 结构差异较大时,汽相可以看作是理想气体,但其液 相由于分子间作用力差异较大,因而不能看作是理想 溶液。对于这类体系,称为化学体系

(1)计算式: 前面我们已经推出VLE的基本计算式为 .y.P-yix.0SPSexp (7-8) PS ·低压高温 p=1 p3=1 VL<<RT ∴.式(7-8)可写为 yP=YiX,PS 对于二元溶液 P=y P=YiX PS P2 =y2P=Y2X2P$=Y2(1-x1)PS P-P1+P2=YiX PS Y2X2PS 对多元体系 P=∑yP=∑yxP 29
29 = P P L i S i S i i i i i ^ S i V dP RT 1 y P x P exp 1 1 S i i ^ = = V dP 1 RT 1 exp P P L i S i = S yi P i xi Pi = S P1 y1 P 1 x1 P1 = = S 2 1 2 S 2 2 2 2 2 P = y P = x P = (1- x )P S 1 x1 P1 S 2 x2 P2 S P yi P i xi Pi = = (1) 计算式: 前面我们已经推出VLE的基本计算式为 (7-8) ∵低压高温 V L i <<RT ∴式(7-8)可写为 对于二元溶液 P=P1 +P2 = + 对多元体系

(2)汽液平衡比K,和相对挥发度 汽液平衡比:在汽液平衡时,组 分在汽相中的摩尔分数与液相中 即 K;=yi 的摩尔分数的比值 Xi 相对挥发度:两组份汽液平衡比的比值。 Kiyilxi K yi/xi 对于化学体系,由上边知: 汽液平衡比 K=-TP刘 P 相对挥发度 Ky:/xrPS Kj y /x;rips 对二元体系 KLylxPS 012 K2 22P 30
30 ij i i i x y K = j j i i j i ij y /x y /x K K = = (2)汽液平衡比Ki和相对挥发度 即 对于化学体系,由上边知: 对二元体系 f(T, P, x) P P S i i = = Ki S j j S i i j j i i j i ij P P y /x y /x K K = = = S 2 2 S 1 1 2 2 1 1 2 1 12 P P y /x y /x K K = = = 汽液平衡比 相对挥发度 汽液平衡比:在汽液平衡时,组 分i在汽相中的摩尔分数与液相中 的摩尔分数的比值. 相对挥发度:两组份汽液平衡比的比值