共轭酸碱对特征(conjugate acid-base pair) 共轭酸碱是成对出现的,形式上相差一个质子(氢离子) Ac HAc X X H3PO-H2PO-HPO2-PO3 P162思考题3 16
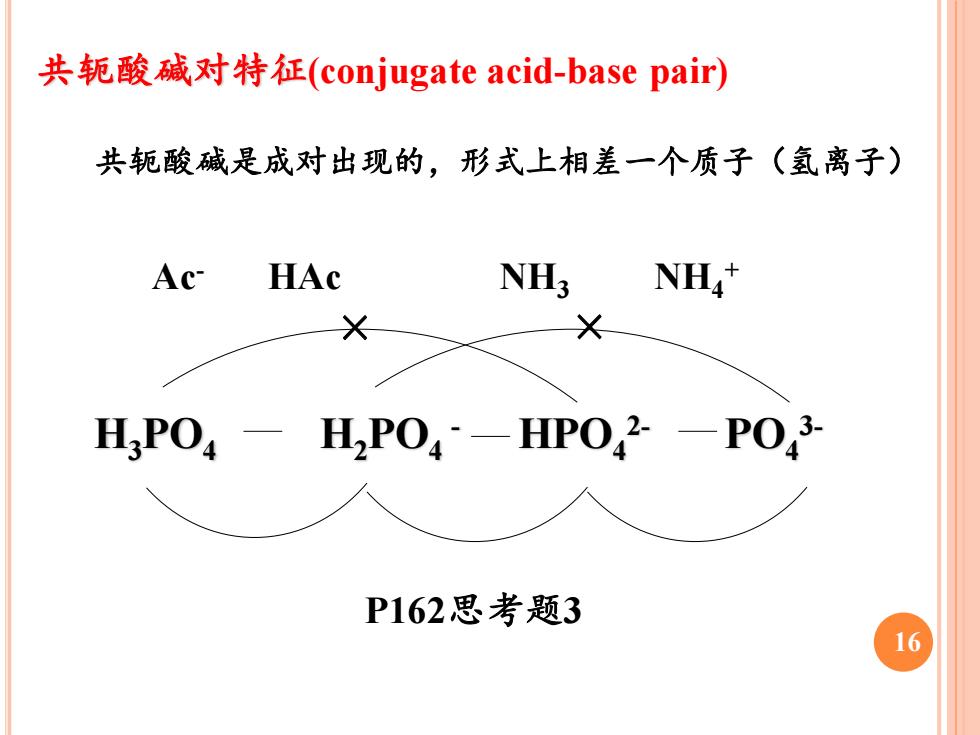
共轭酸碱对特征(conjugate acid-base pair) 共轭酸碱是成对出现的,形式上相差一个质子(氢离子) Ac- HAc NH3 NH4 + H3PO4 H2PO4 - HPO4 2- PO4 3- × × 16 P162思考题3

共轭酸碱对的K和K的关系 (m'Ac KaXK。=H][OH=Kw=1×10-14(25℃) pKa +pkp=pK=14.00(25C) 。 任何共轭酸碱对适用。 。K,和K是成反比的,而K和K正是反映酸和碱的强度, 。在共轭酸碱对中,酸的强度愈大,其共轭碱的强度愈小; ⊙碱的强度愈大,其共轭酸的强度愈小
共轭酸碱对的Ka和Kb的关系 K H Ac HAc a = + − K HAc OH Ac b = − − • Ka×Kb=[H+ ][OH- ]= Kw =1×10-14 (25℃) • pKa + pKb = pKw = 14.00 (25℃) • 任何共轭酸碱对适用。 Ka和Kb是成反比的,而Ka和Kb正是反映酸和碱的强度, 在共轭酸碱对中,酸的强度愈大,其共轭碱的强度愈小; 碱的强度愈大,其共轭酸的强度愈小。 17

共轭酸碱对之间的转变可视作酸碱半反应,两个半反应构成一 个完整的酸碱反应,如氨在水中的离解: 半反应1 NH3(碱1)+Ht亡NH,(酸1) 半反应2 H,0(酸2) OH(碱2)+H中 NH3(碱1)+H,O (酸2)三O(碱2)+NH4+(酸1) 共轭酸碱对 K [NH:JOH-] [NH 而其共轭酸NH十的解离反应为 NHNH+H K;[NH,]tH'] [NH] 18 可见:K= 或 K。·K6=K K
半反应1 NH3(碱1)+ H+ NH4 +(酸1) 半反应2 H2O(酸2) OH-(碱2)+ H+ NH3(碱1) + H2O (酸2) OH- (碱2)+ NH4 + (酸1) 共轭酸碱对 4 3 [ ][ ] [ ] b NH OH K NH + − = 而其共轭酸NH4 +的解离反应为 NH NH H 4 3 + + + ' 3 4 [ ][ ] [ ] a NH H K NH + + = 可见: ' w a b K K K = 或 ' K K K a b w = 18 共轭酸碱对之间的转变可视作酸碱半反应,两个半反应构成一 个完整的酸碱反应,如氨在水中的离解:

>酸碱半反应不可能单独发生 ,酸碱反应是两对共轭酸碱对共同作用的结果 >酸碱反应的实质是质子的转移 质子的转移是通过溶剂和质子来实现的 19
➢酸碱半反应不可能单独发生 ➢酸碱反应是两对共轭酸碱对共同作用的结果 ➢酸碱反应的实质是质子的转移 ➢质子的转移是通过溶剂和质子来实现的 19

多元酸碱的离解 H;PO H2PO+H Kal Kp3 H2P04= HPO2+H+ Ka2 Kp2 HPO2-PO3+H Ka3 Kpl 20
多元酸碱的离解 H3PO4 H2PO4 - + H+ Ka1 Kb3 H2PO4 - HPO4 2- + H+ Ka2 Kb2 HPO4 2- PO4 3- + H+ Ka3 Kb1 20