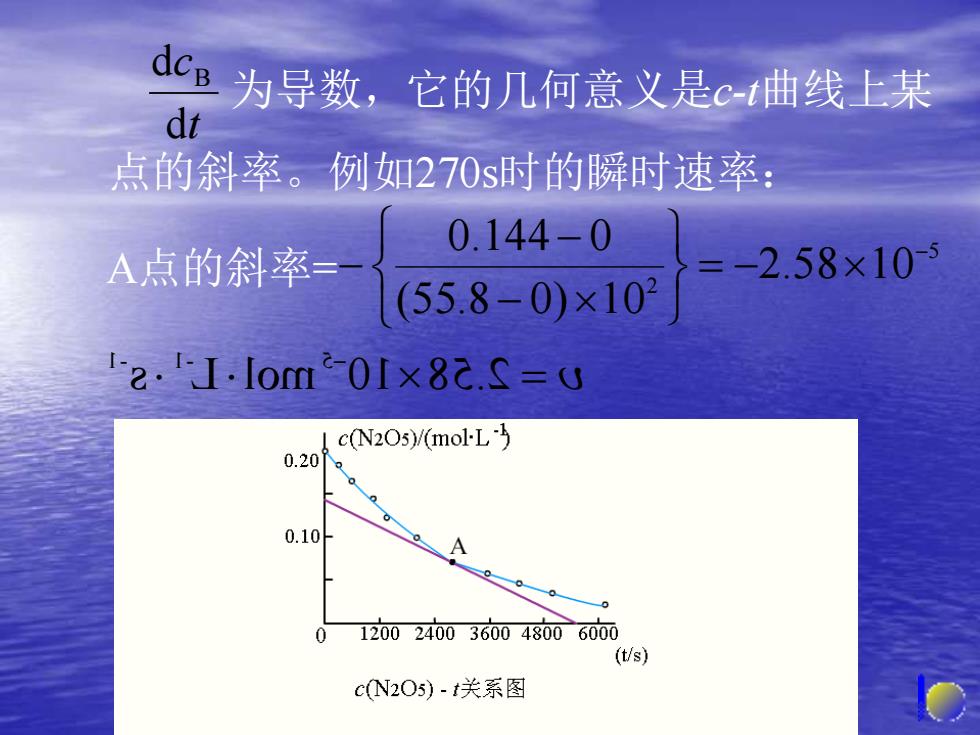
dcB 为导数,它的几何意义是c-t曲线上某 dr 点的斜率。例如270s时的瞬时速率: 0.144-0 A点的斜率= -2.58×10 (55.8-0)×102 2.J.lom01×82.S=g c(N2Os)/(mol-L 0.20 0.10 0 12002400360048006000 (t/s) cN2O5)-关系图
t c d d B 为导数,它的几何意义是c-t曲线上某 点的斜率。例如270s时的瞬时速率: 5 2 2.58 10 (55.8 0) 10 0.144 0 − = − − − A点的斜率=− - 1 - 1 5 s L mol 10 58 . 2 = −

浓意对反寇速牵的影向 一速章方程式 ©>1化学反应速率方程式 2由实验确定反应速率方程的 简单方法一初始速率法 3.2.3 浓度与时间的定量关系 返回
浓度对反应速率的影响 —速率方程式 1 化学反应速率方程式 3.2.3 浓度与时间的定量关系 2 由实验确定反应速率方程的 简单方法—初始速率法
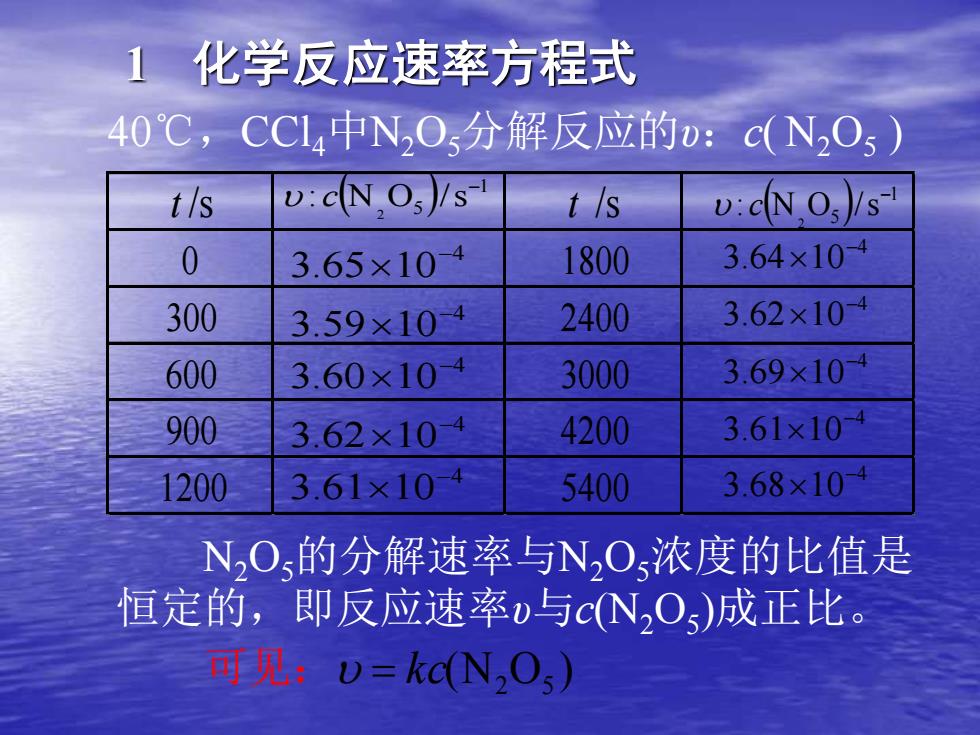
1化学反应速率方程式 40℃,CCl,中NO分解反应的D:c(N2O5) t/s v:cN.O3)/s t/s v:cNO)/s 0 3.65×104 1800 3.64×104 300 3.59×104 2400 3.62×104 600 3.60×104 3000 3.69×10 900 3.62×104 4200 3.61×10 1200 3.61×104 5400 3.68×10 NO的分解速率与NO浓度的比值是 恒定的,即反应速率w与cNOs)成正比。 可见:D=kc(N,Os)
40℃,CCl4中N2O5分解反应的υ:c( N2O5 ) t /s t /s 0 1800 300 2400 600 3000 900 4200 1200 5400 ( ) 1 5 : N O /s 2 − c 4 3.65 10− 4 3.60 10− 4 3.62 10− 4 3.61 10− 4 3.59 10− 4 3.69 10− 4 3.62 10− 4 3.64 10− 4 3.68 10− 4 3.61 10− ( ) 1 5 : N O /s 2 − c 1 化学反应速率方程式 N2O5的分解速率与N2O5浓度的比值是 恒定的,即反应速率υ与c(N2O5 )成正比。 可见: (N O ) 2 5 = kc

对于一般的化学反应: aA+bB->yY+zZ D=kcc昭 a,B一反应级数:若ca=1,A为一级反应 B=2,B为二级反应,则a+B=3,总反应级数 为3。α,B必须通过实验确定其值。通常 0+a,B≠b。 k反应速率系数:零级反应molL1s': 级反应sl;二级反应(molL)ls;k 不随浓度而变,但受温度的影响,通常温度 升高,k增大
对于一般的化学反应: α,β—反应级数:若α=1,A为一级反应; β=2,B为二级反应,则α+β=3,总反应级数 为3。α,β必须通过实验确定其值。通常 α≠a,β≠b。 k —反应速率系数:零级反应 mol·L-1 ·s-1; 一级反应 s -1;二级反应 (mol·L -1 ) -1 ·s-1; k 不随浓度而变,但受温度的影响,通常温度 升高, k 增大。 aA +bB→ yY + zZ A B = kc c

化学计量 速率 反应计量 方程式 方程 级数 数 NO2 (g)+CO(g)- <500K〉 =kc(NO2) 2 1+1 NO(g)+CO,(g) H,(g)+I2(g)→2HI(g)【 =KC(H)c(I) 1+1 1+1 2NO(g)+02(g)->2NO,(g)v=kdNO Yc(O2) 2+1 2+1 2Nog)+2H,g)→N,g)+H,0g)D=kdNo〗cH,) 2+1 2+2 S2o(aq)+3I(aq)-→ 1+1 1+3 2SO (aq)+I (aq) D=kS,00) 5Br-(aq)+BrOj(aq)+6H"(aq)v=kc(Br-) 3Br2(aq)+3H2O(aq) cBo)[日*月1+1+25+1+6
化 学 计 量 方 程 式 速 率 方 程 反 应 级 数 计 量 数 2 1+1 1+1 1+1 2+1 2+1 2+1 2+2 1+1 1+3 1+1+25+1+6 ( ) ( ) 2- - 2 8 = k c S O c I (NO ) (O ) 2 kc c 2 = ( ) ( ) 2 2 = kc H c I ( ) ( ) NO H2 2 = kc c ( ) 2 NO2 = k c ( ) ( ) ( ) 2 - 3 - BrO H Br + = c c k c ( ) ( ) NO(g) CO (g) NO g CO g 2 500K 2 + + ⎯ ⎯⎯→ H (g) I (g) 2HI(g) 2 + 2 → 2NO(g) O (g) 2NO (g) + 2 → 2 ( ) ( ) 2SO (aq) I (aq) S O aq 3I aq 3 2 4 2 2 8 − − − − + + → ( ) ( ) ( ) 3Br (aq) 3H O(aq) Br aq BrO aq 6H aq 2 2 3 + 5 − + − + + → 2NO(g) 2H (g) N (g) H O(g) + 2 → 2 + 2