
例2: Ba2+过量0.01ol1L与SO2反应的BaSO,沉淀溶解度为 S=[S0]= 。_1.1×10-10 =1.1×10-8mol/L [Ba2] 0.01 →200ml溶液中BaSO,沉淀的溶解损失为 1.0×10-8×233.4×200=5.0×104g<<0.2g 2024/10/1
2024/10/1 例2: mol L B a K S SO B a mol L SO BaSO SP 1.1 10 / 0.01 1.1 10 [ ] [ ] 0.01 / 8 1 0 2 2 4 4 2 4 2 − − + − + − = = = = 过量 与 反应的 沉淀溶解度为 mg mg ml BaSO 1.0 10 233.4 200 5.0 10 0.2 200 8 4 4 = − − 溶液中 沉淀的溶解损失为

2.盐效应(Effect of salts): 溶液中存在大量强电解质使沉淀溶解度增大的现象 讨论:K= =[M][AT] 而T一定,K为定值 当存在大量强电解质时,Ywy一K个 注:沉淀溶解度很小时,常忽略盐效应 沉淀溶解度很大,且溶液离子强度很 高时,要考虑盐效应的影响 2024/10/1
2024/10/1 2. 盐效应(Effect of salts): 溶液中存在大量强电解质使沉淀溶解度增大的现象 讨论: 注:沉淀溶解度很小时,常忽略盐效应 沉淀溶解度很大,且溶液离子强度很 高时,要考虑盐效应的影响 + − SP M A 当存在大量强电解质时, K [ ] [ ] 0 + − = = + − M A K K M A SP SP 而T一定,KSP 0 为定值
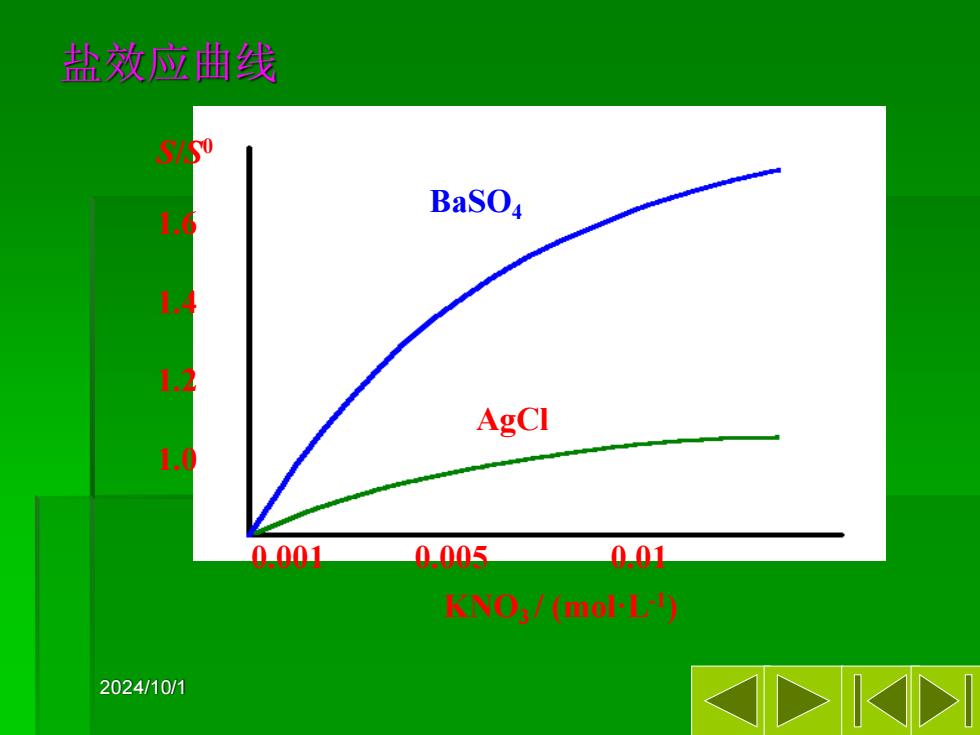
盐效应曲线 BaSOa AgCI 0.001 0.005 0.01 KNO:/(mol L9 2024/10/1
2024/10/1 盐效应曲线 S/S 0 1.6 1.4 1.2 1.0 0.001 0.005 0.01 KNO3 / (mol·L-1 ) BaSO4 AgCl

例3: 分别计算BaSO,在纯水和 0.01 ol/LNaNO3溶液中的溶解度 解 已知KyPo)=1.1x10-07s+=Yoi=0.67 BSO,在水中溶解度 S=VK(o,=V1.1×1010=1.0×1050l/L BaSO,在0.01ol1 LNaNO,溶液中溶解度 S= Ksp Baso 1.1×10-10 =1.57×10-5mol/L YBm2·yso V0.67×0.67 2024/10/1
2024/10/1 例3: 分别计算BaSO4在纯水和 0.01mol/LNaNO3溶液中的溶解度 解: 10 ( ) 1.1 10 4 − 已知KSP BaSO = 2 0.67 4 2+ = − = Ba SO S K mol L BaSO SP BaSO 1.1 10 1.0 10 / 1 0 5 4 4 − − = ( ) = = 在水中溶解度 mol L K S BaSO mol LNaNO Ba SO SP BaSO 1.57 10 / 0.67 0.67 1.1 10 0.01 / 5 0 1 0 4 3 2 4 2 4 − − = = = + − ( ) 在 溶液中溶解度

例4 PbS04在不同浓度Na,S04溶液中溶解度变化。 C(molL) 0 0.001 0.01 0.02 0.04 0.10 0.20 S(mmolL) 0.15 0.024 0.016 0.014 0.013 0.016 0.023 讨论: CNazSO =0~0.04m0l1L时,Cx,so,个,S%so,↓ 一同离子效应为主 Na,S >0.04m0l7L时,Ca,o.个,So.↑ 盐效应为主 2024/10/1
2024/10/1 例4: 讨论: 同离子效应为主 时, , = 2 4 2 4 4 0 ~ 0.04 / CNa SO mol L CNa SO SPbSO 盐效应为主 时, , 2 4 2 4 4 0.04 / CNa SO mol L CNa SO SPbSO PbSO4在不同浓度Na2 S O4溶液中溶解度变化。 C(mol/L) 0 0.001 0.01 0.02 0.04 0.10 0.20 S(mmol/L) 0.15 0.024 0.016 0.014 0.013 0.016 0.023