Na晶体中,n个3s轨道组成n条分子轨道。这n条分子轨 道之间能量差小,电子跃迁所需能量小。这些能量相近的能级组 成能带。能带的能量范围很宽,有时可达数百kJol一1。 能带如下图所示 Na的n个3s轨道,形成个Na金属的分子轨道一3s 能带。 3°满带导带和空带 以Li为例,1s22s12p° 1s轨道充满电子,故组成的能带充满电子,称为满带
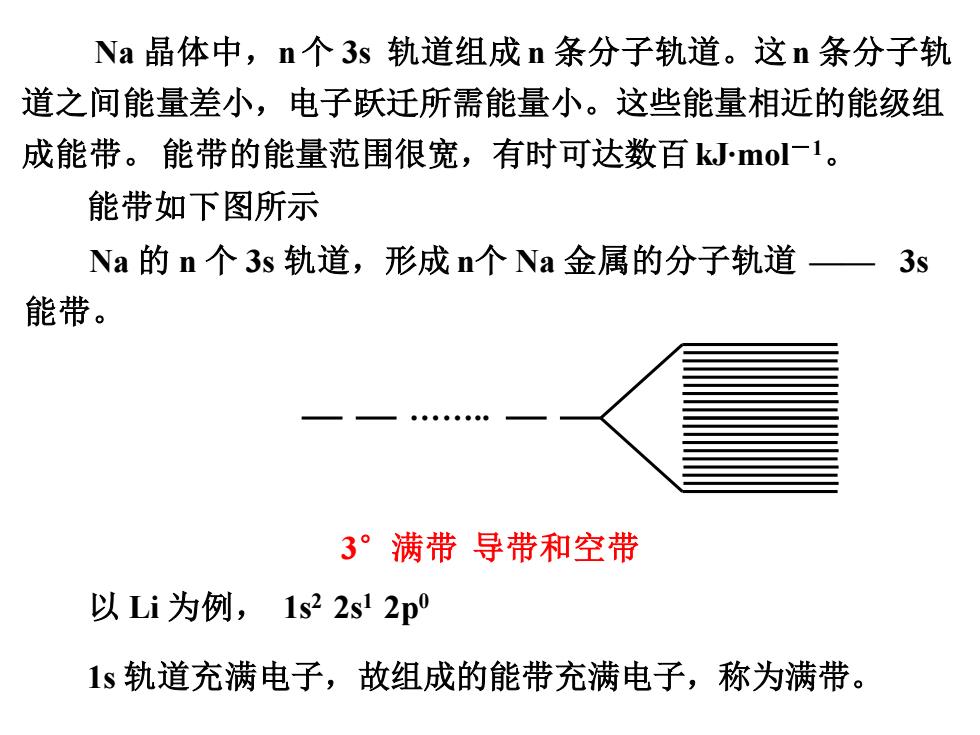
Na 晶体中,n 个 3s 轨道组成 n 条分子轨道。这n 条分子轨 道之间能量差小,电子跃迁所需能量小。这些能量相近的能级组 成能带。 能带的能量范围很宽,有时可达数百kJ∙mol-1 。 3°满带 导带和空带 以 Li 为例, 1s 2 2s1 2p0 1s 轨道充满电子,故组成的能带充满电子,称为满带。 Na 的 n 个 3s 轨道,形成 n个 Na 金属的分子轨道 —— 3s 能带。 . 能带如下图所示

2s轨道电子半充满,组成的能 带电子也半满,称为导带。 2p能带中无电子,称为空带。 从满带顶到导带底(或空带底) 3n个2p 的能量间隔很大,电子跃迁困难。 这个能量间隔称为禁带。 4°能带重叠 n个2s 相邻近的能带,有时可以重叠。 禁带 即能量范围有交叉。如Be的2s能带 和2p能带,可以部分重叠。 Be的2s能带是满带,通过重叠: .l 电子可以跃迁到2p空带中去。 n个1s
从满带顶到导带底( 或空带底 ) 的能量间隔很大,电子跃迁困难。 这个能量间隔称为禁带。 2s 轨道电子半充满,组成的能 带电子也半满,称为导带。 2p 能带中无电子,称为空带。 3n 个 2p n 个 2s 相邻近的能带,有时可以重叠。 即能量范围有交叉。如 Be 的 2s 能带 和 2p 能带,可以部分重叠。 Be 的 2s 能带是满带,通过重叠 电子可以跃迁到2p 空带中去。 4°能带重叠 n 个 1s 禁带