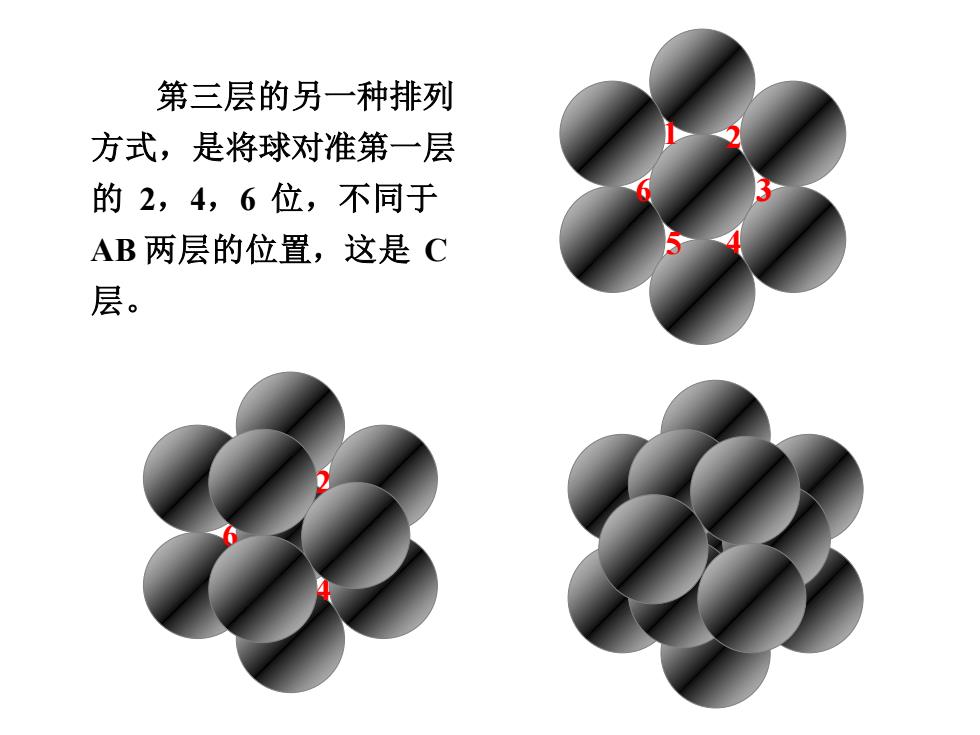
第三层的另一种排列 方式,是将球对准第一层 的2,4,6位,不同于 AB两层的位置,这是C 层
第三层的另一种排列 方式,是将球对准第一层 的 2,4,6 位,不同于 AB 两层的位置,这是 C 层。 1 2 3 5 4 6 1 2 3 5 4 6 1 2 3 5 4 6
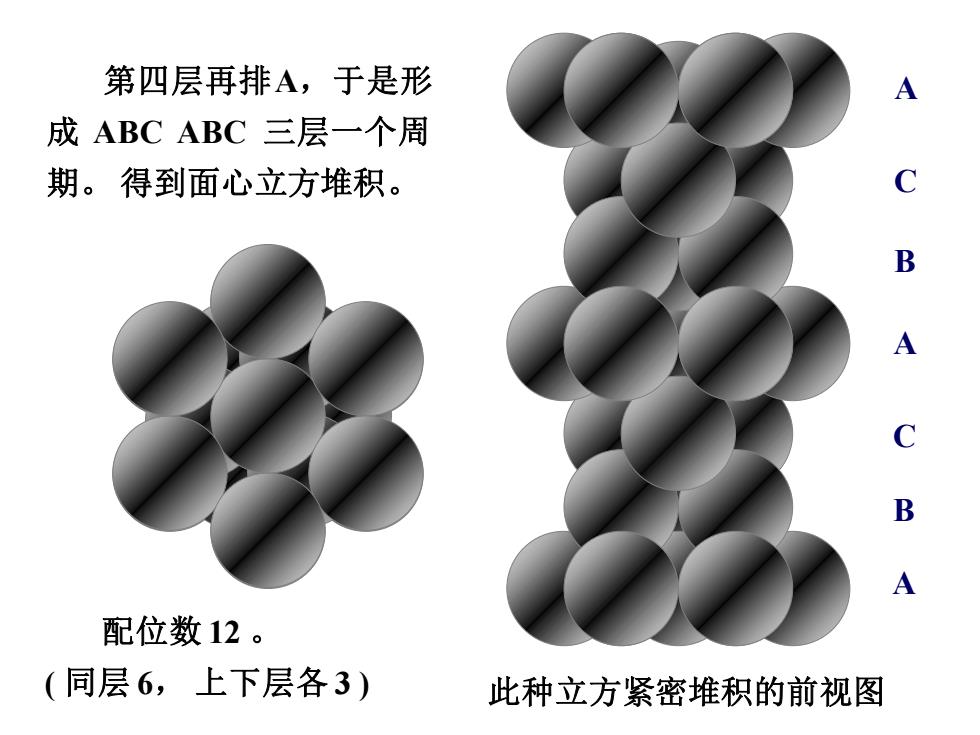
第四层再排A,于是形 A 成ABC ABC三层一个周 期。得到面心立方堆积。 B B A 配位数12。 (同层6,上下层各3) 此种立方紧密堆积的前视图
1 2 3 5 4 6 此种立方紧密堆积的前视图 A B C A A B C 第四层再排A,于是形 成 ABC ABC 三层一个周 期。 得到面心立方堆积。 配位数 12 。 ( 同层 6, 上下层各 3 )
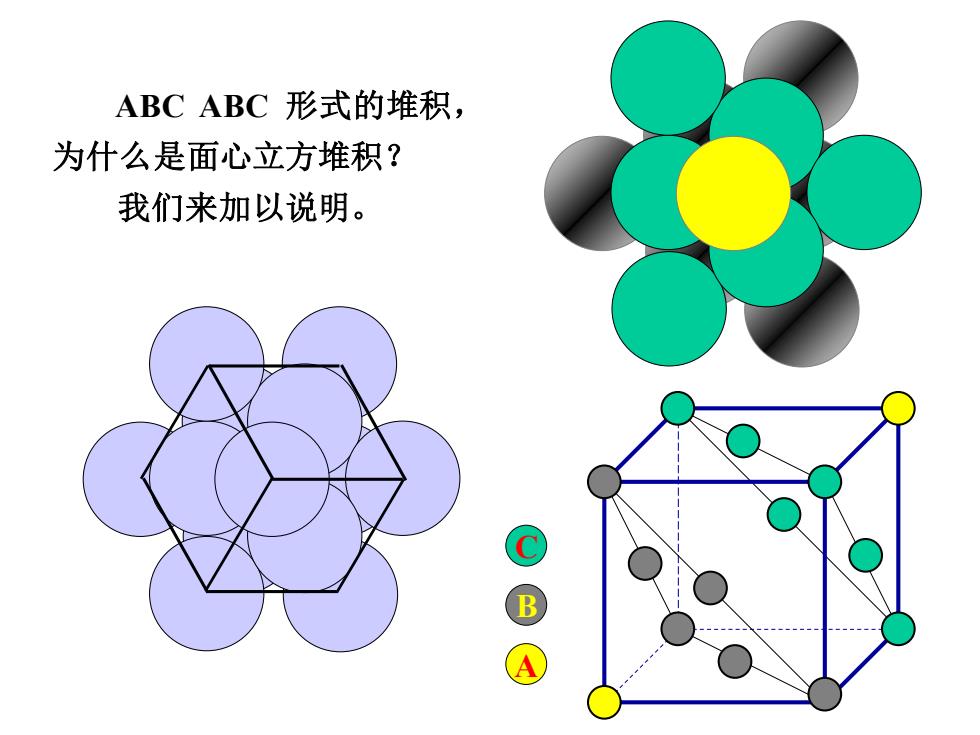
ABC ABC形式的堆积, 为什么是面心立方堆积? 我们来加以说明。 B
B C A ABC ABC 形式的堆积, 为什么是面心立方堆积? 我们来加以说明

这两种堆积都是最紧密堆积,空间利用率为74.05%。 还有一种空间利用率稍低的堆积方式,立方体心堆积:立方 体8个顶点上的球互不相切,但均与体心位置上的球相切。 配位数8,空间利用率为68.02%。 金属钾K的 立方体心堆积 六方紧密堆积 IIB,IVB 金属的 面心立方紧密堆积— 堆积方式 IB,Ni,Pd,Pt 立方体心堆积 IA,VB,VIB
这两种堆积都是最紧密堆积,空间利用率为 74.05%。 金属钾 K 的 立方体心堆积 还有一种空间利用率稍低的堆积方式,立方体心堆积:立方 体 8 个顶点上的球互不相切,但均与体心位置上的球相切。 配位数 8 ,空间利用率为 68.02% 。 六方紧密堆积 —— IIIB,IVB 面心立方紧密堆积—— IB,Ni,Pd, Pt 立方体心堆积 —— IA,VB,VIB 金属的 堆积方式
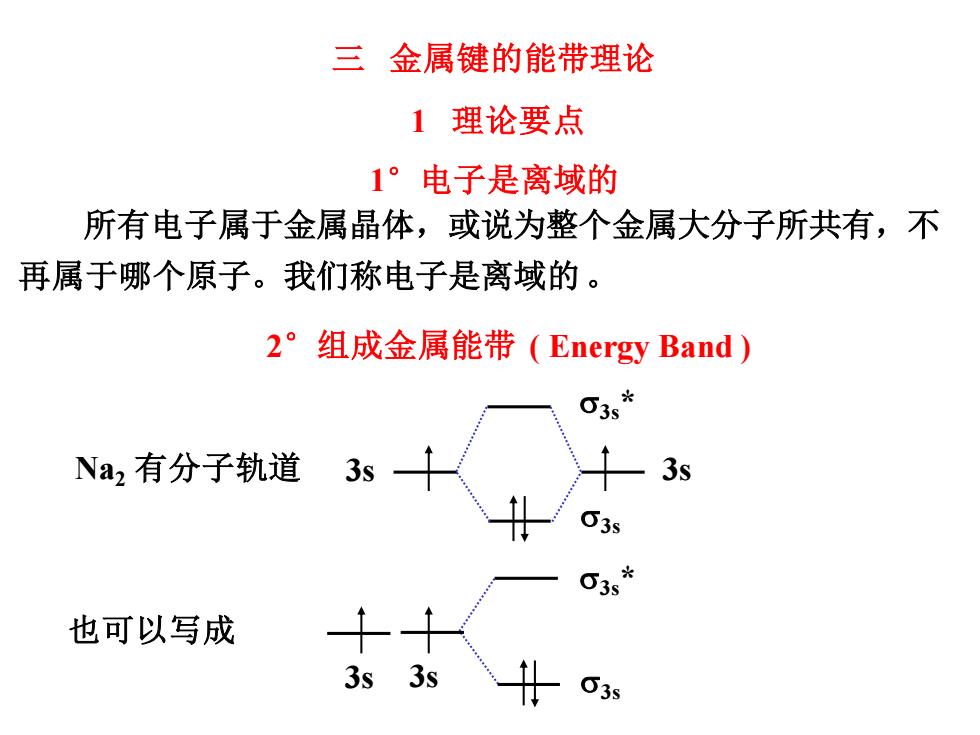
三 金属键的能带理论 1理论要点 1°电子是离域的 所有电子属于金属晶体,或说为整个金属大分子所共有,不 再属于哪个原子。我们称电子是离域的。 2°组成金属能带(Energy Band) Na2有分子轨道3s- —3s 63s 也可以写成 3s 3s 63s
三 金属键的能带理论 1 理论要点 1°电子是离域的 所有电子属于金属晶体,或说为整个金属大分子所共有,不 再属于哪个原子。我们称电子是离域的。 2°组成金属能带 ( Energy Band ) Na2 有分子轨道 3s 3s 3s 3s * 也可以写成 3s 3s 3s 3s *